Цветные металлы: 13 металлов, описание, свойства, где применяются и места добычи

Различные виды цветных металлов широко применяются в современных отраслях промышленности. Особенно они ценятся там, где требуется устойчивость изделий к использованию в агрессивных средах. Но как происходит деление на черные и цветные металлы? К последним относят те, в составе которых отсутствует железо. Групп таких материалов довольно много, а четкая классификация отсутствует.
В нашей статье мы расскажем про основные категории цветных металлов и поговорим о классификации их лома.
Получение цветных металлов
На то, чтобы добыть цветные металлы, уходит много сил и материальных ресурсов, так как они находятся в земле в небольшом количестве, а встретить их в чистом виде практически нереально.
Добытую руду отправляют на завод цветных металлов для дальнейшей переработки посредством особых технологий, включающих ряд металлургических процессов, таких как:
- Пирометаллургия. В этом случае металл получают и очищают при высоких температурах. Так изготавливают примерно 60 % цинка, весь свинец, около 95 % меди.
- Гидрометаллургия. Металл извлекают из руды, концентратов и отходов производства посредством применения химических реагентов с последующим выделением из водных растворов.
- Электрометаллургия. В основе получения металлов и их соединений лежит электролиз, то есть цветные металлы выделяют из растворов либо расплавов их соединений путем пропускания через них постоянного электрического тока. В частности, такую технологию применяют для получения алюминия.

Виды легких цветных металлов
Цветные металлы широко распространены в природе, отличаются прочностью, малой плотностью и высокой химической активностью. Добывать их начали еще в XIX в. Получают их посредством электролиза солей в расплавленном виде, электро- и металлотермии. Многие легкие цветные металлы применяют для производства сплавов.
Ниже рассмотрим виды легких цветных металлов.
Металл серебристого цвета с низкой плотностью и высокой прочностью, точка плавления – около +700 °С. В промышленности его используют в составе сплавов. Его без труда можно резать, пилить, сверлить, варить и гнуть.
Обычно его используют для образования сплавов с металлами, имеющими различные свойства, например, с медью, никелем, магнием и кремнием. Такие соединения очень прочные и стойкие к неблагоприятным погодным условиям. Алюминий обладает высокой тепло- и электропроводностью.
Цвет металла – серебристо-белый, на поверхности имеется окисная пленка. Магний отличается малой плотностью, но при этом хорошо поддается обработке, стоек к воздействию горючих веществ, таких как бензин, керосин, минеральные масла, но растворяется в кислотах. Не магнитен. Характеризуется малой упругостью и низкими литейными свойствами. Неустойчив к коррозии.
Немагнитный легкий металл серебристого цвета с голубым отливом. Имеет высокую прочность и устойчивость к коррозии. Среди недостатков можно выделить маленькую тепло- и электропроводность. При температуре свыше +400 °С титан утрачивает свои механические свойства, а при достижении +540 °С становится хрупким.
При соединении с такими металлами, как алюминий, марганец, хром, молибден и др., механические свойства титана увеличиваются. Такие сплавы отличаются друг от друга прочностью, в зависимости от легирующего металла. Титановые соединения широко востребованы в судо-, машино-, самолетостроении. Их используют в производстве ракетной техники, бытовых приборов и т.д.
Виды тяжелых цветных металлов
Сырьем для производства тяжелых цветных металлов служат сульфидные и окисленные полиметаллические руды. При этом могут использоваться различные производственные техники и способы, основная задача которых состоит в максимальном извлечении ценных компонентов из руды.
При обработке тяжелых цветных металлов используют технологии пиро- и гидрометаллургии. В результате этих процессов образуются черновые металлы, которые в дальнейшем рафинируются и используются в промышленности.
Распространенный тяжелый металл, обладающий высокой электро- и теплопроводностью, пластичностью.
Медь отлично соединяется с другими компонентами. Благодаря этому полученные сплавы широко используются в машиностроении.

Не все сплавы с содержанием цинка используются в промышленной сфере. Все дело в его хрупкости. Однако при нагревании до +150 °С он легко поддается ковке и прокатке. Цинк устойчив к коррозии, но разрушается при взаимодействии с кислотой и щелочью.
Имеет серый цвет, отдающий голубоватым оттенком. Точка его плавления – +327 °С. Свинец одновременно тяжелый и мягкий металл, отлично поддается ковке молотком, не затвердевая при этом. При литье принимает различные формы. Не поддается воздействию соляной, серной, уксусной и азотной кислот.
Латунь представляет собой соединения меди с цинком с добавлением таких металлов, как марганец, свинец, алюминий и др. При этом латунь дешевле меди, несмотря на то, что прочность, вязкость и антикоррозионные свойства выше. Металл обладает отличными литейными свойствами. Он поддается штамповке, раскатке, вытяжке и вальцовке. Из него производят гильзы для снарядов.
Виды малых цветных металлов
К цветным металлам также относят:
Сурьма – это металл серебристо-белого цвета с синеватым оттенком. Отличается особой хрупкостью, что позволяет раскрошить его даже при помощи пальцев рук.
Однако при соединении с другими металлами существенно увеличивает их твердость.
Сурьма пользуется популярностью не только в промышленности, но и в медицине – она является эффективным средством при лечении воспалений слизистой оболочки глаза.
Ртуть – это металл, находящийся в жидком агрегатном состоянии. На протяжении долгого времени используется в медицине (в градусниках), применяется в современных технологиях (в датчиках положения, в ионных двигателях).
Кадмий – белое вещество с металлическим отливом. Несмотря на свою особую твердость, без труда режется даже ножом. Имеет свойства, схожие со ртутью и цинком. В чистом виде ядовит для всего живого.

Виды легирующих цветных металлов
К ним относятся, например:
- молибден;
- вольфрам;
- кобальт;
- ванадий.
Молибден в чистом виде в природе не встречается. По прочности уступает вольфраму, однако более легко поддается обработке. В основном применяется в авиационной и ракетной промышленных отраслях.
Вольфрам – один из наиболее тугоплавких и плотных металлов, имеет серебристо-белый цвет, внешне похож на платину. Он широко применяется в производстве различных режущих инструментов, ювелирных изделий, деталей для самолетов и ракет, боеприпасов.
Кобальт имеет серебристый цвет с желтым или синим отливом. Сплавы с его преобладанием используют при изготовлении различных медицинских деталей и инструментов.
Ванадий – высокопластичный металл серебристо-белого цвета, который активно используют в автомобилестроении, так как он существенно повышает антикоррозионные и механические свойства стали.
Благородные цветные металлы
К таковым относят:
- золото;
- серебро;
- платину.
Золото – металл, обладающей чрезвычайной химической стойкостью. Его не получится окислить даже в расплавленном виде – растворяется только под воздействием состава из соляной и азотной кислот. Отличается высокими показателями текучести, отлично поддается обработке. Цена на бирже цветных металлов за 1 г составляет 2 450 руб.
Серебро – металл, отличающийся пластичностью, высокой электро- и теплопроводимостью, хорошо поддается ковке, не окисляется под воздействием О2.
Платина особенно популярна среди ювелиров, используется ими в чистом виде. Отличается антикоррозийностью и высокой стойкостью к различным химическим реактивами деформациям. В ломбарде 1 г платины стоит 1 600 рублей.
Виды редких цветных металлов
К таким металлам относят:
Тантал – твердый и плотный металл серебристого оттенка, однако хорошо поддающийся обработке. Основные отрасли его применения – металлургическая, химическая и ядерная.
Ниобий – серое вещество со стальным отливом. Отличается особой тугоплавкостью и парамагнитными свойствами. Используется в авиации и радиотехнической отрасли.

Виды и маркировка лома цветных металлов
Некоторые виды лома цветных металлов могут быть переработаны с целью их вторичного использования.
В таблице ниже представлен список металлов и количество видов лома к каждому из них.
| Название металла | Количество видов лома |
| Алюминий | 32 |
| Вольфрам | 17 |
| Кадмий | 2 |
| Кобальт | 3 |
| Магний | 8 |
| Медь | 13 |
| Латунь | 23 |
| Бронза | 15 |
| Молибден | 9 |
| Свинец | 11 |
| Ртуть | 6 |
| Олово | 10 |
| Никель | 26 |
В пункты по приему вторичного сырья чаще всего сдают сплавы цветных металлов. Принадлежность к тому либо иному виду металла определяют по преобладающему в сплаве элементу в процентном соотношении. Оценка происходит посредством применения особого оборудования.
Лом цветных металлов принято делить на группы в зависимости от:
- происхождения;
- химических составляющих;
- физического состояния материала на момент сдачи.
Цветной металл становится ломом, если:
- обнаружен брак;
- списан в отходы промышленного производства;
- является некондиционным;
- стал скрапом готовой продукции.
Химические составляющие лома возможно определить только в лаборатории, именно после этого можно верно сказать, к какому металлу либо сплаву он относится.
Наиболее ценным вторичным сырьем являются нелегированные металлы, содержащие примеси в незначительном количестве. Однако физические параметры скрапа не имеют такую же важность, как и химические.
В соответствии с этими характеристиками виды лома цветных металлов принято делить таким образом:
- класс А – лом и куски отходов;
- класс Б – стружка, проволока и небольшие кусковые отходы;
- класс В – отходы в виде порошка (встречаются нечасто, обычно у определенных металлов, среди которых вольфрам, молибден, кобальт и титан).
- класс Г – остальные виды вторичного сырья.
Весь цветной скрап проходит тщательную проверку на:
- загрязнения химического и радиационного типа;
- степень взрывоопасности.
После ее проведения выдается сертификат, подтверждающий безопасность лома. Без данного документа дальнейшая транспортировка невозможна.

Насыщенность лома вредными веществами не должна превышать норму, установленную ГОСТом 12.1.005.
Министерство природных ресурсов и экологии РФ различает пять классов цветного металлолома, представляющих химическую, радиационную и взрывоопасность. Это скрап:
- Опасный для экологической среды. К таким отходам относят ртуть, а также плутоний и полоний.
- Имеющий высокую опасность, на выведение последствий от применения которого необходимо 30 лет. К нему относят сплавы таких металлов, как свинец, молибден и кобальт.
- Имеющий умеренную опасность, после применения которого на восстановление экологии нужно 10 лет. К нему относят лом с примесями таких металлов, как медь, железо, цинк, никель, алюминий и серебро.
- Имеющий малую опасность, на выведение последствий от применения которого необходимо 3 года. К данному классу относится бронза.
- С низким уровнем опасности, который не наносит ущерб экосистеме. Сюда входит большинство видов лома цветных металлов.
Пункты приема металлолома обязаны иметь лицензию. Эта необходимость обуславливается тем, что цветмет представляет опасность для людей и экологической среды. ГОСТ регулирует определение сортов лома в соответствии с обозначенными параметрами качества.
При этом берутся во внимание некоторые характеристики, присущие скрапу, среди которых:
- величина;
- происхождение;
- степень однородности;
- процент засора;
- химические составляющие;
- физический износ;
- габаритные размеры.
Представительная проба позволяет выявить качество лома. Во время его транспортировки обязательным требованием является маркировка, содержащая следующую информацию:
- наименование;
- обозначение в соответствии с ГОСТом;
- вид вторичного сырья;
- марка сплава.
Маркировка должна быть надежно прикреплена к грузу при транспортировке и хранении.
Для определения марки металла нужно только заглянуть в специальный документ – марочник, который содержит информацию обо всех маркировках интересующего вас металла либо сырья.
Мы с уважением относимся ко всем клиентам и одинаково скрупулезно выполняем задания любого объема.
Наши производственные мощности позволяют обрабатывать различные материалы:
- цветные металлы;
- чугун;
- нержавеющую сталь.
При выполнении заказа наши специалисты применяют все известные способы механической обработки металла. Современное оборудование последнего поколения дает возможность добиваться максимального соответствия изначальным чертежам.
Для того чтобы приблизить заготовку к предъявленному заказчиком эскизу, наши специалисты используют универсальное оборудование, предназначенное для ювелирной заточки инструмента для особо сложных операций. В наших производственных цехах металл становится пластичным материалом, из которого можно выполнить любую заготовку.
Преимуществом обращения к нашим специалистам является соблюдение ими ГОСТа и всех технологических нормативов. На каждом этапе работы ведется жесткий контроль качества, поэтому мы гарантируем клиентам добросовестно выполненный продукт.
Благодаря опыту наших мастеров на выходе получается образцовое изделие, отвечающее самым взыскательным требованиям. При этом мы отталкиваемся от мощной материальной базы и ориентируемся на инновационные технологические наработки.
Мы работаем с заказчиками со всех регионов России. Если вы хотите сделать заказ на металлообработку, наши менеджеры готовы выслушать все условия. В случае необходимости клиенту предоставляется бесплатная профильная консультация.
Цветные металлы: список, названия, классификация и использование :
Ведущей отраслью в экономике нашей страны является металлургия. Для успешного ее развития нужно много металла. В данной статье речь пойдет о цветных тяжелых и легких металлах и их использовании.
Классификация цветных металлов
В зависимости от физических свойств и назначения, они подразделяются на такие группы:
- Легкие цветные металлы. Список этой группы большой: в ее состав входит кальций, стронций, цезий, калий, а также литий. Но в металлургической промышленности чаще всего используются алюминий, титан и магний.
- Тяжелые металлы пользуются большой популярностью. Это всем известные цинк и олово, медь и свинец, а также никель.

- Благородные металлы, такие как платина, рутений, палладий, осмий, родий. Золото и серебро широко применяются для изготовления украшений.
- Редкоземельные металлы — селен и цирконий, германий и лантан, неодим, тербий, самарий и другие.
- Тугоплавкие металлы — ванадий и вольфрам, тантал и молибден, хром и марганец.
- Малые металлы, такие как висмут, кобальт, мышьяк, кадмий, ртуть.
- Сплавы – латунь и бронза.
Легкие металлы
Они имеют широкое распространение в природе. Эти металлы обладают маленькой плотностью. У них высокая химическая активность. Они представляют собой прочные соединения.
Металлургия этих металлов начала развиваться в девятнадцатом веке. Их получают путем электролиза солей в расплавленном виде, электротермии и металлотермии.
Легкие цветные металлы, списоккоторых имеет много пунктов, используются для производства сплавов.
Алюминий
Относится к легким металлам. Имеет серебристый цвет и точку плавления около семисот градусов. В промышленных условиях используется в сплавах. Он применяется везде, где нужен металл. У алюминия плотность низкая, а прочность – высокая. Этот металл легко режется, пилится, сваривается, сверлится, паяется и сгибается.

Сплавы образует с металлами различных свойств, такими как медь, никель, магний, кремний. Они обладают большой прочностью, не ржавеют при неблагоприятных погодных условиях. У алюминия высокая электро- и теплопроводность.
Магний
Он относится к группе легких цветных металлов. Имеет серебристо-белый цвет и пленочное окисное покрытие. Обладает маленькой плотностью, хорошо обрабатывается. Металл устойчив к воздействию горючими веществами: бензином, керосином, минеральными маслами, но подвержен растворению в кислотах. Магний не магнитен. Обладает низкими упругими и литейными свойствами, подвергается коррозии.
Титан
Это легкий металл. Он не магнитен. Имеет серебристый цвет с отливом голубоватого тона. Обладает высокой прочностью и устойчивостью к коррозии. Но у титана маленькая электропроводность и теплопроводность. Теряет механические свойства при температуре 400 градусов, приобретает хрупкость при 540 градусах.

Механические свойства титана повышаются в сплавах с молибденом, марганцем, алюминием, хромом и другими. В зависимости от легирующего металла, сплавы имеют разную прочность, среди них есть и высокопрочные. Такие сплавы применяются в самолетостроении, машиностроении, судостроении. Из них производят ракетную технику, бытовые приборы и многое другое.
Тяжелые металлы
Тяжелые цветные металлы, список которых весьма широк, получают из сульфидных и окисленных полиметаллических руд. В зависимости от их типов, методы получения металлов отличаются по способу и сложности производства, в процессе которого должны полностью извлекаться ценные составляющие сырья.
Металлы этой группы бывают гидрометаллургическими и пирометаллургическими. Полученные любым методом металлы называются черновыми. Они подвергаются процедуре рафинирования. Только после этого их можно использовать в промышленных целях.
Цветные металлы, список которых представлен выше, в промышленности используются не все. В данном случае речь идет о распространенном тяжелом металле – меди. У нее высокая теплопроводность, электропроводность и пластичность.

Сплавы меди нашли широкое применение в такой отрасли промышленности, как машиностроение, а все благодаря тому, что этот тяжелый металл хорошо сплавляется с другими.
Он тоже представляет цветные металлы. Список названий большой. Однако далеко не все тяжелые цветные металлы, к которым относится цинк, используются в промышленности. Этот металл хрупкий.
Но если нагреть его до ста пятидесяти градусов, он будет без проблем коваться и с легкостью прокатываться.
У цинка высокие антикоррозионные свойства, но он поддается разрушению при воздействии щелочью и кислотой.
Свинец
Список цветных металлов будет неполным без свинца. Он серого цвета с проблеском голубого оттенка. Температура плавления составляет триста двадцать семь градусов. Он тяжелый и мягкий. Хорошо куется молотком, при этом не твердеет. Из него выливают различные формы. Устойчив к воздействию кислот: соляной, серной, уксусной, азотной.
Латуни
Это сплавы из меди и цинка с добавлением марганца, свинца, алюминия и других металлов. Стоимость латуни меньше, чем меди, а прочность, вязкость и коррозионная стойкость – выше. У латуни хорошие литейные свойства. Из нее производят детали путем штамповки, раскатки, вытяжки, вальцовки. Из этого металла делают гильзы для снарядов и многое другое.
Использование цветных металлов
Цветными называют не только сами металлы, но и их сплавы. Исключение составляет так называемый «чермет»: железо и, соответственно, его сплавы. В странах Европы цветные металлы носят название нежелезистых.
Цветные металлы, список которых немаленький, нашли широкое применение в разных отраслях во всем мире, в том числе и в России, где являются основной специализацией. Производятся и добываются на территориях всех регионов страны.
Легкие и тяжелые цветные металлы, список которых представлен большим разнообразием наименований, составляют отрасль промышленности под названием «Металлургия». Это понятие включает в себя добычу, обогащение руд, выплавку как металлов, так и их сплавов.

В настоящее время отрасль цветной металлургии получила широкое распространение. Качество цветных металлов очень высокое, они отличаются долговечностью и практичностью, применяются в строительной индустрии: ими отделывают здания и сооружения. Из них производят профильный металл, проволоку, ленты, полосы, фольгу, листы, прутки различной формы.
Особенности цветных металлов и сплавов
Цветные металлы и сплавы известны людям давно. Кузнецы постоянно старались получить новые материалы, соединяя уже известные. Так появлялись новые соединения, которые обладали разными характеристиками. Они используются в разных направлениях промышленности.

Цветные металлы и сплавы
История открытия
Цветные металлы и их сплавы появлялись постепенно. После каменного века настала пора меди. Этот материал использовали для разных целей: изготавливали посуду, делали наконечники к орудиям труда, оружию. Век меди сменился эпохой бронзы. Это был первый сплав — соединение меди и свинца. Постепенно бронзу заменило железо.
С развитием металлургии, осваиванием новых земель, развитием торговли начали появляться драгоценные металлы. Изначально более популярным было серебро, а не золото. Из-за того что, средние века были эпохой войн, сражений, рыцарства, кузнецы искали новые материалы для изготовления доспехов, оружия. Так появлялись новые смеси.
Характеристики и маркировка
К цветным относятся все металлы, кроме тех, которые изготавливаются на основе железа. Они применяются в различных сферах промышленности. Чтобы различать материалы между собой, была создана специальная маркировка. По ней можно определить механические свойства сплавов, температуру расплавления, прочность и другие параметры.
Маркировка разных видов цветных металлов:
- Медь и соединения на её основе. Главный материал обозначается буквой «М». После буквы пишут цифры, которые обозначают чистоту металла. На конце маркировки могут указываться дополнительные буквы. К — обозначает катодный, Б — бескислородный, Р — раскисленный. Если речь идёт о соединении, легирующие добавки обозначаются заглавными буквами дополнительных компонентов.
- Латунь — чистый сплав, обозначающийся буквой «Л», после которой указывается две цифры. Это обозначение содержания меди. Многокомпонентная латунь в своей маркировке имеет дополнительные буквы, указывающие на наличие легирующих компонентов. Далее пишутся цифры, между которыми ставятся прочерки. Первая из них указывает на содержание меди, остальные на количество легирующих добавок по процентам.
- Бронза маркируется буквами «Бр». Если на поверхности изделий из этого материала присутствует буква «Л», это означает что он является литейным.
- Алюминий — материал, который обозначается буквой «А». После неё указываются цифры, которые говорят о количестве содержащихся примесей. Буква «Л» стоящая после указания на алюминий обозначает его литейные качества. Буква «В» говорит о высокой прочности материала.
Остальные цветные металлы и соединения на их основе имеют похожую маркировку. Легирующие добавки обозначаются начальными буквами.
Способы получения
Однородные материалы, смеси на их основе получаются по специальным технологиям. К ним относятся:
- Пирометаллургия — ряд технологический процессов, при которых происходит очистка, получение металлов их соединение под воздействием высокой температуры. По этой технологии изготавливается около 60% цинка, 100% свинца, 95% меди.
- Гидрометаллургия — технология получения металлов из руд с помощью химических растворов. Последующие этапы обработки подразумевают отделение основных компонентов от жидкости.
- Электрометаллургия — совокупность технологических операций, при которых материалы и соединения на их основе получаются под воздействием электрического тока. С помощью этой технологии чаще всего получают алюминий.

Добыча металла
Сферы применения
Цветные металлы и сплавы на их основе используются в различных направлениях промышленности. Из них изготавливают:
- Детали для электрооборудования, электроинструментов.
- Теплообменники, трубопроводы.
- Ювелирные изделия.
- Изготовление высоконагруженных деталей из титана.
- Провода, связывающие элементы для прохождения электрического тока.
- Проволоку, листы, прутья, арматура, крепёж.
Разновидности
Существуют основные сплавы цветных металлов, о которых следует поговорить более подробно. Они применяются чаще всего.
Алюминий и его сплавы
Алюминий — серебристый материал, который хорошо проводит электрический ток, имеет малую удельную массу, низкую температуру плавления. От коррозии он защищен оксидной плёнкой, которая образуется на его поверхности после взаимодействия с кислородом. Соединения на основе этого материала бывают двух типов.

Сплав алюминия
Деформируемые сплавы алюминия
Бывают упрочняемые и неупрочняемые:
- К первой группе относятся дюралюминий, смеси с высоким показателем прочности.
- Ко второй группе относятся соединения на основе алюминия, к которому добавляется магний или марганец.
Химический состав деформируемых алюминиевых сплавов зависит от группы. Упрочняемые соединения могут дополняться легирующими добавками.
Литейные сплавы на основе алюминия
Алюминиевые литейные сплавы называют силуминами. Это соединение основного металла и кремния. Обладают подобные соединение малой удельной массой, высокими литейными свойствами.
Сплавы на основе меди
Медь — материал красного оттенка. Имеет высокий параметр электропроводности, пластичности. Хорошо обрабатывается, однако имеет низкие литейные характеристики. Основным соединения на основе меди — бронза, латунь.
Бронза
Представляет собой смесь на основе меди, легирующими компонентами которой могут быть любые металлы кроме цинка.
Латунь
Соединение меди, цинка и других легирующих добавок. Дополнительных компонентов в составе — не более 8%.
Магний и его сплавы
Магний — металл серебристого оттенка. Плавится при низкой температуре, устойчив к развитию коррозии. Его не используют для конструкционных целей, так как материал обладает низкими механическими параметрами.

Магний
Деформируемые сплавы магния
К деформируемым соединениям на основе магния относятся:
- Смеси с марганцем — не более 2,5%.
- Смесь цинка, магния, алюминия, марганца.
- Соединения магния, цинка, циркония, кадмия.
Литейные сплавы магния
Смесь цинка, магния, алюминия применяется при изготовлении деталей для автомобилей, самолётов, кораблей, ракет. Такие материалы отличаются высокими механическими параметрами.
Цинк и его сплавы
Цинк — металл серых оттенков, с высокими параметрами пластичности, вязкости. Устойчив к воздействию влаги. Существует две группы соединений на основе цинка.
Деформируемые цинковые сплавы
Соединения цинка с алюминием, магнием, медью. Изготавливаются в процессе прокатки, опрессовывания, вытяжки. Во время проведения технологических операций отдельные компоненты нагреваются до 300 градусов. Готовые смеси имеют высокие показатели пластичности, прочности.
Литейные цинковые сплавы
Соединения цинка, меди, магния, алюминия. Обладают высоким показателем текучести. Из готовых соединений изготавливаются корпуса для различных приборов, измерительной аппаратуры.
Изделия
Цветных металлов и смесей на их основе огромное множество. Благодаря этому из них изготавливаются различные изделия:
- крепёж, строительные материалы;
- детали для электрооборудования;
- соединительные элементы, провода, проволока, арматура, прутья, листы;
- ювелирные украшения;
- декоративные элементы для интерьера;
- монеты, слитки;
- статуэтки, элементы часов.
Цветные металлы и сплавы на их основе популярны в разных направлениях промышленности. Чтобы эффективнее работать с этими материалами, нужно знать их параметры. Это поможет избежать брака, сделать качественное изделие. Цветные металлы дороже черных, что делает их более ценными для производства.

Цветная металлургия
Цветная металлургия – это не только комплекс мероприятий по получению цветных металлов (добыча, обогащение, металлургический передел, получение отливок чистых металов и сплавов на их основе), но и переработка лома цветных металлов.
Научно-технический прогресс не стоит на месте, и цветные металлы на сегодняшний день широко используются для разработки инновационных конструкционных материалов. Только отечественная металлургическая промышленность выпускает порядка 70 видов сплавов, используя разнообразное сырье.
В связи с низким содержанием необходимого компонента в руде и примесей других элементов, цветная металлургия является энергозатратным производством и имеет сложную структуру. Так, меди в руде содержится не более 5%, а цинка и свинца не более 5,5%. Колчеданы, добываемые на Урале, многокомпонентные, и в их составе находится порядка 30 химических элементов.

Цветные металлы подразделяются на шесть категорий, согласно своим физическим свойствам и предназначению:
- Тяжелые. Имеют высокую плотность, соответственно, и вес. К ним относятся Cu, Ni, Pb, Zn, Sn.
- Легкие. Имеют малый вес из-за незначительной удельной плотности. К ним относятся: Al, Mg, Ti, Na, Ka, Li.
- Малые: Hg, Co, Bi, Cd, As, Sb.
- Легирующие. В основном используются для получения сталей и сплавов с необходимыми качествами. Это W, Mo, Ta, Nb, V.
- Благородные. Широко известны и используются для изготовления ювелирных украшений. Среди них Au, Ag, Pt.
- Редкоземельные, рассеянные: Se, Zr, Ga, In, Tl, Ge.
Специфика отрасли
Руды цветных металлов, как было выше сказано, содержат малое количество добываемого элемента. Поэтому на тонну той же меди необходимо до 100 т руды. Из-за большой потребности в сырье цветная металлургия, по большей части, располагается вблизи своей сырьевой базы.
Цветные руды для своей переработки требуют большого количества топлива или электроэнергии. Энергетические затраты достигают половины общих затрат, связанных с выплавкой 1 т металла. В связи с этим металлургические предприятия располагаются в непосредственной близости от производителей электроэнергии.
Производство редких металлов в основном основано на восстановлении из соединений. Сырье поступает с промежуточных этапов обогащения руд. Из-за небольших объемов и трудности производства получением редких металлов занимаются лаборатории.
Состав отрасли
Виды цветной металлургии включают в себя отрасли, связанные с получением определенных видов металлов. Так, укрупнено можно выделить следующие отрасли:
- производство меди;
- производство алюминия;
- производство никеля и кобальта;
- производство олова;
- производство свинца и цинка;
- добыча золота.
Получение никеля тесно связано с местом добычи никелевых руд, которые расположены на Кольском полуострове и в Норильском районе Сибири. Многие отрасли цветной металлургии отличаются многоступенчатым металлургическим переделом промежуточных продуктов.

На этом основании эффективен комплексный подход. Это сырье для получения других сопутствующих металлов. Утилизация отходов сопровождается получением материалов, использующихся не только в других отраслях тяжелого машиностроения, но и в химической и строительной отраслях.
Основными этапами получения чистой меди являются выплавка черновой меди и ее дальнейшее рафинирование. Черновая медь добывается из руд, а низкая концентрация меди в уральских медных колчеданах и большие ее объемы не позволяют перенести производственные мощности с Урала. В качестве резерва выступают: медистые песчаники, медь-молибденовые, медь-никелевые руды.
Рафинирование меди и переплавка вторичного сырья производится на предприятиях, которые удалены от источников добычи и первичной плавки. Благоприятствует им низкая стоимость электричества, так как для получения тонны меди расходуется до 5 кВт энергии в час.

Утилизация сернистых газов с последующей переработкой послужила стартом для получения серной кислоты в химической промышленности. Из остатков апатитов производит фосфатные минеральные удобрения.
Получение свинца и цинка
Металлургия цветных металлов, таких как свинец и цинк, имеет сложную территориальную разобщенность. Добычу руды ведут на Северном Кавказе, в Забайкалье, Кузбассе и на Дальнем Востоке. А обогащение и металлургический передел проводится не только возле мест выемки руды, но и на других территориях с развитой металлургией.
Свинцовые и цинковые концентраты богаты на химическую элементную базу. Однако сырье имеет разное процентное содержание элементов, из-за чего не всегда цинк и свинец можно получить в чистом виде. Поэтому технологические процессы в районах различны:
- В Забайкалье получают только концентраты.
- На Дальнем Востоке получают свинец и цинковый концентрат.
- На Кузбассе получают цинк и свинцовый концентрат.
- На Северном Кавказе ведут передел.
- На Урале производят цинк.
Металлургия легких металлов
Наиболее распространенным легким металлом является алюминий. Сплавы на его основе обладают свойствами, присущими конструкционным и специальным сталям.
Для получения алюминия сырьем являются бокситы, алуниты, нефелины. Производство разделено на две стадии:
- На первой стадии получают глинозем и необходим большой объем сырья.
- На второй стадии электролитическим методом производят алюминий, на что требуется недорогая энергия. Поэтому этапы производства находятся на разных территориях.
Получение алюминия и сплавов сосредоточено в промышленных центрах. Сюда же поставляется лом на вторичную переработку, что в итоге снижает себестоимость готовой продукции.
Цветные металлы: применение и особенности обработки
Сегодня цветные металлы очень много значат в производстве современной техники. Металл, с точки зрения химии — простое вещество, обладающее способностью проводить тепло и электричество. Его поверхность имеет характерный блеск.
Металлы классифицируют по разным критериям, тем не менее, среди них выделяют три основные группы:
- черные;
- цветные;
- благородные (драгоценные).
Цветные металлы — понятие, включающее металлы и сплавы (исключением является железо, относящееся к черным металлам). Они очень востребованы на территории России, поэтому их производством занимаются во многих регионах страны.
Прежде всего, детали из цветных металлов отличаются от других металлоизделий своей стоимостью. Ограниченные запасы и сложности добычи материала — вот основные аспекты, объясняющие различия в цене.
К тому же, детали из цветных металлов характеризуются уникальными свойствами, причем, как физическими, так и химическими: мягкостью, пластичностью, энергопроводимостью.
Данная группа включает в себя большое количество металлов, отличающихся друг от друга, в первую очередь по внешнему виду, а потом уже по своим характеристикам.
Отрасль металлургии, специализирующаяся на добыче, обогащении руд, выплавке цветных металлов, называется цветной металлургией.
В РФ имеется несколько баз цветной металлургии, различающихся между собой отличиями географии легких/тяжелых металлов. Легкими металлами занимается титано-магниевая и алюминиевая промышленности, а тяжелыми — оловянная, никель-кобальтовая, свинцово-цинковая и медная.
Основные металлы
Алюминий — металл, характеризующийся высокой электропроводностью, прекрасной пластичностью и, вместе с тем, низкими механическими свойствами. При этом различают первичный и вторичный алюминий
Медь — наиболее распространенный цветной металл, обладающий великолепной электро- и теплопроводностью, а также пластичностью. На основе данного материала создается множество сплавов, широко используемых в машиностроении. Это обусловлено свойством меди хорошо сплавляться с другими металлами.
Еще один основной цветной металл — цинк. При температуре окружающей среды он достаточно хрупкий, однако если его нагреть до 100-150 оС, он замечательно поддается обработке ковкой и прокатом. Цинк обладает антикоррозионными свойствами, но при воздействии щелочей и кислот начинает разрушаться. Его температура плавления — 419 оС.
Сфера применения
Популярность цветных металлов ежегодно возрастает. Этому способствует динамичное развитие ракетной/атомной техники, авиастроения, химической промышленности, где в качестве конструкционных материалов используется титан, цирконий, молибден, никель, гафний и прочее.
Область применения отдельных металлов довольно разнообразна:
- медь и сплавы на ее основе востребованы на предприятиях химического машиностроения. Из этих материалов выполняются трубопроводы, сосуды для криогенной техники;
- алюминий пользуется особым спросом в химической/пищевой промышленности (из него изготавливают всевозможные емкости). В авиа- и судостроительстве этот металл популярен благодаря высокой прочности при небольшой плотности, стойкостью к коррозии и отличных механических свойств при температурах ниже нуля.
Особенности
Детали из цветных металлов получают различными способами. Здесь может быть применена и механическая обработка, и сварка, и множество других технологий. Выбирая ту или иную методику, нужно принять во внимания отличительные особенности обрабатываемого материала.
Магний, медь и алюминий, характеризуются прекрасными показателями теплопроводности и теплоемкости, которые способствуют быстрому охлаждению участков сварки.
Следовательно, чтобы сварить такой материал, потребуются мощные источники теплоты, а может и дополнительный подогрев детали. Более того, у этих металлов при нагреве резко ухудшаются механические свойства.
От этого они легче разрушаются от ударов, а под действием собственного веса может даже провалиться сварочная ванна.
При нагреве больших объемов цветных сплавов они на химическом уровне начинают взаимодействовать практически со всеми газами (исключение составляют инертные), а также растворяют атмосферные газы.
В этом плане наиболее активными являются тугоплавакие металлы, такие как:
- цирконий и молибден;
- тантал и титан.
Средства защиты
Цветные металлы, как было отмечено ранее, прочны, долговечны и способны запросто переносить воздействие высоких температур. Они обладают лишь одним изъяном — под воздействием кислорода эти металлы корродируют.
- Наиболее действенный способ, позволяющий уберечь цветной металл от атмосферной коррозии — нанесение специальных лакокрасочных покрытий. Для защиты металлической поверхности разработаны следующие средства:
- • грунтовка; • краска;
- • «3 в 1».
Грунтовка является основным средством борьбы с окислением металла. Однослойное грунтование выполняется перед окрашиванием поверхности, улучшая адгезию к основанию.
Обработка металлов — процесс, сопряженный со множеством нюансов, поэтому качественно выполнить задачу такого характера под силу лишь опытным профессионалам, способным находить правильный выход из самых непредсказуемых ситуаций. Доверившись им, можно быть уверенным, что они выполнят все именно так, как того требует заказчик.
Цветные металлы: понятие, область использования, особенности обработки

Любой металл можно описать как вещество с характерным металлическим блеском, несложного химического состава, с хорошей ковкостью, электро- и теплопроводностью.
Группы металлов:
- Черные – железо и железные сплавы;
- Цветные – не содержащие железо, а также их сплавы;
- Благородные – золото, серебро, металлы платиновой группы;
- Легкие – металлы малой плотности;
- Тяжелые – имеющие плотность больше плотности железа.
Цветные металлы
Делятся на подгруппы по различным признакам:
- Легкие – магний, титан, алюминий
- Тяжелые – медь, цинк, олово, никель, свинец;
- Благородные — золото, серебро, металлы платиновой группы;
- Тугоплавкие – плохо поддающиеся термообработке;
- Рассеянные – встречаются в виде примесей в минералах. в данную группу входят рубидий, таллий, галлий, индий, скандий, германий и другие;
- Редкоземельные – 17 элементов, в том числе иттрий, скандий, лантан и лантаноиды. Залежи встречаются нечасто, но запасы сырья в месторождениях достаточны.
- Радиоактивные – излучают во внешнюю среду потоки элементарных частиц.
Естественными (природными) радиоактивными считаются уран, полоний, радий, торий, актиний, протактиний. Искусственные образцы созданы человеком.
Цветные металлы вырабатываются в огромном количестве благодаря их востребованности в промышленности. Цветная металлургия охватывает работы по добыче и обогащению руд, выплавке чистых металлов и получению сплавов. Отрасль делится на легкую металлургию и металлургию тяжелых цветных металлов. В РФ хорошо развита алюминиевая, титано-магниевая, медная, цинковая, никель-кобальтовая промышленность.
Цветным металлам присущ ряд общих свойств
- Высокая тепловодность и удельная теплоемкость. Для сварочных работ необходим мощный тепловой импульс, но после прекращения воздействия наблюдается быстрое остывание. В ряде случаев свариванию предшествует разогрев детали – это особенно касается алюминия, меди и магния.
- Поглощение атмосферных газов (кроме инертных газов) при термообработке. Особенно ярко выражено у тугоплавких химически активных циркония, титана, тантала, молибдена.
- Медь, алюминий и магний, как и все их сплавы теряют механические свойства при нагревании и разрушаются даже при слабых ударах.
Немного подробнее по алюминий, медь, цинк

Алюминий – отличный электропроводник, пластичен, но его механические свойства невысоки. Первичный алюминий выплавляют из руды и рудных металлов, вторичный – из лома и промышленных отходов. Все алюмосплавы прочны, легки, коррозионно инертны, невосприимчивы ко многим агрессивным средам, сохраняют механические характеристики при сильном нагреве.
Медь – самый распространенный представитель цветных металлов, с отличными показателями пластичности, тепло- и электропроводности. Легко образует высококачественные сплавы, востребованные в современном машиностроении.
Цинк – хрупкий при обычных условиях, но при температуре 100-150 градусов становится ковким и пластичным. Устойчив к коррозии, но не выдерживает взаимодействия с кислотами и щелочами. Плавится при 419 градусах.
Применение
Расход цветных металлов и сплавов сегодня огромен, и тенденция роста потребления не снижается, а наоборот, возрастает. Наибольшей материалоемкостью отмечены следующие области:
- Авиастроение, ракетная, атомная, химическая промышленности. Цветные металлы со сплавами используются как конструкционные элементы машин, зданий и сооружений, несущие силовую нагрузку.
- Медь со сплавами востребованы в химическом машиностроении, производстве труб, емкостей для жидкости, криогенной техники.
- Из алюминия и сплавов строятся самолеты, ракеты, суда; возводятся здания и сооружения; в химической и пищевой промышленности он нужен для создания различных емкостей.
Особенности обработки
Обработка направлена на защиту металлов от коррозии и контакта с кислородом.
Для этого их покрывают специальными лакокрасочными покрытиями. Существует 3 категории средств защиты: краски, грунтовые растворы и универсальные составы. Наиболее эффективна против атмосфеной коррозии грунтовка, к тому же она повышает адгезию к основанию детали. Ее наносят на поверхность перед окрашиванием в один, а лучше несколько слоев.

Важно правильно определить тип грунтовки, так как состав различен для разных металлов.Для деталей из алюминия и его сплавов подойдут грунтовые составы на основе цинка; также пригодны уретановые краски.
Медь, латунь, бронза не нуждаются в окрашивании, поскольку на рынок они поступают с заводской обработкой; защищая поверхность, она выгодно оттеняет природную эстетику этих металлов. Разрушенное заводское покрытие легко удалить с помощью обычного растворителя. Затем нанести на изделие или деталь эпоксидный или полиуретановый лак.
Цветные металлы (Non-ferrous metal) — это
название определенного класса металлов и их сплавов, не содержащих черных металлов — железа и сплавов на его основе, имеющих способность образовывать защитную пленку оксида на воздухе и другие полезные свойства, которых нет у железа
Цветные металлы определение, свойства цветных металлов, классификация цветных металлов, примеры цветных металлов, производство цветных металлов, цветная металлургия, сплавы цветных металлов, запасы цветных металлов в мире, применение цветных металлов, воровство цветных металлов в России, воровство цветных металлов в мире.
Структура публикации
Цветные металлы — это, определение
Цветные металлы — это определенная и большая группа металлов, в технической и промышленной классификации отделяемая от железа и его сплавов, называемых черными металлами, по сути это нежелезные металлы, не содержащие в себе или своих сплавах железо, или в некоторых из них его содержание является второстепенным, это сравнительно дорогостоящие, но широко применяемые человеком металлы в различных сферах, обладающие различными преимуществами перед железом, главным из которых является их долговечность и сохранение свойств, способность образовывать защитную оксидную пленку и не ржаветь.

Разнообразие цветных металлов
Цветные металлы — это медь, алюминий, цинк, олово, свинец, никель, хром, серебро и т.п. Они имеют общее свойство образовывать на поверхности оксидную пленку, которая предотвращает дальнейшее разрушение металла. Цветной металл в промышленности подвергают различным видам механической обработки, а также воздействуют на него давлением. Процессы, производимые над цветным металлом, включают ковку, штамповку, прессование, резание, прокатку,сварку, пайку.

Некоторые изделия из распространенных цветных металлов
Цветные металлы — это распространенное сырье для производства металлопроката, металлических конструкций и изделий из металла. Оно востребовано большинством областей современной промышленности. Область применения цветных металлов очень широка: машиностроение, радиоэлектроника, сфера высоких технологий, бытовые коммуникации. Цветной металл обычно представлен изделиями проката, которые являются своего рода полуфабрикаты для дальнейшего использования.

Прокат из цветного металла
Цветные металлы — это группа металлов, отличающихся от железа некоторыми особенностями: антикоррозийностью, способностью образовывать сплавы кислотоупорные, огнестойкие, антифрикционные и высокого сопротивления (электр. и механ.). К цветным металлам относятся медь, олово, свинец, цинк, алюминий, магний и никель.

Некоторые цветные металлы в таблице Менделеева
Цветные металлы — это техническое название всех металлов и их сплавов (кроме железа и его сплавов, называемых чёрными металлами). Термин «Цветные металлы» в русском языке соответствует термину «нежелезные металлы» во многих др.языках: английский — non-ferrous metals; французский — мétaux non-ferreux, métaux non-ferrugineux; немецкий — Nichteisenmetalle (также farbige Metalle — цветные металлы и Buntmetalle, дословно — пёстрые металлы).

Не все цветные металлы имеют яркие отличающиеся цвета, но некоторые полностью оправдывают это название
Цветные металлы — это простые вещества, отличающиеся блеском и обладающее такими качествами, как способность проводить электрический ток и тепло, ковкость. Сюда относятся все сплавы и металлы, кроме железа. Поэтому во многих европейских странах вместо понятия «цветной металл» используется «нежелезный».

Литые детали из цветных металлов
Цветные металлы — это наиболее дорогой и ценный технический материал. К цветным металлам, наиболее широко применяемым в технике, относятся медь, алюминий, олово, свинец, цинк, магний, титан и их сплавы. В чистом виде цветные металлы используют редко, в основном их применяют в виде сплавов.

Золото — один из наиболее дорогих цветных металлов
Цветные металлы — это металлы, полученные из цветных руд методом высокотемпературной плавки. Такие металлы согласно своим физико-химическим свойствам подразделяют на: легкие металлы — это алюминий, магний, титан и др, — обладают малым удельным весом и плотностью.Тяжелые металлы — это медь, никель, свинец, олово цинк. Наиболее часто применяются и пром. Производстве металлы второй группы. Вся продукция из цветных металлов обладает отличительными свойствами, выгодно отличающими ее от продукции из черных металлов.

Выплавка золотых слитков
Цветные металлы — это металлы или сплавы, не содержащие железа, или сплавы, в которых железо не является главным компонентом (напр. медь, цинк, бронза, латунь).

Изделия из меди — одного из самых распространенных цветных металлов
Цветные металлы — это техническое название категории металлов и их сплавов, за исключением железа и сплавов, в состав которых оно входит. В русскоязычной терминологии понятие цветных металлов эквивалентно нежелезным металлам в европейской классификации. Многие классификации на других языках также цветные металлы обозначают как нежелезные.

Слитки очень востребованнго цветного металла -алюминия
Свойства цветных металлов
Для цветных металлов характерны такие свойства, как коррозионная устойчивость, химическая инертность по отношению к определенным видам сред, высокая теплопроводность и электропроводность, стабильность физических свойств в широком диапазоне температур. Изделия из цветных металлов более долговечны, чем из других материалов. Чистые цветные металлы характеризуются отсутствием примесей и добавок сторонних химических элементов, и представляют собой только один химический элемент например Cu -медь.

Некоторые свойства цветных металлов
Самое главное отличие цветных металлов от чёрных — это то, что они не ржавеют и значительно более долгое время сохраняют свои свойства. Однако это совсем не значит, что на них никак не влияют агрессивные внешние факторы. Так, цинк и оцинкованные поверхности со временем приобретают белесый, меловатый оттенок. Это происходит под влиянием кислорода и влаги. Как и в случае черных металлов, эти факторы окисляют металл на поверхности. Тем не менее, цветные металлы хороши тем, что влага и кислород действуют только на поверхность металла и не могут проникнуть внутрь.

Некоторые свойства распространенного цветного металла алюминия
На сегодняшний день цветные металлы имеют огромное значение для производства любого типа техники. Металл является химически простым веществом, обладающим такими характеристиками, как ковкость, теплопроводность, электропроводность; внешне отличается особым блеском. Некоторые металлы (медь, магний, алюминий) обладают сравнительно высокими теплопроводностью и удельной теплоемкостью, что способствует быстрому охлаждению места сварки, требует применения более мощных источников теплоты при сварке, а в ряде случаев предварительного подогрева детали.

Свойства востребованного цветного металла меди
Для некоторых металлов (медь, алюминий, магний) и их сплавов наблюдается довольно резкое снижение механических свойств при нагреве, в результате чего в этом интервале температур металл легко разрушается от ударов, либо сварочная ванна даже проваливается под действием собственного веса (алюминий, бронза).
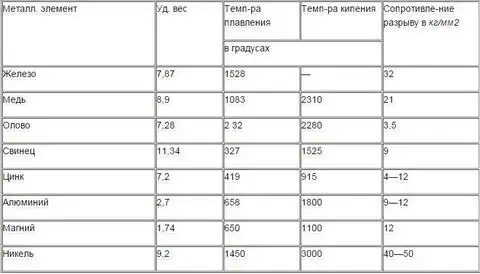
Свойства некоторых цветных металлов по отношению к железу
Все цветные сплавы при нагреве в значительно больших объемах, чем черные металлы, растворяют газы окружающей атмосферы и химически взаимодействуют со всеми газами, кроме инертных. Особенно активные в этом смысле более тугоплавкие и химически более активные металлы: титан, цирконий, ниобий, тантал, молибден. Эту группу металлов часто выделяют в группу тугоплавких, химически активных металлов.
Классификация цветных металлов
Классификация цветных металлов достаточно условна, чаще их по физико-химическим и другим свойствам разделяют на 5 или 7 групп. Наиболее простой и ясной представляется разделение на 7 групп: тяжёлые металлы, лёгкие металлы, благородные металлы, малые металлы, тугоплавкие металлы, рассеянные металлы, радиоактивные металлы. Цветные металлы классифицируют по различным признакам, характерным для той или иной групп.

Условная классификация цветных металлов
Тяжелые цветные металлы
Тяжёлые цветные металлы — это название группы цветных металлов, включающей Cu, Ni, Со,Pb, Sn, Zn, Cd, Bi, Sb, Hg. Мировое производство Cu, Pb, Zn, Ni исчисляется миллионами тонн в год. Сырьём для получения Т. ц. м. служат сульфидные и окисленные полиметаллические руды, в которых обычно содержатся также многие благородные, редкие и др. ценные элементы, добываемые попутно с основными металлами. Многообразием типов руд и номенклатуры металлов обусловлено большое число разнообразных и достаточно сложных методов их получения, обеспечивающих максимально полное извлечение всех ценных составляющих сырья.

Тяжелые цветные металлы
Медь — элемент одиннадцатой группы четвёртого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 29. Обозначается символомCu (лат. Cuprum). Простое вещество медь (CAS-номер: 7440-50-8) — это пластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки). C давних пор широко используется человеком.

Медь в периодической системе Менделеева
Медь — один из первых металлов, которые человек начал применять для технических целей. Вместе с золотом, серебром, железом, оловом, свинцом и ртутью, медь известна людям с древнейших времен и сохраняет свое важное техническое значение до наших дней.Медь — металл розово-красного цвета, относится к группе тяжелых металлов, является отличным проводником тепла и электрического тока. Электропроводность меди в 1,7 раза выше, чем у алюминия, и в 6 раз выше, чем у железа.

Медные бруски-пластины (шины)
Латинское название меди Copper произошло от названия острова Кипр, где уже в III в. до н. э. существовали медные рудники и выплавлялась медь. Около II — III в. выплавка меди производилась в широком масштабе в Египте, в Месопотамии, на Кавказе, в других странах древнего мира. Но, тем не менее, медь — далеко не самый распространенный в природе элемент: содержание меди в земной коре составляет 0,01%, а это лишь 23-е место среди всех встречающихся элементов.

Трубы из меди
Никель
Никель — это один из сравнительно недавно открытых и используемых человеком элементов, относится к тяжелым цветным металлам, в чистом виде на земле не встречается — обычно входит в состав различных руд, обладает хорошими свойствами пластичности и ковкости, высокой твердостью, хорошо полируется, на воздухе покрывается малозаметной пленкой оксида, является ферромагнетиком — притягивается магнитом, в периодической системе Менделеева обозначается символом Ni и имет 28 порядковый номер.

Никель в периодической системе Менделеева
Никель (англ., франц. и нем. Nickel) открыт в 1751 г. Однако задолго до этого саксонские горняки хорошо знали руду, которая внешне походила на медную и применялась в стекловарении для окраски стёкол в зелёный цвет. Все попытки получить из этой руды медь оказались неудачными, в связи с чем в конце XVII в. руда получила название купферникель (Kupfernickel), что приблизительно означает «Медный дьявол». Данную руду (красный никелевый колчедан NiAs) в 1751 г. исследовал шведский минералог Кронштедт. Ему удалось получить зелёный окисел и путём восстановления последнего — новый металл, названный никелем.

Кусок металла никеля
Когда Бергман получил металл в более чистом виде, он установил, что по своим свойствам металл похож на железо; более подробно никель изучали многие химики, начиная с Пруста. Никкел — ругательное слово на языке горняков. Оно образовалось из искажённого Nicolaus — родового слова, имевшего несколько значений. Но главным образом слово Nicolaus служило для характеристики двуличных людей; кроме того, оно обозначало «озорной маленький дух», «обманчивый бездельник» и т. д. В русской литературе начала XIX в. употреблялись названия николан (Шерер, 1808), николан (Захаров, 1810), николь и никель (Двигубский, 1824).

Гранулированный никель
Цинк — элемент побочной подгруппы второй группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 30. Обозначается символом Zn (лат. Zincum). Простое вещество цинк (CAS-номер: 7440-66-6) при нормальных условиях — хрупкий переходный металл голубовато-белого цвета(тускнеет на воздухе, покрываясь тонким слоем оксида цинка).

Цинк в периодической системе Менделеева
Сплав цинка с медью — латунь — был известен ещё в Древней Греции, Древнем Египте, Индии (VII в.), Китае (XI в.). Долгое время не удавалось выделить чистый цинк. В 1738 году в АнглииУильямом Чемпионом был запатентован дистилляционный способ получения цинка. В промышленном масштабе выплавка цинка началась также в XVIII в.: в 1743 году в Бристоле вступил в строй первый цинковый завод, основанный Уильямом Чемпионом, где получение цинка проводилось дистилляционным способом.

Небольшой слиток цинка
В 1746 А. С. Маргграф в Германии разработал похожий на способ Чемпиона дистилляционный способ получения чистого цинка путём прокаливания смеси его окиси с углём без доступа воздуха в глиняных огнеупорных ретортах с последующейконденсацией паров цинка в холодильниках. Маргграф описал свой метод во всех деталях и этим заложил основы теории производства цинка.

Куски цинка
Поэтому его часто называют первооткрывателем цинка. В 1805 году Чарльз Гобсон и Чарльз Сильвестр из Шеффилда запатентовали способ обработки цинка — прокатка при 100-150 градусах. Первый в России цинк был получен на заводе «Алагир» 1 января 1905 года. Первые заводы, где цинк получали электролитическим способом появились в 1915 году в Канаде и США.

Слитки из цветного металла — цинка
Свинец
Свинец (лат. Plumbum; обозначается символом Pb) — элемент 14-й группы (по устаревшей классификации — главной подгруппы IV группы), шестого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 82 и, таким образом, содержит магическое число протонов. Простое вещество свинец (CAS-номер:7439-92-1) — ковкий, сравнительно легкоплавкий металл серебристо-белого цвета с синеватым отливом. Известен с глубокой древности.

Свинец — свойства, место в таблице Менделеева
Свинец используется многие тысячелетия, поскольку он широко распространён, легко добывается и обрабатывается. Он очень ковкий и легко плавится. Выплавка свинца была первым из известных человеку металлургических процессов. Бусины из свинца, датируемые 6400 г. до н.э., были найдены в культуре Чатал-Хююк.

Кусок свинца
Самым древним предметом, сделанным из свинца, часто считается статуэтка стоящей женщины в длинной юбке времён первой династии Египта, датируемая 3100-2900 гг. до н.э., хранящаяся в Британском музее (инвентарный номер EA 32138). Она была найдена в храме Осириса в Абидосе и привезена из Египта в 1899 году. В Древнем Египте использовались медальоны из свинца. В раннем бронзовом веке свинец использовался наряду с сурьмой и мышьяком. Указание на свинец как на определённый металл имеется в Ветхом Завете.

Слитки цветного металла — свинца
Олово
Олово (лат. Tin; обозначается символом Sn) — элемент 14-й группы периодической таблицы химических элементов (по устаревшей классификации — элемент главной подгруппы IV группы), пятого периода, с атомным номером 50. Относится к группе лёгких металлов. При нормальных условиях простое вещество олово — пластичный, ковкий и легкоплавкий блестящий металл серебристо-белого цвета. Олово образует две аллотропические модификации: ниже 13,2 °C устойчивое α-олово (серое олово) с кубической решёткой типа алмаза, выше 13,2 °C устойчиво β-олово (белое олово) с тетрагональной кристаллической решеткой.

Олово в периодической системе Менделеева
Олово было известно человеку уже в IV тысячелетии до н. э. Этот металл был малодоступен и дорог, поэтому изделия из него редко встречаются среди римских и греческих древностей. Об олове есть упоминания в Библии, Четвёртой Книге Моисеевой. Олово является (наряду с медью) одним из компонентов оловянистой бронзы, изобретённой в конце или середине III тысячелетия до н. э.. Поскольку бронза являлась наиболее прочным из известных в то время металлов и сплавов, олово было «стратегическим металлом» в течение всего «бронзового века», более 2000 лет (очень приблизительно: 35-11 века до н. э.).

Самодельные слитки олова
Легкие цветные металлы
Легкие цветные металлы — Металлы этой группы имеют самую низкую среди всех металлов плотность (удельную массу).

Легкие и тяжелые цветные металлы сравнение
Алюминий
Алюминий — элемент 13-й группы периодической таблицы химических элементов (по устаревшей классификации — элемент главной подгруппы III группы), третьего периода, с атомным номером 13. Обозначается символом Al (лат. Aluminium). Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости химический элемент в земной коре (после кислорода и кремния).

Алюминий в таблице Менделеева
Простое вещество алюминий (CAS-номер: 7429-90-5) — лёгкий парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия.

Кусок алюминия
Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы калия на хлорид алюминия с последующей отгонкой ртути. Название элемента образовано от лат. alumen — квасцы. До открытия промышленного способа получения алюминия этот металл был дороже золота. В 1889 г. британцы, желая почтить богатым подарком великого русского химика Д.И Дмитрия Ивановича Менделеева, подарили ему весы из золота и алюминия.

Самодельные алюминиевые слитки
Магний
Магний — элемент главной подгруппы второй группы, третьего периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 12. Обозначается символом Mg (лат. Magnesium). Простое вещество магний (CAS-номер: 7439-95-4) — лёгкий, ковкий металл серебристо-белого цвета.

Магний в периодической системе Менделеева
Магний это один из самых легких металлов, устойчивых на воздухе. Благодаря этому, а так же тому, что он широко распространен в природе и относительно дешев, магний достаточно часто используется как конструкционный материал в авиастроении и в других отраслях, где прежде всего важен низкий вес конструкционных материалов.

Кусочки магния
Магний — активный металл: если нагреть небольшой кусок магния до температуры плавления, он загорится и сгорит ослепительным пламенем. Хотя в сухом воздухе, при комнатной температуре, он окисляется достаточно медленно. Повысить коррозионную устойчивость магния можно введением в магниевые сплавы различных добавок.

Слитки цветного металла — магния
Титан
Тита́н (лат. Titanium; обозначается символом Ti) — элемент побочной подгруппы четвёртой группы, четвёртого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 22. Простое вещество титан — лёгкий прочный металл серебристо-белого цвета. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура полиморфного превращения α↔β 883 °C. Температура плавления 1660±20 °C. Tитан имеет твердость по Бринеллю 175 МПа.

Титан в периодической системе Менделеева
Открытие TiO2 сделали практически одновременно и независимо друг от друга англичанин У. Грегор и немецкий химик М. Г. Клапрот. У. Грегор, исследуя состав магнитного железистого песка (Крид, Корнуолл, Англия, 1791), выделил новую «землю» (оксид) неизвестного металла, которую назвал менакеновой. В 1795 г. немецкий химик Клапрот открыл в минерале рутиле новый элемент и назвал его титаном. Спустя два года Клапрот установил, что рутил и менакеновая земля — оксиды одного и того же элемента, за которым и осталось название «титан», предложенное Клапротом.

Кусочки титана
Через 10 лет открытие титана состоялось в третий раз. Французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные оксиды титана. Первый образец металлического титана получил в 1825 году Й. Я. Берцелиус. Из-за высокой химической активности титана и сложности его очистки чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 году термическим разложением паров иодида титана TiI4.

Таблетки — маленькие слитки титана
Бериллий
Бериллий — элемент второй группы (по устаревшей классификации — главной подгруппы второй группы), второго периода периодической системы химических элементов сатомным номером 4. Обозначается символом Be (лат. Beryllium). Высокотоксичный элемент. Простое вещество бериллий (CAS-номер: 7440-41-7) -относительно твёрдый металл светло-серого цвета, имеет весьма высокую стоимость.

Бериллий в таблице Менделеева
Открыт в 1798 году французским химиком Луи Никола Вокленом, который назвал его глюцинием. Современное название элемент получил по предложению химиков немца Клапрота и шведа Экеберга. Большую работу по установлению состава соединений бериллия и его минералов провёл российский химик И. В. Авдеев (1818-1865).

Кусок металлического бериллия
Именно он доказал, что оксид бериллия имеет состав BeO, а не Be2O3, как считалось ранее. В свободном виде бериллий был выделен в 1828 году французским химиком Бюсси и независимо от него немецким химиком Вёлером. Чистый металлический бериллий был получен в 1898 году французским физиком Лебо с помощью электролиза расплавленных солей.

Слиток цветного металла — бериллия
Кальций
Кальций — элемент главной подгруппы второй группы, четвёртого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 20. Обозначается символом Ca (лат. Calcium). Простое вещество кальций (CAS-номер: 7440-70-2) — мягкий, химически активный щёлочноземельный металл серебристо-белого цвета.

Кальций в периодической системе Менделеева
Название элемента происходит от лат. calx (в родительном падеже calcis) — «известь», «мягкий камень». Оно было предложено английским химиком Хэмфри Дэви, в 1808 г. выделившим металлический кальций электролитическим методом. Дэви подверг электролизу смесь влажной гашёной извести с оксидом ртути HgO на платиновой пластине, которая являлась анодом.Катодом служила платиновая проволока, погруженная в жидкую ртуть. В результате электролиза получалась амальгама кальция. Отогнав из неё ртуть Дэви получил металл, названный кальцием.

Брусочек кальция в азотной среде, чтобы не окисляться
Соединения кальция — известняк, мрамор, гипс (а также известь — продукт обжига известняка) применялись в строительном деле уже несколько тысячелетий назад. Вплоть до конца XVIII века химики считали известь простым телом. В 1789 году А. Лавуазье предположил, что известь, магнезия, барит, глинозём и кремнезём — вещества сложные.

Гранулы кальция в запаянной банке для получения водорода в полевых условиях (предмет армии США)
Стронций
Стронций — элемент главной подгруппы второй группы, пятого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 38. Обозначается символом Sr (лат. Strontium). Простое вещество стронций (CAS-номер: 7440-24-6) — мягкий, ковкий и пластичный щёлочноземельный металл серебристо-белого цвета. Обладает высокой химической активностью, на воздухе быстро реагирует с влагой и кислородом, покрываясь жёлтой оксидной плёнкой.

Стронций в таблице Менделеева
Новый элемент обнаружили в минерале стронцианите, найденном в 1764 году в свинцовом руднике близ шотландской деревни Стронти́ан (англ. Strontian, гэльск. Sron an t-Sìthein), давшей впоследствии название новому элементу. Присутствие в этом минерале оксида нового металла было установлено в 1787 году Уильямом Крюйкшенком и Адером Кроуфордом. Выделен в чистом виде сэром Хемфри Дэви в 1808 году.

Цветной металл стронций, запаянный в ампулу
Барий
Барий — элемент главной подгруппы второй группы, шестого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 56. Обозначается символом Ba (лат. Barium). Простое вещество барий (CAS-номер: 7440-39-3) — мягкий, ковкий щёлочноземельный металл серебристо-белого цвета. Обладает высокой химической активностью.

Барий в периодической системе Менделеева
Барий был открыт в виде оксида BaO в 1774 г. Карлом Шееле и Юханом Ганом. В 1808 году английский химик Гемфри Дэви электролизом влажного гидроксида бария с ртутным катодом получил амальгаму бария; после испарения ртути при нагревании он выделил металлический барий. Своё название получил от др.-греч. βαρύς — «тяжёлый», от названия минерала барит — тяжёлый шпат.

Кусок цветного металла бария окисленный на воздухе
Литий
Литий (лат. Lithium; обозначается символом Li) — элемент первой группы (по устаревшей классификации — главной подгруппы первой группы), второго периода периодической системы химических элементов с атомным номером 3. Простое вещество литий — мягкий щелочной металл серебристо-белого цвета.

Литий в таблице Менделеева
Литий был открыт в 1817 году шведским химиком и минералогом Иоганном Арфведсоном сначала в минерале петалите (Li,Na)(Si4AlO10), а затем в сподумене LiAl(Si2O6) и в лепидолитеKLi1.5Al1.5(Si3AlO10)(F,OH)2. Металлический литий впервые получил Гемфри Дэви в 1818 году. Своё название литий получил из-за того, что был обнаружен в «камнях» (греч. λίθος — камень). Первоначально назывался «литион», современное название было предложено Берцелиусом.

Неокисленный кусочек цветного металла лития в аргоновой атмосфере
Натрий
Натрий — элемент первой группы (по старой классификации — главной подгруппы первой группы), третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 11. Обозначается символом Na (лат. Natrium). Простое вещество натрий (CAS-номер: 7440-23-5) — мягкий щелочной металл серебристо-белого цвета.

Натрий в периодической системе Менделеева
Натрий (а точнее, его соединения) известен и использовался с давних времён. Еврейское слово neter (греч. νίτρον, лат. nitrum) встречается уже в Библии как название вещества, которое, по Соломону, вскипает с уксусом. Сода (натрон), встречается в природе в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Плиний Старший пишет, что в дельте Нила соду (в ней была достаточная доля примесей) выделяли из речной воды. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или даже чёрный цвет.

Ампулы с цветным металлом натрием заводского изготовления
Калий
Калий — элемент главной подгруппы первой группы, четвёртого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий (CAS-номер: 7440-09-7) — мягкий щелочной металл серебристо-белого цвета. В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь.

Калий в периодической системе Менделеева
Во многих свойствах калий очень близок натрию, но с точки зрения биологической функции и использования клетками живых организмов они антагонистичны. Соединения калия используются с древнейших времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K2SO4, соду и хлорид калия KCl.

Калий в ампуле
19 ноября 1807 года в Бэкеровской лекции английский химик Дэви сообщил о выделении калия электролизом расплава едкого кали (KOH)[3](в рукописи лекции Дэви указал, что он открыл калий 6 октября 1807 года) и назвал его «потасий» (лат. potasium:32; это название (правда, в некоторых языках с двумя буквами s) до сих пор употребительно в английском, французском, испанском, португальском и польском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль-кали — поташ). Это название вошло в немецкий язык, оттуда в большинство языков Северной и Восточной Европы (в том числе русский) и «победило» при выборе символа для этого элемента — K.

Кусок цветного металла калия после консервации, виден свежий срез, который быстро окислится на воздухе
Рубидий
Рубидий — элемент главной подгруппы первой группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 37. Обозначается символом Rb (лат. Rubidium). Простое вещество рубидий (CAS-номер: 7440-17-7) — мягкий легкоплавкий щелочной металл серебристо-белого цвета. Не смотря на то, что рубидий обычно рассматривают вместе с цезием (эдакая сладкая парочка), свойствами он довольно сильно напоминает так же и калий. Цветом и поведением на воздухе тоже.
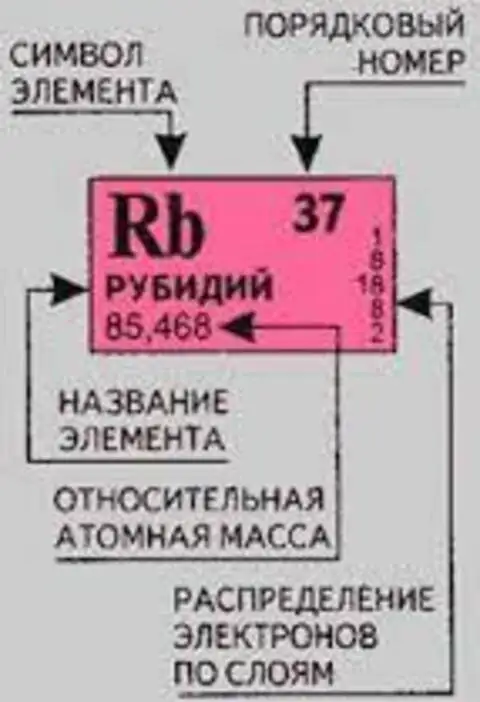
Рубидий в периодической системе Менделеева
В 1861 году немецкие учёные Роберт Вильгельм Бунзен и Густав Роберт Кирхгоф, изучая с помощью спектрального анализа природные алюмосиликаты, обнаружили в них новый элемент, впоследствии названный рубидием по цвету наиболее сильных линий спектра.

Цветной металл рубидий в запаянной ампуле
Цезий
Цезий (лат. Caesium, обозначается символом Cs) — элемент главной подгруппы первой группы шестого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, атомный номер — 55. Простое вещество цезий (CAS-номер: 7440-46-2) — мягкий щелочной металл серебристо-жёлтого цвета. Своё название цезий получил за наличие двух ярких синих линий в эмиссионном спектре (от лат. caesius — небесно-голубой).

Цезий в периодической системе Менделеева
Цезий это один из трех интенсивно окрашенных металлов (другие два — Cu и Au). По окраске, чистый цезий больше всего напоминает золото (но очень чистый металл немного светлее). А вот по реакционной способности это полная его противоположность. Активность цезия настолько высока, что он самовоспламеняется на воздухе и взрывается при контакте с водой. Температура плавления цезия близка к комнатной, и не очень чистый металл при нормальных условиях находится в полужидком состоянии.

Цветной металл цезий в запаянной ампуле и дополнительнь в блоке из полиэфирной смолы
Цезий был открыт в 1860 году немецкими учёными Р. В. Бунзеном и Г. Р. Кирхгофом в водах Бад-Дюркхаймского минерального источника в Германии методом оптической спектроскопии, тем самым, став первым элементом, открытым при помощи спектрального анализа. В чистом виде цезий впервые был выделен в 1882 году шведским химиком К. Сеттербергом при электролизе расплава смеси цианида цезия (CsCN) и бария.

Довольно чистый цезий в ампуле, предположительно для промышленного применения
Благородные цветные металлы
Благородные цветные металлы — эта группа металлов обладает высокой стойкостью к воздействию окружающей среды и агрессивных сред.

Описание благородных металлов
Золото
Золото — элемент 11 группы (по устаревшей классификации — побочной подгруппы первой группы), шестого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 79. Обозначается символом Au (лат. Aurum). Простое вещество золото — благородный металл жёлтого цвета. Регистрационный номер CAS: 7440-57-5. Золото — это редко встречающийся элемент. Его среднее содержание всего 0,3 г на тонну веса Земли, включая металлическое ядро, концентрация золота в котором, по крайней мере, в пять раз больше средней.

Золото в периодической системе Менделеева
Золото — венец драгоценных металлов. По мнению многих ученых, золото было первым металлом, который человечество начало использовать для изготовления украшений, предметов домашнего обихода и религиозного культа. Золотые изделия были найдены в культурных слоях эпохи неолита (V-IV тысячелетия до н.э.). Оно всегда было и остается символом красоты, богатства и власти. Золото — это «металл царей» и «царь металлов».

Мерный слиток благородного цветного металла золота (Швейцарский банк Banca della Swizzera Italiana)
Серебро
Серебро — элемент 11 группы (по устаревшей классификации — побочной подгруппы первой группы), пятого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 47. Обозначается символом Ag (лат. Argentum). Простое вещество серебро (CAS-номер: 7440-22-4) — ковкий, пластичный благородный металл серебристо-белого цвета. Кристаллическая решётка — гранецентрированная кубическая. Температура плавления — 962 °C, плотность — 10,5 г/см³.

Серебро в таблице Менделеева
Серебро известно человечеству с древнейших времён. Это связано с тем, что в своё время серебро, равно как и золото, часто встречалось в самородном виде — его не приходилось выплавлять из руд. Это предопределило довольно значительную роль серебра в культурных традициях различных народов. Одним из древнейших центров добычи и обработки серебра была доисторическая Сардиния, где оно было известно с раннего энеолита.

Серебряный слиток американского банка
В Ассирии и Вавилоне серебро считалось священным металлом и являлось символом Луны. В Средние века серебро и его соединения были очень популярны среди алхимиков. С середины XIII века серебро становится традиционным материалом для изготовления посуды. Кроме того, серебро и по сей день используется для чеканки монет.

Самодельные слитки цветного благородного металла — серебра
Платина
Платина (исп. Platina) — химический элемент 10-й группы (по устаревшей классификации — побочной подгруппы восьмой группы), 6-го периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 78; блестящий благородный металл серебристо-белого цвета.

Платина в таблице Менделеева
После открытия (а точнее обнаружения в природе) платина не сразу была оценена по достоинству. Сначала она считалась бесполезной примесью, встречающейся в золотых россыпях. Затем фальшивомонетчики начали добавлять её к золоту (поскольку удельный вес сплава при этом почти не менялся), а в Сибири, в 18 веке, зерна самородной платины использовались для стрельбы вместо дроби.

Слиток благородного цветного металла — платины швейцарского банка
Отношение к платине изменилось только после того, как была разработана технология переработки этого тугоплавкого металла и из неё научились делать разнообразную химическую посуду и детали оборудования, устойчивые в агрессивных средах. В настоящее время, область применений платины значительно расширилась и основное количество этого металла (и его соединений) идет на производство разнообразных катализаторов.

Платиновые электроды заводского изготовления
Осмий
Осмий (лат. Osmium) — химический элемент с атомным номером 76 в Периодической системе химических элементов Д. И. Менделеева, обозначается символом Os. Пристандартных условиях представляет собой блестящий серебристо-белый с голубоватым отливом металл. Переходный металл, относится к платиновым металлам. Наряду сиридием обладает наибольшей плотностью среди всех простых веществ. Согласно теоретическим расчётам его плотность даже выше, чем у иридия.

Осмий в таблице Менделеева
Осмий открыт в 1803 году английским химиком Смитсоном Теннантом в сотрудничестве с Уильямом Х. Уолластоном в осадке, остающемся после растворения платины в царской водке. Сходные исследования проводились французскими химиками Колле-Дескоти, Антуаном Франсуа де Фуркруа и Вокленом, которые тоже пришли к выводу о содержании неизвестного элемента в нерастворимом остатке платиновой руды.

Небольшой слиток цветного благородного металла осмия
Гипотетическому элементу было присвоено имя птен (греч. πτηνος — крылатый), однако опыты Теннанта продемонстрировали, что это смесь двух элементов — иридия и осмия. Открытие новых элементов было задокументировано в письме Теннанта Лондонскому королевскому обществу от 21 июня 1804 года.

Кристаллы цветного металла осмия
Рутений
Рутений — элемент побочной подгруппы восьмой группы пятого периода периодической системы химических элементов, атомный номер — 44. Простое вещество рутений — переходный металл серебристого цвета. Относится к платиновым металлам.

Рутений в периодической таблице Менделеева
Открыт профессором Казанского университета Карлом Клаусом в 1844 году, в том же году опубликовавшим о новом элементе большую статью «Химические исследования остатков Уральской платиновой руды и металла рутения» в «Учёных записках Казанского университета». б открытии, методе получения и свойствах нового элемента Клаус сообщил в письме Г. И. Гессу на немецком языке, который зачитал его на заседании Петербургской Академии наук 13 сентября 1844 года, этот текст был опубликован в бюллетене Академии и в переводе на русский язык — в «Горном журнале».

Компактный слиток рутения — благородного цветного металла
ОКлаус выделил рутений из уральской платиновой руды в чистом виде и указал на сходство между триадами рутений — родий — палладий и осмий — иридий — платина. Первооткрыватель элемента К. К. Клаус назвал рутений в честь России (Ruthenia — латинское название Руси/России). Название «рутений» было предложено в 1828 году Г. В. Озанном для элемента, который он по ошибке принял за новый элемент, и Клаус, действительно открывший новый элемент в 1844 году, дал ему это название.

Кристаллы цветного металла рутения
Родий
Родий (лат. Rhodium; обозначается символом Rh) — элемент побочной подгруппы восьмой группы пятого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, атомный номер — 45. Простое вещество родий (CAS-номер: 7440-16-6) — твёрдый переходный металл серебристо-белого цвета. Благородный металл платиновой группы.

Родий в таблице Менделеева
Открыт в Англии в 1803 году Уильямом Гайдом Волластоном в ходе работ с самородной платиной. Внешне родий выглядит достаточно красиво. Он имеет очень светлую окраску и напоминает по виду серебро, но, в отличие от серебра, родий не темнеет на воздухе и поэтому родирование применяется для защиты серебряных изделий от потемнения. Родий достаточно пластичен, и из него можно изготовить фольгу методом прокатки (хотя для этого потребуется несколько промежуточных отжигов для рекристаллизации).

Небольшой слиток благородного цветного металла — родияю
Сегодня родий – самый дорогой нерадиоактивный металл (естественно, не учитывая индивидуальные изотопы элементов, цена на которые в основном определяется стоимостью их выделения из природной смеси). Пожалуй, на примере родия (ну, может еще палладия) лучше всего наблюдать колебания рыночной цены металлов. Родий используется для производства гетерогенных и металлоорганических катализаторов, жидкокристаллических дисплеев, зеркал, тиглей и т.п.

Кристаллы цветного металла — родия
Палладий
Палладий — элемент побочной подгруппы восьмой группы пятого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, атомный номер — 46. Обозначается символом Pd (лат. Palladium). Простое вещество палладий (CAS-номер: 7440-05-3) — пластичный переходный металл серебристо-белого цвета. Благородный металл платиновой группы.

Палладий в периодической системе Менделеева
Открыт английским химиком Вильямом Волластоном (William Hyde Wollaston) в 1803 году. Волластон выделил его из платиновой руды, привезённой из Южной Америки. Для выделения элемента Волластон растворил руду в царской водке (aqua regia), нейтрализовал кислоту раствором NaOH, затем осадил платину из раствора действием хлорида аммония NH4Cl (в осадок выпадаетхлорплатинат аммония). Потом к раствору был добавлен цианид ртути, при этом образовался цианид палладия. Чистый палладий был выделен из цианида нагреванием.

Благородный цветной металл палладий в гранулах (одна унция)
Малые тяжелые цветные металлы
Малые тяжелые цветные металлы — они являются природными спутниками основных тяжелых металлов. Обычно их получают попутно, но производят в значительно меньших количествах.

Малые тяжелые цветные металлы
Кобальт
Кобальт — элемент девятой (по старой классификации — побочной подгруппы восьмой группы) четвёртого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, атомный номер — 27. Обозначается символом Co (лат. Cobaltum). Простое вещество кобальт (CAS-номер: 7440-48-4) — серебристо-белый, слегка желтоватый металл с розоватым или синеватым отливом. Существует в двух кристаллических модификациях: α-Co с гексагональной плотноупакованной решёткой, β-Co с кубической гранецентрированной решёткой, температура перехода α↔β 427 °C.

Кобальт в таблице Менделеева
Соединения кобальта известны человеку с глубокой древности, синие кобальтовые стёкла, эмали, краски находят в гробницах Древнего Египта. Так, в гробнице Тутанхамона нашли много осколков синего кобальтового стекла, неизвестно, было ли приготовление стёкол и красок сознательным или случайным. Первое приготовление синих красок относится к 1800 году.

Куски кобальта — цветного металла
Кобальт упоминается у Бирингуччо, Василия Валентина, Парацельса и других авторов XV — XVII вв. В «Алхимическом лексиконе» Руланда (1612) о кобальте говорится: «Кобол кобальт (Koboltum, Kobaltum) или коллет (Colletum) — металлическая материя, чернее свинца и железа, растягивающаяся при нагревании. Кобальт — черная, немного похожая по цвету на золу материя, которую можно ковать и лить, но она не обладает металлическим блеском, и которая представляет собой вредную взвесь, уводящую (при плавке) вместе с дымом хорошую руду».

Гранула цветного металла кобальта
Очевидно, здесь говорится о металлическом кобальте. Тем не менее в истории химии принято считать, что металлический кобальт был впервые описан в 1735 г. упсальским профессором Брандтом. В диссертации «О полуметаллах» Брандт указывает, в частности,что получаемый из руд металлический висмут не представляет собой чистого металла, а содержит «кобальтовый королек» (металлический кобальт). Он же выяснил,что соли кобальта окрашивают стекла в синий цвет. В чистом виде металлический кобальт был получен Верцелиусом.

Кобальт в цилиндриках
Кадмий
Кадмий — элемент двенадцатой группы (в устаревшей классификации — побочной подгруппы второй группы), пятого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 48. Обозначается символом Cd (лат. Cadmium). Простое вещество кадмий (CAS-номер: 7440-43-9) при нормальных условиях — мягкий ковкий тягучий переходный металл серебристо-белого цвета. Устойчив в сухом воздухе, во влажном на его поверхности образуется плёнка оксида, препятствующая дальнейшему окислению металла.

Кадмий в таблице Менделеева
Открыт немецким профессором Ф. Штромейером в 1817. Провизоры Магдебурга при изучении оксида цинка ZnO заподозрили в нём примесь мышьяка. Штромейер выделил из ZnO коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий.

Слиток цветного металла — кадмия
Сурьма
Сурьма (лат. Stibium; обозначается символом Sb) химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) пятого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича; имеет атомный номер 51. Простое вещество сурьма (CAS-номер: 7440-36-0) — полуметалл серебристо-белого цвета с синеватым оттенком, грубозернистого строения. Известны четыре металлических аллотропных модификаций сурьмы, существующих при различных давлениях, и три аморфные модификации (взрывчатая, чёрная и жёлтая сурьма).

Сурьма в таблице Менделеева
Сурьма известна с глубокой древности. В странах Востока она употреблялась примерно за 3000 лет до н. э. для изготовления сосудов. В Древнем Египте уже в 19 в. до н. э. порошок сурьмяного блеска (природный Sb2S3) под названием mesten или stem применялся для чернения бровей. В Древней Греции он был известен как στίμμι и στίβι, отсюда лат. stibium. Около 12-14 вв. н. э. появилось название antimonium. Подробное описание свойств и способов получения сурьмы и её соединений впервые дано алхимиком Василием Валентином (Германия) в 1604.

Слиток цветного металла сурьмы в виде прутка (чистота 99.99%)
В 1789 А. Лавуазье включил сурьму в список химических элементов под названием antimoine (современный английский antimony, испанский и итальянский antimonio, немецкий Antimon). Русское слово «сурьма» произошло от турецкого и крымско-татарского sürmä; им обозначался порошок свинцового блеска PbS, также служивший для чернения бровей (по другим данным, «сурьма» — от персидского «сурме» — металл).

Кусок достаточной чистоты цветного металла — сурьмы
Висмут
Висмут — химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) шестого периода периодической системы химических элементов Д. И. Менделеева; имеет атомный номер 83. Обозначается символом Bi (лат. Bismuthum). Простое вещество представляет собой при нормальных условиях блестящий серебристый с розоватым оттенком металл.

Висмут в периодической системе Менделеева
Предположительно латинское Bismuthum или bisemutum происходит от немецкого weisse Masse, «белая масса». В Средневековье висмут часто использовался алхимиками во время опытов. Добывающие руду шахтёры называли его tectum argenti, что означает «производство серебра», при этом они считали, что висмут был наполовину серебром. Висмут использовали не только в Европе. Инки применяли висмут в процессе изготовления холодного оружия, из-за него мечи отличались особой красотой, а их блеск был вызван радужным окислением, которое являлось следствием образования на поверхности металла тонкой плёнки оксида висмута.

Гранулированный висмут для лабораторного применения

Палочка из цветного металла висмута (чистота 99.9% )
Ртуть
Ртуть (Hg, от лат. Hydrargyrum) — элемент шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 80, относящийся кподгруппе цинка (побочной подгруппе II группы). Простое вещество ртуть — переходный металл, при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй такой элемент — бром).

Ртуть в таблице Менделеева и ее описание
Ртуть известна с древних времен. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом природной киновари. Древние греки и римляне использовали ртуть для очистки золота (амальгамирование), знали о токсичности самой ртути и её соединений, в частности сулемы. Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твердость при помощи серы или мышьяка, то получится золото.

Ртуть в запаянной колбе
Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 г. Для представления элемента как у алхимиков, так и в нынешнее время используется символ планеты Меркурий. Но принадлежность ртути к металлам была доказана только трудами Ломоносова и Брауна, которые в декабре 1759 года смогли заморозить ртуть и установить её металлические свойства: ковкость, электропроводность и др.

Гайка плавает на поверхности цветного металла ртути
Мышьяк
Мышьяк (лат. Arsenicum; обозначается символом As) — химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) четвёртого периода периодической системы; имеет атомный номер 33. Простое вещество представляет собой хрупкий полуметалл стального цвета с зеленоватым оттенком (в серой аллотропной модификации). CAS-номер: 7440-38-2.

Мышьяк в таблице Менделеева
Мышьяк является одним из древнейших элементов, используемых человеком. Сульфиды мышьяка As2S3 и As4S4, так называемые аурипигмент («арсеник») и реальгар, были знакомы римлянам и грекам. Эти вещества ядовиты. Мышьяк является одним из элементов, встречающихся в природе в свободном виде. Его можно сравнительно легко выделить из соединений. Поэтому история не знает, кто впервые получил в свободном состоянии элементарный мышьяк.

Кусочки цветного металла мышьяка в ампуле с азотной средой
Многие приписывают роль первооткрывателя алхимику Альберту Великому. В трудах Парацельса также описано получение мышьяка в результате реакции арсеника с яичной скорлупой. Многие историки науки предполагают, что металлический мышьяк был получен значительно раньше, но он считался представителем самородной ртути. Это можно объяснить тем, что сульфид мышьяка был очень похож на ртутный минерал. И выделение из него было очень легким, как и при выделении ртути.

Образец самородного природного мышьяка
Элементарный мышьяк был известен в Европе и в Азии ещё со средних веков. Китайцы получали его из руд. Мышьяк — ядовитое вещество. Европейцы не могли диагностировать наступление смерти из-за отравления мышьяком, а вот китайцы могли это делать. Но этот метод анализа до настоящих времен не дошел, так и остался загадкой. Европейцы научились определять наступление смерти при отравлении мышьяком, это впервые сделал Д.Марше. Данная реакция используется и в настоящее время.

Расплавленный мышьяк в запаянной кварцевой ампуле
Тугоплавкие цветные металлы
Тугоплавкие металлы — класс химических элементов (металлов), имеющих очень высокую температуру плавления и стойкость к изнашиванию. Выражение тугоплавкие металлычаще всего используется в таких дисциплинах как материаловедение, металлургия и в технических науках. Определение тугоплавких металлов относится к каждому элементу группыпо разному. Основными представителями данного класса элементов являются элементы пятого периода — ниобий и молибден; шестого периода — тантал, вольфрам и рений. Все они имеют температуру плавления выше 2000 °C, химически относительно инертны и обладают повышенным показателем плотности. Благодаря порошковой металлургии из них можно получать детали для разных областей промышленности.
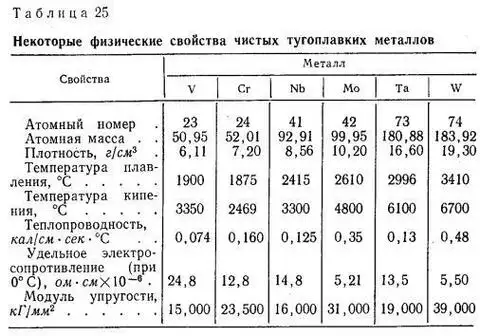
Тугоплавкие металлы — некоторые свойства
Вольфрам
Вольфрам — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева, обозначается символом W (лат. Wolframium). При нормальных условиях представляет собой твёрдый блестящий серебристо-серый переходный металл. Вольфрам — самый тугоплавкий из металлов. Более высокую температуру плавления имеет только неметаллический элемент — углерод. При стандартных условиях химически стоек.

Вольфрам в таблице Менделеева
Название Wolframium перешло на элемент с минерала вольфрамит, известного ещё в XVI в. под названием лат. Spuma lupi («волчья пена») или нем. Wolf Rahm («волчьи сливки», «волчий крем»). Название было связано с тем, что вольфрам, сопровождая оловянные руды, мешал выплавке олова, переводя его в пену шлаков («пожирает олово как волк овцу»). В настоящее время в США, Великобритании и Франции для вольфрама используют название «tungsten» (швед. tung sten — «тяжелый камень»).

Цветной металл вольфрам в запаянной ампуле
В 1781 году знаменитый шведский химик Шееле, обрабатывая азотной кислотой минерал шеелит, получил жёлтый «тяжёлый камень» (триоксид вольфрама). В 1783 годуиспанские химики братья Элюар сообщили о получении из саксонского минерала вольфрамита как растворимой в аммиаке жёлтой окиси нового металла, так и самого металла. При этом один из братьев, Фаусто, был в Швеции в 1781 году и общался с Шееле. Шееле не претендовал на открытие вольфрама, а братья Элюар не настаивали на своём приоритете.

Вольфрамовое кольцо (получено кристаллизацией вольфрама из газовой фазы)
Молибден
Молибден — элемент шестой группы (по старой классификации — побочной подгруппы шестой группы) пятого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, атомный номер 42. Обозначается символом Mo (лат. Molybdaenum). Простое вещество молибден (CAS-номер: 7439-98-7) — переходный металл светло-серого цвета. Главное применение находит в металлургии.

Молибден в периодической системе Менделеева
Открыт в 1778 году шведским химиком Карлом Шееле, который, прокаливая молибденовую кислоту, получил МоО3. В металлическом состоянии впервые получен П. Гьельмом в 1781 г. восстановлением оксида углём: он получил молибден, загрязненный углеродом и карбидом молибдена. Чистый молибден в 1817 году получил Й. Берцелиус восстановлением оксида водородом.

Брусок из спресованного и спеченного порошка молибдена
Название происходит от др.-греч. μόλυβδος, означающего «свинец». Оно дано из-за внешнего сходства молибденита (MoS2), минерала, из которого впервые удалось выделить оксид молибдена, со свинцовым блеском (PbS). Вплоть до XVIII в. молибденит не отличали от графита и свинцового блеска, эти минералы носили общее название «молибден».

Лист из цветного металла молибдена
Ванадий
Ванадий — элемент побочной подгруппы пятой группы, четвёртого периода периодической системы химических элементов Д. И. Дмитрия Ивановича Менделеева, с атомным номером 23. Обозначается символом V (лат. Vanadium). Простое вещество ванадий (CAS-номер: 7440-62-2) — пластичный металл серебристо-серого цвета.

Ванадий в таблице Менделеева
Ванадий был открыт в 1801 г. профессором минералогии из Мехико Андресом Мануэлем Дель Рио в свинцовых рудах. Он обнаружил новый металл и предложил для него название «панхромий» из-за широкого диапазона цвета его соединений, сменив затем название на «эритроний». Дель Рио не имел авторитета в научном мире Европы, и европейские химики усомнились в его результатах. Затем и сам Дель Рио потерял уверенность в своём открытии и заявил, что открыл всего лишь хромат свинца.

Куски цветного металла ванадия
В 1830 году ванадий был открыт заново шведским химиком Нильсом Сефстрёмом в железной руде. Новому элементу название дали Берцелиус и Сефстрём. Шанс открыть ванадий был у Фридриха Вёлера, исследовавшего мексиканскую руду, но он серьёзно отравился фтороводородом незадолго до открытия Сефстрёма и не смог продолжить исследования. Однако Вёлер довёл до конца исследование руды и окончательно доказал, что в ней содержится именно ванадий, а не хром.

Кристаллы цветного металла ванадия в запаянной ампуле
Тантал
Тантал — химический элемент с атомным номером 73 в Периодической системе химических элементов Д. И. Менделеева, обозначается символом Ta (лат. Tantalum). При стандартных условиях представляет собой блестящий серебристо-белый металл (со слабым свинцовым оттенком вследствие образования плотной оксидной плёнки).

Тантал в периодической системе Менделеева
Тантал открыт в 1802 году шведским химиком А. Г. Экебергом в двух минералах, найденных в Финляндии и Швеции. Однако в чистом виде выделить его не удалось. Из-за трудностей получения этот элемент был назван по имени героя древнегреческой мифологии Тантала.

Листы чистого цветного металла тантала
В последующем тантал и «колумбий» (ниобий) считали тождественными. Лишь в 1844 году немецкий химик Генрих Розе доказал, что минерал колумбит-танталит содержит два различных элемента — ниобий и тантал. Пластичный металлический тантал впервые получен немецким учёным В. Болтоном в 1903 году. Первый промышленный штабик тантала был получен в 1922 году, при этом он не превышал по величине спичечную головку. Тогда элемент начал применяться в выпрямителях тока и радиолампах. Активное производство тантала было развёрнуто в самом конце Второй Мировой войны.

Кусок танталовой мишени для нанесения тонких пленок тантала
Ниобий
Ниобий — элемент побочной подгруппы пятой группы пятого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, атомный номер — 41. Обозначается символом Nb (лат. Niobium). Простое вещество ниобий (CAS-номер: 7440-03-1) — блестящий металл серебристо-серого цвета с кубической объёмноцентрированной кристаллической решеткой типа α-Fe, а = 0,3294. Для ниобия известны изотопы с массовыми числами от 81 до 113.

Ниобий в периодической системе Менеделеева
Ниобий был открыт в 1801 г. английским учёным Чарльзом Хэтчетом в минерале, присланном ещё в 1734 году в Британский музей из штата Массачусетс Джоном Уинтропом (внуком Джона Уинтропа младшего). Минерал был назван колумбитом, а химический элемент получил название «колумбий» (Cb) в честь страны, откуда был получен образец — Колумбии (в то время синоним США).В 1802 году А. Г. Экеберг открыл тантал, который совпадал практически по всем химическим свойствам с ниобием, и поэтому долгое время считалось, что это один и тот же элемент.

Пруток чистого металлического ниобия (чистота 99.9%)
Лишь в1844 году немецкий химик Генрих Розе установил, что это отличный от тантала элемент и переименовал его в «ниобий» в честь дочери Тантала Ниобы, чем подчеркнул сходство между элементами. Однако в некоторых странах (США, Англии) долго сохранялось первоначальное название элемента — колумбий, и только в 1950 году решением Международного союза теоретической и прикладной химии (ИЮПАК, IUPAC) элементу окончательно было присвоено название ниобий. Впервые чистый ниобий был получен в конце XIX века французским химиком Анри Муассаном электротермическим путем, восстанавливая оксид ниобия углеродом в электропечи.

Кристаллы цветного металла ниобия
Хром — элемент побочной подгруппы 6-й группы 4-го периода периодической системы химических элементов Д. И. Менделеева с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром (CAS-номер: 7440-47-3) — твёрдый металл голубовато-белого цвета. Хром иногда относят к чёрным металлам.

Хром в периодической системе Менделеева
Хром, является самым твердым металлом, по крайней мере так пишут в учебниках. Пожалуй было бы точнее сказать: один из самых твердых. Кристаллы хрома и в самом деле царапают стекло на “на ура”, но например кусок иридия так же запросто оставляет царапину на хроме.

Мишень для вакуумного напыления из чистого цветного металла хрома (США, чистота 99.9%)
Открыт на Среднем Урале, в Березовском золоторудном месторождении. Впервые упоминается в труде М. В. Ломоносова «Первые основания металлургии» (1763 год), как красная свинцовая руда, PbCrO4. Современное название — крокоит. В 1797 французский химик Л. Н. Воклен выделил из него новый тугоплавкий металл (скорее всего, Воклен получил карбид хрома).

Друза кристаллов цветного металла хрома
Марганец
Марганец — элемент побочной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича с атомным номером 25. Обозначается символом Mn (лат. Manganum, ма́нганум, в составе формул по-русски читается как марганец, например, KMnO4 — калий марганец о четыре). Простое вещество марганец (CAS-номер: 7439-96-5) — металл серебристо-белого цвета. Наряду с железом и его сплавами относится к чёрным металлам. Известны пять аллотропных модификаций марганца — четыре с кубической и одна с тетрагональной кристаллической решёткой.

Марганец в периодической системе Менделеева
Один из основных минералов марганца — пиролюзит — был известен в древности как чёрная магнезия и использовался при варке стекла для его осветления. Его считали разновидностью магнитного железняка, а тот факт, что он не притягивается магнитом, Плиний Старший объяснил женским полом чёрной магнезии, к которому Магнит «равнодушен».

Куски цветного металла марганца
В 1774 г. шведский химик К. Шееле показал, что в руде содержится неизвестный металл. Он послал образцы руды своему другу химику Ю. Гану, который, нагревая в печке пиролюзит с углем, получил металлический марганец. В начале XIX века для него было принято название «манганум» (от немецкого Manganerz — марганцевая руда).

Кусочек марганца в запаянной колбе
Цирконий
Цирконий (лат. Zirconium; обозначается символом Zr) — элемент побочной подгруппы четвёртой группы пятого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 40. Простое вещество цирконий (CAS-номер: 7440-67-7) — блестящий металл серебристо-серого цвета. Обладает высокойпластичностью, устойчив к коррозии. Существует в двух кристаллических модификациях: α-Zr с гексагональной решёткой типа магния, β-Zr с кубической объёмноцентрированной решёткой типа α-Fe, температура перехода α↔β 863 °C.

Цирконий в периодической системе Менделеева
Цирконий в виде двуокиси впервые был выделен в 1789 году немецким химиком М. Г. Клапротом в результате анализа минерала циркона. В свободном виде цирконий впервые был выделен шведским химиком Берцелиусом в 1824 году. Свободный от примесей чистый цирконий удалось получить лишь в начале XX века. Происхождение самого слова циркон неясно. Возможно, оно происходит от арабского zarkûn (киноварь) или от персидского zargun (золотистый цвет).

Пруток из цветного металла циркония
Редкоземельные цветные металлы
Редкоземельные элементы (редкие земли) — группа из 17 элементов, включающая лантан, скандий, иттрий и лантаноиды. Все эти элементы — металлы серебристо-белого цвета, при том все имеют сходные химические свойства (наиболее характерна степень окисления +3).

Редкоземельные цветные металлы в ампулах
Лантан
Лантан — химический элемент побочной подгруппы третьей группы шестого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 57,атомная масса — 138,9055. Обозначается символом La (лат. Lanthanum). Простое вещество лантан (CAS-номер: 7439-91-0) — блестящий металл серебристо-белого цвета, относится к редкоземельным элементам.
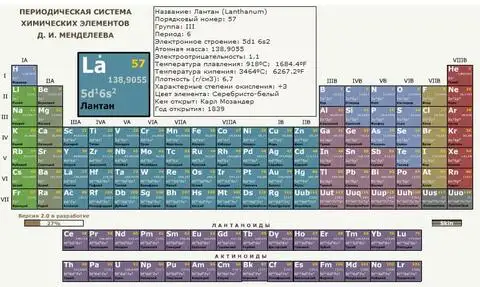
Лантан в периодической системе Менделеева
Лантан как химический элемент не удавалось открыть на протяжении 36 лет. В 1803 г. 24-летний шведский химик Йёнс Якоб Берцелиус исследовал минерал, известный теперь под названием церита. В этом минерале была обнаружена иттриевая земля и ещё одна редкая земля, очень похожая на иттриевую. Её назвали цериевой. В 1826 г. Карл Мозандер исследовал цериевую землю и заключил, что она неоднородна, что в ней, помимо церия, содержится ещё один новый элемент. Доказать сложность цериевой земли Мозандеру удалось лишь в 1839 г. Он сумел выделить новый элемент, когда в его распоряжении оказалось большее количество церита.

Цилиндрик из цветного металла лантана в запаянной ампуле с азотом
Церий
Церий — химический элемент из группы лантаноидов, серебристый металл. Церий – Се (Cerium), химический элемент III группы периодической системы элементов, атомный номер 58, атомная масса 140,12 относится к редкоземельным элементам.

Церий в периодической системе Менделеева
Церий был открыт в 1803 Й.Берцелиусом и В.Хизингером, а также независимо от них в том же году М.Клапротом. Назван в честь самой большой из малых планет, Цереры (Ceres), в свою очередь названной в честь римской богини плодородия. Немецкий химик М. Г. Клапрот, открывший цериевую землю почти одновременно со своими шведскими коллегами — В. Хизингером и Й. Я. Берцелиусом, возражал против названия «церий», предлагая «церерий». Берцелиус, однако, отстоял своё название, ссылаясь на трудности произношения того имени, которое предлагал новому элементу Клапрот.

Кусочек цветного металла церия, запаянный в ампулу
Празеодим
Празеодим — химический элемент из группы лантаноидов, серебристый металл. Празеодим — (лат. Praseodymium), Pr, химический элемент III группы периодической системы Менделеева, атомный номер 59, атомная масса 140,9077.

Празеодим в периодической системе Менделеева
Празеодим был открыт в 1885 году австрийским химиком Карлом Ауэром фон Вельсбахом. Он установил, что обнаруженный в 1839 году шведским химиком Карлом Мосандером элемент дидимявляется смесью двух элементов с близкими физическими и химическими свойствами, которым он дал названия неодим и празеодим.

Кусочки цветного металла празеодиома, запаянные в ампуле
Неодим
Неодим — химический элемент, редкоземельный металл серебристо-белого цвета с золотистым оттенком. Относится к группе лантаноидов. Легко окисляется на воздухе. Неодим (лат. Neodymium), Nd, химический элемент III группы периодической системы, атомный номер 60, атомная масса 144,24.

Неодим в периодической системе Менделеева
Неодим был открыт в 1885 году австрийским химиком Карлом Ауэром фон Вельсбахом. Он разделил дидим — смесь двух редкоземельных металлов, трудно разделяемую из-за чрезвычайной близости их химических свойств и ранее считавшуюся индивидуальным химическим элементом, — на неодим и празеодим. Получить неодим в чистом виде, практически свободном от примесей празеодима, удалось лишь в 1925 году. Используется как компонент сплавов с алюминием и магнием для самолёто- и ракетостроения.

Кусочки цветного металла неодима, запаянного в колбу
Самарий
Самарий — химический элемент, металл из группы лантаноидов. Самарий (Sm) — редкоземельный металл, атомный номер 62, атомная масса 150,36, температура плавления 1 074°C, плотность 7,45 г/см3.

Самарий в периодической системе Менделеева
Элемент был выделен из минерала самарскита ((Y,Ce,U,Fe)3(Nb,Ta,Ti)5O16). Этот минерал в 1847 году был назван в честь русского горного инженера, полковника В. Е. Самарского-Быховца (по предложению немецкого химика Генриха Розе, которому Самарский предоставил для исследования образцы этого минерала).

Цветной металл самарий в запаянной колбе
Новый, ранее неизвестный элемент в самарските был обнаружен спектроскопически французскими химиками Лафонтеном в 1878 году и Лекоком де Буабодраном в 1879 году. В 1880 году открытие было подтверждено швейцарским химиком Ж. де Мариньяком. Чистый металлический самарий был впервые химически выделен только в начале XX века.

Кусок цветного металла самария с оксидной пленкой
Европий
Европий — (Europium), Eu, химический элемент III группы периодической системы, атомный номер 63, атомная масса 151,96; относится к редкоземельным элементам, относится к группе лантаноидов.

Европий в периодической системе Менделеева
Европий — наиболее легкий лантаноид цериевой подгруппы, относящийся к категории редкоземельных, и характеризующийся наименьшей устойчивостью к корродирующему действию влажного воздуха и воды. Представляет собой мягкий и пластичный металл серебристо-белого цвета. Хранится исключительно в емкостях с жидким парафином или специальных ампулах. Относится к числу малотоксичных химических элементов. Влияние его на организм человека не доказано!

Цветной металл европий в запаянной колбе
Официально был получен в 1937 г., хотя ученые причисляют это открытие периоду 1886-1901 годов. Первыми полосу спектра, относимую впоследствии к европию, наблюдали Крукс (1886) и Лекок де Буабодран (1892). Демарсе обнаружил полосу спектра элемента в самариевой земле в 1896 году, а в 1901 году смог выделить элемент, описал его и дал ему название в честь Европы.

Около 300 грамм сублимированных дендритов цветного металла европия в специальном боксе
Гадолиний
Гадолиний (лат. Gadolinium), Gd — химический элемент III группы периодической системы Дмитрия Ивановича Менделеева, атомный номер — 64, атомная масса — 157,25. Относится к лантаноидам.

Гадолиний в периодической системе Менделеева
Гадолиний классифицируется как лантаноид, редкоземельный металл. Обнаружил его спектроскопическим путем в 1880 году французский исследователь Ж.-де-Мариньяк. Элемент получил свое название по имени его коллеги Ю. Гадолина. Элемент обладает наибольшим показателем по присоединению тепловых нейтронов среди известных металлов. Еще одной отличительной характеристикой является высокое удельное сопротивление.

Кусочки металла гадолиния в запаянной ампуле
В крайне малых количествах содержится в почве и соленой морской воде. Также обнаружен в составе некоторых минералов. Синтезируется путем восстановления хлорида, а также фторида гадолиния с использованием кальция.

Кусок цветного металла гадолиния
Тербий
Тербий (от названием селения Иттербю, Ytterby, в Швеции; лат. Terbium * а. terbium; к. Terbium; ф. terbium; и. terbio), Tb, — химический элемент III группы периодической системы Менделеева, атомный номер 65, атомная масса 158,9254, относится к лантаноидам. В чистом виде металл получили только в начале 20 столетия. Тербий — один из самых дорогих и редких металлов. Его получают путем выделения из смеси редкоземельных видов металла. Для этого подходят методы ионной экстракции или хроматографии.

Тербий в периодической системе Менделеева
В 1843 году шведский химик К. Г. Мосандер обнаружил примеси в концентрате Y2O3 и выделил из него три фракции: иттриевую, розовую terbia (которая содержала современный элемент эрбий) и бесцветную erbia (содержала элемент тербий, нерастворимый оксид тербия имеет коричневый оттенок).

Кусочки металла тербия в запаянной ампуле
Из-за бесцветности erbia существование этого соединения долгое время подвергалось сомнению, также были перепутаны названия фракций. Тербий в исходном концентрате составлял около 1 %, однако этого было достаточно, чтобы придать ему желтоватый оттенок. Чистый тербий начале XX века первым получил французский химик Жорж Урбэн, использовавший технологию ионного обмена.

Кусок металла тербия
Иттербий
Иттербий — элемент побочной подгруппы третьей группы шестого периода периодической системы химических элементов Д. И. Менделеева, лантаноид, атомный номер — 70. Обозначается символом Yb (лат. Ytterbium). Относится к редкоземельным элементам (иттриевая подгруппа).

Иттербий в таблице Менделеева
Простое вещество иттербий (CAS-номер: 7440-64-4) — металл светло-серого цвета. Существует в двух кристаллических модификациях: α-Yb с кубической решёткой типа медии β-Yb с кубической объёмноцентрированной решёткой типа α-Fe, температура перехода α↔β 792 °C.

Промышленный слиток цветного металла иттербия
Открыт Мариньяком в 1878 году в окиси эрбия. Жан-Шарль Галлисар де Мариньяк думал, что обнаружил его в 1878 году в иттриевой земле. Вначале предполагалось, что это — новый единый элемент, но в 1907 году удалось доказать, что на самом деле он состоит из двух элементов (Жорж Урбан, одновременно с Карлом Ауэр фон Вельсбах, выделил оксиды иттербия и лютеция)

Кусочки иттербия в запаянной ампуле
Диспрозий
Диспрозий (др.-греч. δυσπρόσιτος — труднодоступный) — химический элемент с атомным номером 66; редкоземельный металл с блеском серебра. Не встречается в природе в чистом виде, но входит в состав некоторых минералов, например, ксенотима.

Диспрозий в периодической системе Менделеева
Диспрозий – химический элемент иттриевой подгруппы, редкоземельный металл. Имеет серебристый цвет, характеризуется тусклым блеском. Медленно окисляется на воздухе, не растворяется в воде. Мало чем отличается по своим характеристикам от других лантаноидов, к числу которых причисляется.

Кусочки металла диспрозия в запаянной ампуле (10 грамм, чистота 99.9%)
Получается с помощью восстановления хлоридами, натрием, кальцием или литием. В малых количествах диспрозий входит в состав фосфоров, магнитных сплавов, специальных стекол. Его название переводится как «труднодоступный», что полностью подтверждает процесс его получения, требующий много времени. П. Э. Лекок де Буабодран открыл диспрозий в 1886 году при спектроскопическом анализе гольмии, или гольмиевой земли, а затем выделил оксид. В 1906 году Ж. Урбэн получил диспрозий в чистом виде.

Кусок цветного металла диспрозия
Гольмий
Гольмий(лат. Holmium), химический элемент III группы периодической системы, относится к лантаноидам. Название от латинского Holmia Стокгольм. Серебристо-белый металл; плотность 8,80 г/см3, tпл 1470ºC. Компонент специальных стёкол, активатор люминофоров.

Гольмий в периодической системе Менделеева
Открыт в 1879 шведским химиком Пьером Клеве Теодором. Исследуя выделенный незадолго до этого Карлом Густавом Мосандером оксид эрбия («эрбиевую землю»), он обнаружил смесь трех элементов — эрбия, гольмия и тулия.

Кристаллы цветного металла гольмия в запаянной ампуле
Эрбий
Эрбий (лат. Erbium) — Er, химический элемент III группы Периодической системы, атомный номер 68, атомная масса 167,26, относится к лантаноидам. Металл, плотность 9,045 г/см³, tпл 1522 .С. Компонент магнитных сплавов с железом, кобальтом, никелем.

Эрбий в периодической системе Менделеева
Впервые эрбий был выделен в 1843 году шведским химиком К. Г. Мосандером, из минерала, найденного около селения Иттербю.

Кусочки цветного металла эрбия
Тулий
Тулий (лат. Thulium) — химический элемент тринадцатой группы шестого периода периодической системы химических элементов. Обозначается символом Tm, атомный номер — 69, относится к группе лантаноидов. Простое вещество тулий представляет собой легко обрабатываемый металл серебристо-белого цвета.
Туллий в периодической системе Менделеева
Тулий был открыт шведским химиком П. Т. Клеве в 1879 году при поиске примесей к оксиду эрбия Er2O3. Этот же метод ранее позволил К. Г. Мосандеру открыть другие редкоземельные элементы. При выделении примесей Клеве получил два окисла — коричневый оксид гольмия и зелёный оксид тулия. В 1911 году Т. У. Ричардс получил элемент в чистом виде и измерил его атомный вес.

Кусочек цветного металла туллия в запаянной ампуле (аргоновая среда)
Лютеций
Лютеций — это (лат. Lutetium), Lu, химический элемент III группы периодической системы, атомный номер 71, атомная масса 174,967, относится к лантаноидам. Название от Lutecia — латинского названия Парижа. Серебристо-белый металл. Плотность 9,849 г/см3, tпл 1660 °С.

Лютеций в периодической системе Менделеева
Элемент в виде оксида в 1907 году независимо друг от друга открыли французский химик Жорж Урбэн, австрийский минералог Карл Ауэр фон Вельсбах и американский химик Чарльз Джеймс. Все они обнаружили лютеций в виде примеси к оксиду иттербия, который, в свою очередь, был открыт в 1878 г. как примесь к оксиду эрбия, выделенному в 1843 г. из оксида иттрия, обнаруженного в 1797 г. в минерале гадолините. Все эти редкоземельные элементы имеют очень близкие химические свойства. Приоритет открытия принадлежит Ж. Урбэну.

Кусочек цветного металла лютеция в запаянной ампуле
Прометий
Прометий — (лат. Promethium), Pm, химический элемент III группы Периодической системы элементов Дмитрия Ивановича Менделеева, атомный номер 61, атомная масса 144,9128, относится к лантаноидам. Радиоактивен; наиболее устойчивый изотоп 145Pm (период полураспада ?18 лет). В природе не найден, образуется при делении изотопа 235U в ядерных реакторах. Назван по имени Прометея. Металл, плотность 7,26 г/см3, tпл 1170 °С. Изотоп 147Pm применяют в люминофорах (светятся непрерывно несколько лет) и в миниатюрных атомных батарейках.

Прометий в периодической системе Менделеева
История открытия прометия наглядно демонстрирует те чрезвычайные трудности, которые пришлось преодолеть нескольким поколениям исследователей при изучении и открытии редкоземельных элементов. После открытия в 1907 году иттербия и лютеция считалось, что серия редкоземельных элементов полностью завершена.

Слиток редкоземельного цветного металла прометия
Однако некоторые видные исследователи редких земель, в частности, Б. Браунер, полагали, что в серии редких земель между неодимом и самарием должен существовать ещё один элемент, так как разница в атомной массе этих двух элементов была аномально высока. После того, как Г. Мозли установил связь заряда ядра атома с местом в Периодической системе, стало очевидным отсутствие в группе редкоземельных элементов элемента 61, и в 1920-х годах начались его интенсивные поиски.

Цветной металл прометиум
В 1924-1926 годах были заявления об открытии элемента 61 флоренций в Италии (из бразильского минерала монацита) и иллиний в Иллинойском университете в Урбана-Шампейн в США, впоследствии оказавшиеся ошибочными. В 1945 г. американские химики Д. Маринский, Л. Гленденин и Ч. Кориэлл выделили прометий из продуктов деления урана с помощью ионообменных смол. В 1947 г., благодаря исследованиям химических свойств прометия, было доказано существование нового элемента.

Кусок прометия
Скандий
Скандий (лат. Scandium; обозначается символом Sc) — элемент побочной подгруппы третьей группы, четвёртого периода периодической системы химических элементовД. И. Дмитрия Ивановича Менделеева, с атомным номером 21.

Скандий в периодической системе Менделеева
Простое вещество скандий (CAS-номер: 7440-20-2) — лёгкий металл серебристого цвета с характерным жёлтым отливом. Существует в двух кристаллических модификациях: α-Sc с гексагональной решёткой типа магния, β-Sc с кубической объёмноцентрированной решёткой, температура перехода α↔β 1336 °C.

Куски цветного металла скандия
Элемент был предсказан Д. И. Менделеевым (как экабор) в статье, датированной 11 декабря (29 ноября по старому стилю) 1870 года, и открыт в 1879 году шведским химиком Ларсом Нильсоном. Нильсон назвал элемент в честь Скандинавии.

Кусочек чистого цветного металла скандия в запаянной ампуле
Иттрий
Иттрий — элемент побочной подгруппы третьей группы пятого периода периодической системы химических элементов Д. И. Менделеева Дмитрия Ивановича, с атомным номером 39. Обозначается символом Y (лат. Yttrium). Простое вещество иттрий (CAS-номер: 7440-65-5) — металл светло-серого цвета. Существует в двух кристаллических модификациях: α-Y с гексагональной решёткой типа магния, β-Y с кубической объёмноцентрированной решёткой типа α-Fe, температура перехода α↔β 1482 °C.

Иттрий в периодической системе Менделеева
В 1794 году финский химик Юхан (Иоганн) Гадолин (1760-1852) выделил из минерала иттербита оксид элемента, который он назвал иттрием — по названию шведского населённого пункта Иттербю, находящегося на острове Ресарё, входящем в Стокгольмский архипелаг (иттербит был найден здесь в заброшенном карьере).

Кусок слитка цветного металла иттрия
В 1843 году Карл Мосандер доказал, что этот оксид на самом деле является смесью оксидов иттрия, эрбия и тербия и выделил из этой смеси Y2O3. Металлический иттрий, содержащий примеси эрбия, тербия и других лантаноидов, был получен впервые в 1828 году Фридрихом Велером.

Проточенный цилиндрик иттрия в запаянной ампуле
Рассеянные цветные металлы
Рассеянные элементы — химические элементы, которые практически не встречаются в природе в виде самостоятельных минералов и концентрированных залежей, а встречаются лишь в виде примесей в различных минералах. Рассеянные элементы извлекают попутно из руд других металлов или полезных ископаемых (углей, солей, фосфоритов, природных вод и пр.). К рассеянным элементам принадлежат рубидий, таллий, галлий, индий, скандий, германий и др.
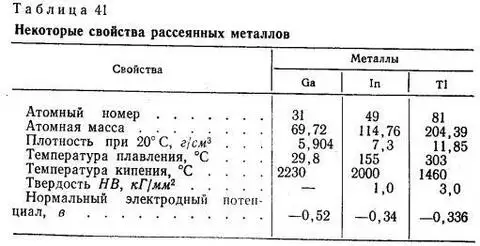
Рассеянные металлы — некоторые свойства
Индий
Индий — элемент 13-й группы периодической таблицы химических элементов (по устаревшей классификации — элемент главной подгруппы III группы), атомный номер 49. Обозначается символом In (лат. Indium). Относится к группе лёгких металлов. Простое вещество индий — ковкий, легкоплавкий, очень мягкий металл серебристо-белого цвета. Сходен по химическим свойствам с алюминием и галлием, по внешнему виду с цинком.

Индий в периодической таблице Менделеева
Индий обнаружили немецкие химики Фердинанд Райх и Теодор Рихтер (Theodore Richter) в 1863 году при спектроскопическом исследовании цинковой обманки. Они искали таллий, однако вместо зелёной линии этого элемента нашли в спектрах яркую неизвестную линию голубого цвета (Профессор Ф. Райх страдал дальтонизмом и не мог различать цвета спектральных линий, поэтому все наблюдения регистрировал его ассистент Рихтер).

Промышленный слиток цветного металла индия (1 кг, фирма Amalloy, чистота 99.99%)
Впоследствии металл был выделен Рихтером в незначительном количестве, но на Всемирной выставке 1867 г. уже был представлен полукилограммовый слиток Индия.

Цветной металл индий режется ножом почти как пластилин
Германий
Германий — химический элемент 14-й группы (по устаревшей классификации — главной подгруппы четвёртой группы) 4 периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 32. Обозначается символом Ge (нем. Germanium). Простое вещество германий (номер CAS 7440-56-4) — твёрдый металл серо-белого цвета, с металлическим блеском. Германий был открыт в 1886 году немецким химиком Клеменсом Винклером при изучении им минерала аргиродита.

Германий в периодической системе Менделеева
В природе германий встречается в сульфидных рудах, железной руде, обнаруживается почти во всех силикатах. Германий используется в электротехнической промышленности в качестве полупроводника в транзисторах и других электронных устройствах. Также германий широко применяется в волоконной и инфракрасной оптиках. Германий не является важным элементом для живых организмов. Но некоторые органические соединения Германия изучаются как потенциальные лекарственные средства, эффективность таких средств пока не доказана. Некоторые соединения Германия обладают токсичностью.

Слиток очень чистого германия, полученного зонной плавкой (чистоа 6N или >99.9999% )
В своём докладе о периодическом законе химических элементов в 1869 году русский химик Дмитрий Иванович Менделеев предсказал существование нескольких неизвестных на то время химических элементов, в частности и Германия. В статье, датированной 11 декабря (29 ноября по старому стилю) 1870 года, Д. И. Менделеев Дмитрий Иванович назвал неоткрытый элемент экасилицием (из-за его местонахождения в Периодической таблице) и предсказал его атомную массу и другие свойства.

Самодельный слиток цветного металла германия
В 1885 году в Фрайберге (Саксония) в одной из шахт был обнаружен новый минерал аргиродит. При химическом анализе нового минерала немецкий химикКлеменс Винклер обнаружил новый химический элемент. Учёному удалось в 1886 году выделить этот элемент, также химиком была отмечена схожесть Германия с сурьмой. Об открытии нового элемента Винклер сообщил в двухстраничной статье, датируемой 6 февраля 1886 года и предложил в ней имя для нового элемента Germanium и символ Ge. В последующих двух больших статьях 1886-1887 гг. Винклер подробно описал свойства Германия.

Кусочки цветного металла германия в запаянной ампуле
Первоначально Винклер хотел назвать новый элемент «нептунием», но это название было дано одному из предполагаемых элементов, поэтому элемент получил название в честь родины учёного — Германии. Путём анализа тетрахлорида Германия GeCl4 Винклер определил атомный вес Германия, а также открыл несколько новых соединений этого металла. До конца 1930-х годов германий не использовался в промышленности. Во время Второй мировой войны германий использовался в некоторых электронных устройствах, главным образом в диодах.

Монокристалл цветного металла германия
Таллий
Таллий — элемент 13-й группы периодической таблицы химических элементов (по устаревшей классификации — элемент главной подгруппы III группы), шестого периода,атомный номер 81. Обозначается символом Tl (лат. Thallium). Относится к группе тяжёлых металлов. Простое вещество таллий (CAS-номер: 7440-28-0) — мягкий металл серебристо-белого цвета с голубоватым оттенком.

Таллий в периодической системе Менделеева
Таллий был открыт спектральным методом в 1861 году английским учёным Уильямом Круксом в шламах свинцовых камер сернокислотного завода города Гарц. Чистый металлический таллий был независимо получен Круксом и французским химиком Клодом-Огюстом Лами в 1862 году. Название элемент получил по характерным зелёным линиям своего спектра и зелёной окраске пламени. От др.-греч. θαλλός — молодая, зелёная ветвь.

Кусочек цветного металла таллия в запаянной ампуле
Рений
Рений (лат. Rhenium) — химический элемент с атомным номером 75 в Периодической системе химических элементов Д. И. Дмитрия Ивановича Менделеева, обозначается символом Re. При стандартных условиях представляет собой плотный серебристо-белый переходный металл.

Рений в периодической системе Менделеева
Существование рения было предсказано Д. И. Менделеевым («тримарганец») в 1871 году, по аналогии свойств элементов в группе периодической системы. Элемент открыли в 1925 году немецкие химики Ида и Вальтер Ноддак, исследуя минерал колумбит спектральным анализом в лаборатории компании Siemens & Halske. Об этом было доложено на собрании немецких химиков в Нюрнберге. В следующем году группа учёных выделила из молибденита первые 2 мг рения. Относительно чистый рений удалось получить только в 1928 году. Для получения 1 г рения требовалось переработать более 600 кг норвежского молибденита.

Cлиток цветного металла рения, полученный методом электронно-лучевой плавки
Первое промышленное производство рения было организовано в Германии в 1930-х годах. Мощность установки составляла 120 кг в год, что полностью удовлетворяло мировую потребность в этом металле. В 1943 году в США после переработки молибденовых концентратов были получены первые 4,5 кг рения. Рений стал последним открытым элементом, у которого известен стабильный изотоп. Все элементы, которые были открыты позднее рения (в том числе и полученные искусственно), не имели стабильных изотопов.

Толстостенная трубка, изготовленная из рения
Гафний
Гафний — химический элемент 4-й группы длиннопериодной формы периодической системы Д. И. Менделеева Дмитрия Ивановича (по короткой форме периодической системы — побочной подгруппы IV группы), шестого периода, с атомным номером 72. Обозначается символом Hf (лат. Hafnium). Простое вещество — тяжёлый тугоплавкий серебристо-белый металл.

Гафний в периодической системе Менделеева
Элемент был открыт в 1923 г. Гафний искали среди редкоземельных элементов, так как не было выяснено строение 6-го периода системы Д. И. Дмитрия Ивановича Менделеева. В 1911 г. французский химик Ж. Урбен объявил об открытии нового элемента, названного им кельтием. В действительности он получил смесь, состоящую из иттербия, лютеция и небольшого количества гафния. И только после того, как Н. Бор на основании квантовомеханических расчётов показал, что последним редкоземельным элементом является элемент с номером 71, стало ясно, что гафний — аналог циркония.

Кусок прутка из цветного металла гафния
Базируясь на выводах Бора, который предсказал его свойства и валентность, в 1923 Дирк Костер и Дьёрдь де Хевеши систематически проанализировали рентгеноспектральным методомнорвежские и гренландские цирконы. Совпадение линий рентгенограмм остатков после выщелачивания циркона кипящими растворами кислот с вычисленными по закону Мозли для 72-го элемента позволило исследователям объявить об открытии элемента, который они назвали гафнием в честь города, где было сделано открытие (лат. Hafnia — латинское название Копенгагена).

Гафниевая стружка полученная обработкой прутка на токарном станке
Начавшийся после этого спор о приоритете между Ж. Урбеном, Н. Костером и Д. Хевеши продолжался длительное время. В 1949 г. название элемента «гафний» было утверждено Международной комиссией и принято всюду.

Гранулы цветного металла гафния в запаянной колбе
Селен
Селен — химический элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), 4-го периода в периодической системе, имеет атомный номер 34, обозначается символом Se (лат. Selenium), хрупкий блестящий на изломе неметалл чёрного цвета (устойчивая аллотропная форма, неустойчивая форма — киноварно-красная). Относится к халькогенам.

Селен в периодической системе Менделеева
Cелен открыт в 1817 году Йенсом Якобом Берцелиусом. Сохранился рассказ самого Берцелиуса о том, как произошло это открытие: » Я исследовал в содружестве с Готлибом Ганом метод, который применяют для производства серной кислоты в Грипсхольме. Мы обнаружили в серной кислоте осадок, частью красный, частью светло-коричневый.

Ампула с гексагональным или металлическим селеном
Любопытство, вызванное надеждой обнаружить в этом коричневом осадке новый редкий металл, заставило меня исследовать осадок. . Я нашел, что масса (то есть осадок) содержит до сих пор неизвестный металл, очень похожий по своим свойствам на теллур. В соответствии с этой аналогией я назвал новое тело селеном (Selenium) от греческого selhnh (луна), так как теллур назван по имени Tellus — нашей планеты «.

Излом слитка стекловидного селена
Теллур
Теллур — химический элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы, халькогены), 5-го периода в периодической системе, имеет атомный номер 52; обозначается символом Te (лат. Tellurium), относится к семейству металлоидов.

Теллур в периодической системе Менделеева
Впервые был найден в 1782 году в золотоносных рудах Трансильвании горным инспектором Францем Йозефом Мюллером (впоследствии барон фон Райхенштейн), на территории Австро-Венгрии. В 1798 году Мартин Генрих Клапрот выделил теллур и определил важнейшие его свойства. Название происходит от латинского tellus, родительный падеж telluris, Земля.

Слиток цветного металла теллура высокой чистоты (очищен зонной плавкой)
Радиоактивные цветные металлы
Радиоактивные металлы (radioactive metals) — это металлы, занимающие места в Периодической системе элементов с атомным номером больше 83 (Bi), испускающие радиоактивные частицы:нейтроны, протоны, альфа-, бетачастицы или гамма-кванты. В природе обнаружены: At, Ac, Np, Pa, Ро, Pm,Pu, Ra, Тс, Th, U. Остальные радиоактивные металлы, как и большинство найденных в природе (кроме U, Thи Ra), получают посредством ядерных реакций.

Значек радиционной опасности
Уран (устаревший вариант ураний) — химический элемент с атомным номером 92 в периодической системе, атомная масса — 238,029; обозначается символом U (лат. Uranium), относится к семейству актиноидов. При нормальных условиях — металл. Уран — слаборадиоактивный элемент, он не имеет стабильных изотопов. Самым распространенным изотопом урана является уран-238 (имеет 146 нейтронов, составляет 99,3 % из всего урана в природе) и уран-235 (143 нейтрона, ≈0,7 % всего урана, найденного в природе).

Уран в периодической системе Менделеева
Ещё в древнейшие времена (I век до нашей эры) природная окись урана использовалась для изготовления жёлтой глазури для керамики. Первая важная дата в истории урана — 1789 г., когда немецкий натурфилософ и химик Мартин Генрих Клапрот восстановил извлечённую из саксонской смоляной руды золотисто-жёлтую «землю» до чёрного металлоподобного вещества.

Кусок радиоактивного металла урана
В честь самой далёкой из известных тогда планет (открытой Гершелем восемью годами раньше) Клапрот, считая новое вещество элементом, назвал его ураном (этим он хотел поддержать предложение Иоганна Боде назвать новую планету «Уран» вместо «Звезда Георга», как предложил Гершель). Пятьдесят лет уран Клапрота числился металлом. Только в 1841 г. французский химик Эжен Мелькиор Пелиго (англ.) (1811-1890) доказал, что, несмотря на характерный металлический блеск, уран Клапрота не элемент, а оксид UO2.
Кусочек урана в специальной запаянной колбе
В 1840 г. Пелиго удалось получить настоящий уран — тяжёлый металл серо-стального цвета — и определить его атомный вес. Следующий важный шаг в изучении урана сделал в 1874 г. Д. И. Менделеев Дмитрий Иванович. Опираясь на разработанную империодическую систему, он поместил уран в самой дальней клетке своей таблицы. Прежде атомный вес урана считали равным 120. Великий химик удвоил это значение. Через 12 лет предвидение Дмитрия Ивановича Менделеева было подтверждено опытами немецкого химика Циммермана.

Диск из цветного радиоактивного металла урана
Торий
Торий — (лат. Thorium) — Th, химический элемент III группыпериодической системы, атомный номер 90, атомная масса 232,0381, относится к актиноидам.Радиоактивен, наиболее устойчивый изотоп 232Th (период полураспада 1,389.1010 лет). Название от именибога Тора. Серебристо-белый металл; плотность 11,724 г/см³, tпл 1750 .С. Добывают главным образом измонацита. Применяется для легирования сплавов, как геттер при изготовлении электроламп. Перспективноеядерное топливо, в котором 232Th мог бы превращаться в уран 233U. Последний может участвовать вцепной реакции деления. ThO2 — огнеупорный материал.
Торий в периодической системе Менделеева
Торий получил название за 15 лет до того, как был открыт. В 1815 г. Берцелиус, анализируя один редкий минерал из округа Фалюн в Швеции, пришел к заключению, что в нем содержится новый металл, который Берцелиус поспешил наименовать торием. И хотя это заключение было совершенно ошибочным, в те времена мало кто мог оспаривать результаты анализа, сделанного столь авторитетным ученым. Ошибку обнаружил 10 лет спустя сам Берцелиус. Оказалось то, что он принял за окисел нового металла, было основным фосфатом иттрия. Однако название торий оказалось весьма живучим.

Кусочек цветного металла тория в запаянной ампуле
В 1828 г. Берцелиус получил из Норвегии образец минерала, найденного в сиенитах на острове Левен. Черный тяжелый мягкий минерал (он легко резался ножом) был похож на гадолинит и в нем можно было подозревать присутствие тантала. По просьбе норвежских ученых отца и сына Эсмарк Берцелиус сделал анализ минерала и обнаружил, что он состоит из кремнезема и окисла неизвестного металла, который вновь получил название торий (Thorium) от имени древнескандинавского божества Тора.

Порошок и фольга из тория в запаянной ампуле
Эсмарки предложили назвать новый минерал в честь Берцелиуса берцелитом, но сам Берцелиус дал ему общепринятое название торит (силикат тория). Попытки Берцелиуса выделить торий в металлическом виде не увенчались успехом. Это сделал Нильсон в 1882 г.

Куски и порошок тория
Протактиний
Протактиний — (лат. Protactinium) — Pa, химический элемент IIIгруппы Периодической системы элементов Менделеева Дмитрия Ивановича, атомный номер 91, атомная масса 231,0359,относится к актиноидам. Радиоактивен; наиболее устойчивый изотоп 231Pa (период полураспада 32 500лет). Название от греч. protos — первый и актиний (изотоп 227Ac образуется при a-распаде 231Pa). Светло-серый металл, плотность 15,37 г/см³, tпл ок. 1570 .С. Добывают из урановой руды.

Протактиний в периодической системе Менделеева
В результате расширения исследований радиоактивных превращений урана становилось все очевиднее, что актиний является продуктом одного из таких превращений. В частности, это подтверждалось постоянством отношения актиний: уран в урановых минералах. Однако установить последовательность превращений и найти звенья цепи образования актиния удалось не сразу. Содди, Руссель и Фаянс независимо друг от друга предсказали существование радиоактивного элемента — члена уранового ряда, который как аналог тантала (эка-тантал) должен занять пустующую клетку ниже ванадия.

Радиоактивный и цветной металл протактиний
И действительно, в 1917 г. Мейтнер, а год спустя Содди, Крэнстон и Флэкк открыли элемент 91, который оказался первым в ряду актиния, образуя актиний в результате аlfa-излучения. Элемент наименовали протактинием от греч.первый, исходный, начальный и актиний. Название это фиксирует тот факт, что протактиний является исходным элементом в ряду образования актиния. В 1927 г. Гроссе впервые выделил несколько миллиграмм чистой пятиокиси протактиния (Ра2О5).
Протактиний
Радий
Радий — элемент главной подгруппы второй группы, седьмого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 88. Обозначается символом Ra (лат. Radium). Простое вещество радий (CAS-номер: 7440-14-4) — блестящий щёлочноземельный металл серебристо-белого цвета, быстро тускнеющий на воздухе. Обладает высокой химической активностью. Радиоактивен; наиболее устойчив нуклид 226Ra (период полураспада около 1600 лет).

Радий в периодической системе Менделеева
Французские ученые Пьер и Мария Кюри обнаружили, что отходы, остающиеся после выделения урана из урановой руды (урановая смолка, добывавшаяся в городе Иоахимсталь, Чехия), более радиоактивны, чем чистый уран. Из этих отходов супруги Кюри после нескольких лет интенсивной работы выделили два сильно радиоактивных элемента: полоний и радий. Первое сообщение об открытии радия (в виде смеси с барием) Кюри сделали 26 декабря 1898 года во Французской Академии наук.

Факт о радиоактивном металле радии
В 1910 году Кюри и Андре Дебьерн выделили чистый радий путём электролизахлорида радия на ртутном катоде и последующей дистилляции в водороде. Выделенный элемент представлял собой, как сейчас известно, изотоп радий-226, продукт распада урана-238. За открытие радия и полония супруги Кюри получили Нобелевскую премию. Радий образуется через многие промежуточные стадии при радиоактивном распаде изотопа урана-238 и поэтому находится в небольших количествах в урановой руде.

Радиоактивный и цветной металл радий 226
Актиний
Актиний — химический элемент с атомным номером 89, обозначается в периодической системе элементов символом Ac (лат. Actinium). Не имеет стабильных изотопов. При нормальных условиях представляет собой тяжёлый серебристо-белый металл. Относится к семейству актиноидов.

Актиний в периодической системе Менделеева
Актиний был открыт в 1899 году А. Дебьерном в отходах от переработки урановой смолки, из которой удалили полоний и радий. Новый элемент был назван актинием. Вскоре после открытия Дебьерна независимо от него немецкий радиофизик Ф. Гизель из такой же фракции урановой смолки, содержащей редкоземельные элементы, получил сильно радиоактивный элемент и предложил ему название «эманий». Дальнейшее исследование показало идентичность препаратов, полученных Дебьерном и Гизелем, хотя они наблюдали радиоактивное излучение не самого актиния, а продуктов его распада — 227Th (радиоактиний) и 230Th (ионий).

Радиоактивный актиний
Нептуний
Нептуний — химический элемент с атомным номером 93 в периодической системе; обозначается символом Np, относится к семейству актиноидов. Это первый трансурановый элемент, на Земле он встречается лишь в следовых количествах, и был получен искусственно из урана посредством ядерных реакций.

Нептуний в периодической системе Менделеева
До принятия теории расщепления атомного ядра, которая обосновала существование синтезированного позднее реального такого элемента, трижды были сделаны оказавшиеся ошибочными объявления о независимых открытиях элемента 93: аусоний (Ausonium) в Италии (Энрико Ферми) и богемий (Bohemium) в Чехословакии в 1934 и секваний (Sequanium) в Румынии в 1939. Нептуний был впервые получен Э. М. Макмилланом и Ф. Х. Абельсоном в 1940 году. Реакция синтеза: 238U(n,γ)239U(β−)239Np.

Радиоактивный и цветной металл нептуний
Плутоний
Плутоний (обозначается символом Pu; атомное число 94) — тяжёлый хрупкий радиоактивный металл серебристо-белого цвета. В периодической таблице располагается в семействе актиноидов. Плутоний был открыт в конце 1940 г. в Калифорнийском университете. Его синтезировали Мак-Миллан, Кеннеди и Валь, бомбардируя окись урана (U3O8) сильно ускоренными в циклотроне ядрами дейтерия (дейтронами).

Плутоний в периодической системе Менделеева
Позднее было установлено, что при этой ядерной реакции сначала получается короткоживущий изотоп нептуний-238, а из него уже плутоний-238 с периодом полураспада около 50 лет. Годом позже Кеннеди, Сиборг, Сегрэ и Валь синтезировали более важный изотоп — плутоний-239 посредством облучения урана сильно ускоренными в циклотроне нейтронами. Плутоний-239 образуется при распаде нептуния-239; он испускает alfa-лучи и имеет период полураспада 24 000 лет. Чистое соединение плутония впервые получено в 1942 r. Затем стало известно, что существует природный плутоний, обнаруженный в урановых рудах, в частности в рудах, залегах в Конго.

Кольцо из радиоактивного и цветного металла плутония
Название элемента было предложено в 1948 г.: Мак-Миллан назвал первый трансурановый элемент нептунием в связи с тем, что планета Нептун — первая за Ураном. По аналогии элемент 94 решили назвать плутонием, так как планета Плутон является второй за Ураном. Плутон, открытый в 1930 г., получил свое название от имени бога Плутона — властителя подземного царства по греческой мифологии. В начале XIX в. Кларк предлагал наименовать плутонием элемент барий, производя это название непосредственно от имени бога Плутона, но его предложение не было принято.

Плутоний в специальном контейнере
Америций
Америций — (лат. Americium), химический элемент III группы периодической системы, относится к актиноидам.Радиоактивен, наиболее устойчивый изотоп 243Am (период полураспада 7370 лет). Название от слова«Америка» (по месту открытия). Серебристый металл, плотность 13,67 г/см3, tпл 1173ºC.

Америций в периодической системе Менделеева
Синтезирован в конце 1944 — начале 1945 американскими учёными Г. Сиборгом, Р. Джеймсом, Л. Морганом и А. Гиорсо в результате облучения плутония 239Pu нейтронами. Название А. дано от слова «Америка» по аналогии с гомологом А. в ряду лантаноидов — европием, который занимает после лантана такое же место (шестое), как и А. после актиния. Известны изотопы А. с массовыми числами 237-246 и ядерные изомеры 242mAm, 244mAm и т. н. делящиеся ядерные изомеры 238mfAm, 240mfAm, 242mf.

Радиоактивный и цветной металл америций-241
Калифорний
Калифорний — (лат. Californium), Cf, химический элемент III группы периодической системы, атомный номер 98, относится к актиноидам. Свойства: радиоактивен, наиболее устойчивый изотоп 251Cf (период полураспада 900 лет). t>пл 900 °С.

Калифорний в периодической системе Менделеева
Калифорний впервые получен в 1950 группой американских ученых (С. Томпсон, А. Гиорсо, К. Стрит и <>Г. Сиборг ) при облучении нескольких микрограмм 242Cm a-частицами, разогнанными на ускорителе до энергии 35 МэВ по ядерной реакции: 242 96 Cm(, 2n) 24498Bk. Назван по американскому штату Калифорния, в научно-исследовательском центре которого был открыт этот элемент.

Кусочек калифорния под микроскопом
Эйнштейний
Эйнштейний — (лат. Einsteinium), Es,- радиоакт. хим. элемент III группы периодич. системы элементов, ат. номер 99,относится к тяжёлым актиноидам (т. н. трансплутониевым элементам). Радиоактивный, серебристый металл. Известны изотопы Эйнштейния с массовыми числами 245-256, все они радиоактивны.

Эйнштейний в периодической системе Менделеева
Открыт в 1952 А. Гиорсо (A. Ghiorso), C. Томпсоном (S. G. Thompson) и Г. Хиггинсом (G. H. Higgins), назван в честь А. Эйнштейна. А.Гьорсо и Г.Т.Сиборг (Беркли, США) в продуктах взрыва термоядерного устройства, произведенного на коралловом островке Элугелаб, входящем в атолл Эниветок в Тихом океане в ноябре 1952 (операция «Майк) обнаружили два новых элемента — эйнштейний и фермий.

Свечение эйнштейния (253Es) в темноте
Обнаруженный изотоп 253Es с периодом полураспада T = 20,5 сут образовался при β -распаде 253U и дочерних изотопов (253U образовался в результате преимущественно последовательного захвата 15 нейтронов ядрами 238U). Затем были найдены и другие пути синтеза элемента. В частности, этот элемент был получен при применении бомбардировке ионами азота урановых мишеней.
Радиоактивный и цветной металл Эйнштений
Фермий
Фермий — (лат. Fermium), химический элемент III группы периодической системы, относится к актиноидам. Радиоактивен, наиболее устойчивый изотоп 257Fm (период полураспада 100,5 сут). Химический элемент (Fm) , радиоактивный металл серебристо-белого цвета, относящийся к актиноидам. Назван в честь итальянского физика Э.Ферми (1901 — 1954), получен искусственно. В свободном виде должен проявлять свойства металла.

Фермий в периодической системе Менделеева
Впервые фермий получен в конце 1952 года американцем А. Гиорсо и другими учеными Лос-Аламосской лаборатории в виде изотопа 255Fm с периодом полураспада Т1/2 = 20,1 ч, который содержался в пыли после первого термоядерного взрыва, произведённого США на атолле Эниветок 1 ноября 1952 года. Обнаруженный изотоп — продукт последовательного захвата 17 нейтронов ядрами 238U и восьми β−-распадов, превращающих нейтроны в протоны и увеличивающих атомный номер нуклида.
Сплав фермия и иттербия (Oak Ridge National Laboratory)
Менделевий
Менделевий — Mendelevium, Md, радиоактивный химический элемент III группы периодической системы, атомный номер 101; относится к актинидам; металл. Наиболее характерная валентность менделевия равна 3+.Менделевий — трансфермиевый химический элемент с атомным номером 101 в периодической системе, обозначается символом Md. Назван в честь Дмитрия Ивановича Дмитрия Ивановича Менделеева, создателя периодической системы элементов.

Менделевий в периодической системе Менделеева и описание
Впервые 256Md (период полураспада около 1 ч) получен американскими физиками А.Гиорсо, Б.Харви, Г.Шоппеном, С.Томсоном и Г.Сиборгом в 1955 при бомбардировке ничтожных количеств 253Es ионами гелия в 152-см циклотроне в Беркли (Калифорния, США). Первая идентификация элемента была удивительна, так как в опытах было получено всего 1 или 2 атома элемента. 258Md был получен в 1967. Оказалось, что он имеет исключительно большой период полураспада (

Менеделевий радиоактивный и цветной металл
Нобелий
Нобелий (No, лат. Nobelium) — искусственно полученный трансфермиевый химический элемент группы актиноидов с атомным номером 102. Имеет несколько нестабильных изотопов, самый долгоживущий из которых 259No имеет период полураспада 58 минут. Первыми об открытии 102 элемента заявила в 1957 году группа учёных, работавших в Стокгольме (Швеция). Они же и предложили назвать элемент нобелий в честь Альфреда Нобеля. Однако позже эти данные не были подтверждены работами других лабораторий.

Нобелий в периодической системе Менделеева
102 элемент был впервые получен в ходе экспериментов на ускорителе Объединённого института ядерных исследований в Дубне в 1963 году-1967 годах группой Г. Н. Флёрова. Независимо от них примерно в то же время элемент был получен и в Калифорнийском университете в г. Беркли (США).

Объединенный институт ядерных исследований в Дубне
В 1992 году международное научное сообщество признало приоритет открытия 102 элемента за физиками Дубны. В СССР это достижение было признано как научное открытие и занесено в Государственный реестр открытий СССР под № 34 с приоритетом от 9 июля 1963 г.

Из истории открытия нобелия
Советские исследователи предложили назвать новый элемент жолиотий (Jl) в честь Фредерика Жолио-Кюри, а американцы дали ему имя нобелий (No). Оба этих названия (Jl и No) имели хождение в изданных в разные годы Периодических таблицах элементов, пока, согласно решению ИЮПАК, за 102 элементом не было закреплено название нобелий в честь Альфреда Нобеля.

Из истории открытия нобелия — продолжение
Лоуренсий
Лоуренсий (Lr, англ. Lawrencium) — искусственно полученный химический элемент группы актиноидов с атомным номером 103. Атомная масса (266) (по наиболее долгоживущему из известных изотопов, 266Lr). Элемент 103 был получен в СССР на ускорителе в Объединённом институте ядерных исследований (наукоград Дубна) в 1961-1965 г. группой Г. Н. Флёрова и независимо в Национальной лаборатории им. Лоуренса в Беркли (США, 14 февраля 1961 г.).

Лоуренcий в периодической системе и описание
Советское достижение в СССР было признано как научное открытие и занесено в Государственный реестр открытий СССР под № 132 с приоритетом от 20 апреля 1965 г. в следующей формулировке: «Экспериментально обнаружено неизвестное ранее явление образования элемента с атомным номером 103, впервые полученный изотоп которого синтезирован при облучении америция-243 ионами кислорода-18. Имеет массовое число 256, период полураспада 35 с и сложный спектр энергий альфа-частиц в интервале 8,3-8,6 мегаэлектрон-вольт».

Лаборатория Калифорнийского университета, где было открыты различные химические элементы
Получение и производство цветных металлов
Цветные металлы играют большую роль в промышленности. Самый «популярный» металл – это алюминий. Не менее нужными являются свинец, олово, медь и другие цветные металлы, широко применяемые на производстве. Цветные металлы производятся из различных руд, содержащих тот или иной металл, отрасль промышленности, занимающаяся получением цветных металлов называется цветной металлургией.

Производство алюминия в процессе
Цветная металлургия
Цветная металлургия — отрасль металлургии, которая включает добычу, обогащение руд цветных металлов и выплавку цветных металлов и их сплавов. По физическим свойствам и назначению цветные металлы условно можно разделить натяжёлые (медь, свинец, цинк, олово, никель) и лёгкие (алюминий, титан, магний). На основании этого деления различают металлургию лёгких металлов и металлургию тяжёлых металлов.

Описание цветной металлургии
Основные сплавы цветных металлов
Сплав — макроскопически однородный металлический материал, состоящий из смеси двух или большего числа химических элементов с преобладанием металлических компонентов. Сплавы состоят из основы (одного или нескольких металлов), малых добавок специально вводимых в сплав легирующих и модифицирующих элементов, а также из не удалённых примесей (природных, технологических и случайных). Сплавы являются одним из основных конструкционных материалов. Среди них наибольшее значение имеют сплавы на основе железа и алюминия. В технике применяется более 5 тыс. сплавов.

Описание и определение цветных сплавов
Латунь (медь, цинк)
Латунь — сплав меди с цинком (10. 40 %), хорошо поддается холодной прокатке, штамповке, вытягиванию <7ь = 25О. 4ОО МПа, 6=35..15%. При маркировке лату-ней (Л96, Л90, . Л62) цифры указывают на содержание меди в процентах. Кроме того, выпускают латуни многокомпонентные, т. е. с другими элементами (Мп, Sn, Pb, Al).

Металлопрокат из латуни — прутки
Бронза (медь, олово и др.)
Бронза — сплав меди с оловом (до 10%), алюминием, марганцем, свинцом и другими элементами. Обладает хорошими литейными свойствами (вентили, краны, люстры). При маркировке бронзы Бр.ОЦСЗ-12-5 отдельные индексы обозначают: Бр — бронза, О — олово, Ц — цинк, С — свинец, цифры 3, 12, 5 — содержание в процентах олова цинка, свинца. Свойства бронзы зависят от состава: бв=15О. 21О МПа, б=4. 8%, НВ60 (в среднем).

Бронзовые прутки — металлопрокат из бронзы
Силумины (алюминий, кремний)
Силумины — сплавы алюминия с кремнием (до 14%), они обладают высокими литейными качествами, малой усадкой, прочностью ои = 200 МПа, твердостью НВ50. 70 при достаточно высокой пластичности 6== =5. 10 %. Механические свойства силуминов можно существенно улучшить путем модифицирования. При этом увеличивается степень дисперсности кристаллов, что повышает прочность и пластичность силуминов.

Детали и изделия из силумина
Дюралюмины, дюралюминий (алюминий, медь и др.)
Дюралюмины — сложные сплавы алюминия с медью (до 5,5 %), кремнием (менее 0,8%). марганцем (до 0,8 %), магнием (до 0,8 %) и др. Их свойства улучшают термической обработкой (закалкой при температуре 500. 520°С с последующим старением). Старение осуществляют на воздухе в течение 4. 5 сут при нагреве на 170°С в течение 4. 5 ч.

Прокат из дюралюминия — прутки
Цветная металлургия мира

Характеристика цветной металлулгии мира (часть первая)

Характеристика цветной металлургии мира (часть вторая)
Значение России в цветной металлургии мира
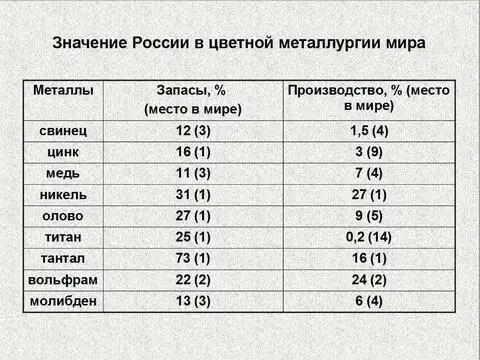
Значение России в цветной металлургии мира
Производство и запасы основных цветных металлов в мире
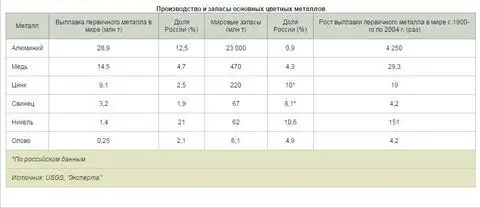
Таблица производства и запасов цветных металлов в мире
Применение цветных металлов
Цветные металлы — это распространенное сырье для производства металлопроката, металлических конструкций и изделий из металла. Оно востребовано большинством областей современной промышленности. Область применения цветных металлов очень широка: машиностроение, радиоэлектроника, сфера высоких технологий, бытовые коммуникации. Цветной металл обычно представлен изделиями проката, которые являются своего рода полуфабрикаты для дальнейшего использования.

Некоторое описание применения цветных металлов
Сортовой прокат, листовой прокат и прочие изделия проката становятся сырьем для дальнейшей обработки и использования, в качестве отдельных компонентов в разных сферах деятельности. Спрос на цветные металлы и сплавы постоянно растет, так как они все шире применяются в современной технике. Цветные металлы используются в авиастроении, ракетной и атомной технике, химической промышленности. В последнее время стали применять в качестве конструкционных материалов такие металлы и сплавы на их основе, как титан, цирконий, никель, молибден и даже ниобий, гафний и др.

Прокат из цветных металлов и некоторые изделия
Цветные металлы в бытовой сфере
Быт — часть физической и социальной жизни человека, включающая удовлетворение духовных и материальных потребностей в: пище, одежде для защиты от неблагоприятного воздействия окружающей среды (одежда, обувь и др.), жилье́, поддержании физического здоровья, сохранении и продолжении семьи (рода). Быт в широком смысле — уклад стереотипного видения повседневной жизни. Часто проводится противопоставление быта как «низкой» стороны жизни человека и различных «высоких» сторон: любовь, культура, наука, другие. Любопытно, что краткий термин с полным соответствием понятию «быт» отсутствует во многих языках (например, в английском).

Определение понятия быт
Термометры (ртуть)
Ртуть широко применяется в производстве термометров. Температура плавления ртути — –38 градусов, кипения — +356.58. Но существуют способы расширить эти границы и производить термометры, работающие как при более низких, так и при более высоких температурах. Для понижения температуры плавления, в ртуть добавляют таллий (забавная комбинация, два наиболее токсичных металла) – образующийся эвтектический сплав плавится при – 60 градусах.

Ртутный термометр
Чтобы повысить температуру кипения ртути, нужно увеличить давление. Этого достигают, закачивая в капилляр над ртутью примерно 30 атмосфер азота. При этом давлении, температура кипения поднимается до 600 градусов. Термометр выполнен в виде толстостенного капилляра. Поскольку при 600 градусах стекло может уже очень медленно течь, такие термометры нельзя применять для длительных измерений.
Медицинские ртутные термометры
Алюминиевая посуда (алюминий)
Преимущества алюминиевой посуды в хорошей теплопроводности, лёгкости в эксплуатации. Пригодна для нанесения антипригарных покрытий. По методу производства бывает литой и штампованной. Штампованная посуда достигает 5 мм в толщину, днище литой посуды начинается с 4 мм и доходит до 10 мм. Как правило, чем толще днище посуды, тем лучше в ней распределяется тепло и тем лучше сама посуда, конечно, необходимо обращать внимание и на характеристики антипригарного покрытия, нанесённого на посуду.

Кастрюли алюминиевые
Так же производителями посуды выпускается продукция из анодированного алюминия (anodised aluminium) — алюминий с прочным оксидным покрытием, получаемым с помощью электролитической ванны. В советские времена практиковался выпуск и непокрытой алюминиевой посуды, но так как контакт алюминия с пищей приводит к химической реакции и выделению металла в пищу, на данный момент такая посуда мало встречается в обиходе. В нынешнее время, также, существует одноразовая алюминиевая посуда — касалетки.

Одноразовая алюминиевая посуда (касалетка)
Лампы накаливания (вольфрам)
Лампа накаливания — искусственный источник света, в котором свет испускает тело накала, нагреваемое электрическим током до высокой температуры. В качестве тела накала чаще всего используется спираль из тугоплавкого металла (чаще всего — вольфрама), либо угольная нить. Чтобы исключить окисление тела накала при контакте с воздухом, его помещают в вакуумированную колбу, либо колбу, заполненную инертными газами или парами галогенов.

Лампа накаливания общего назначения
Столовые приборы (серебро, алюминий и др.)
Столовый прибор — инструмент или набор инструментов для манипуляций с пищей непосредственно за столом, изготавливается из пластмассы, дерева, алюминия, нержавеющей стали, мельхиора или столового серебра. Приборы из столового серебра и мельхиора применяют при сервировке столов на приёмах, банкетах и торжественных вечерах.

Набор серебрянных столовых приборов
Стеклянные зеркала (алюминий)
Зеркало — гладкая поверхность, предназначенная для отражения света (или другого излучения). Наиболее известный пример — плоское зеркало. Практически все стеклянные зеркала, изготовленные до начала XX века, имеют серебряный зеркальный слой. Он наносился на стекло или натиранием серебряной амальгамой или осажденем серебра из раствора (например по известной «реакции серебряного зеркала»). В настоящее время, серебро в производстве зеркал практически повсеместно вытеснено алюминием, который наносят на стекло методом вакуумного напыления.

Большое стеклянное зеркало в комнате
У этого процесса существует несколько вариантов: магнетронное напыление, испарение электронным пучком, резистивное напыление. В последнем варианте, алюминий (например в виде вот таких таблеток-цилиндриков), нагревается в высоком вакууме, испаряется и конденсируется на поверхности стекла формируя зеркальный слой. Для получения равномерного, качественного покрытия, исходный алюминий должен иметь высокую чистоту. Чистота металла в таблетках на первом фото — 4N.

Таблетки алюминия с чистотой 4N
На втором — в таблетках меньшего размера — 5N.

Таблетки алюминия с чистотой 5N
Люминесцентные газоразрядные лампы (ртуть, кальций и др)
Люминесцентная лампа — газоразрядный источник света, в котором электрический разряд в парах ртути создаёт ультрафиолетовое излучение, которое преобразуется в видимый свет с помощью люминофора — например, смеси галофосфата кальция с другими элементами.

Люминесцентные газоразрядные лампы
Никель-кадмиевые батареи (никель, кадмий)
Никель-кадмиевый аккумуля́тор (NiCd) — вторичный химический источник тока, в котором катодом является гидрат закиси никеля Ni(OH)2 с графитовым порошком (около 5–8%), электролитом — гидроксид калияKOH плотностью 1,19–1,21 с добавкой гидроксида лития LiOH (для образования никелатов лития и увеличения ёмкости на 21–25%), анодом — гидрат закиси кадмия Cd(OH)2 или металлический кадмий Cd (в виде порошка). ЭДС никель-кадмиевого аккумулятора — около 1,37 В, удельная энергия — порядка 45–65 Вт·ч/кг.

Никель-кадмиевые аккумуляторы (батарейки)
В зависимости от конструкции, режима работы (длительные или короткие разряды) и чистоты применяемых материалов, срок службы составляет от 100 до 900 циклов заряда-разряда. Современные (ламельные) промышленные никель-кадмиевые батареи могут служить до 20-25 лет. Никель-кадмиевые аккумуляторы (NiCd) наряду с Никель-Солевыми аккумуляторами могут храниться разряженными, в отличие от никель-металл-гидридных (NiMH) и литий-ионных аккумуляторов (Li-ion), которые нужно хранить заряженными.

Никель-кадмиевый аккумулятор
Фольга (олово, алюминий и др.)
Фольга (польск. folia, устар. folga<нем. Folie<лат. folium — лист) — металлическая «бумага», тонкий (толщиной от 0,001 до 0,5 мм; в большинстве стран — до 0,2 мм) и гибкий металлический лист, например, из алюминия, стали, олова, серебра или золота. Алюминиевая фольга и стальная фольга используется в фармацевтической (блистеры) и пищевой промышленности для упаковки.

Алюминиевая фольга для бытового применения
Банки для консервов (олово, алюминий)
Консервная банка — герметичный контейнер для долгосрочного хранения пищевых продуктов в герметичной среде, выполненный из тонкой лужёной стали (консервной жести). Основное отличие от другой тары для хранения продуктов — невозможность обратной герметизации после вскрытия, так как вскрытие банки подразумевает разрезание металла контейнера.

Луженая консервная банка
В консервных банках может храниться абсолютно различное содержимое, но чаще всего это консервированные продукты. Иногда встречаются консервные банки, выполненные из алюминия и других металлов. Долгосрочное хранение продуктов в консервных банках обеспечивается при соблюдении надлежащих условий хранения.

Консервы в банках
Сусальное золото (золотая фольга)
Золото это самый пластичный металл, из него можно изготовить фольгу толщиной меньше микрометра. Такая фольга называется «сусальное золото» и используется для декоративной отделки различных предметов (рамок картин и т.п.). Поскольку золото — очень мягкий металл, работать с такой фольгой непросто. Если взять её пальцами, она прилипнет к ним и разорвется, поэтому для разглаживания и нанесения фольги на изделие обычно используют мягкую кисточку.

Золотая фольга — сусальное золото
Раньше сусальное золото изготавливали, расплющивая молотками тонкие листы, разделенные специальными прокладками (обычно из кишок крупного рогатого скота). Сейчас, насколько я знаю, применяются прокатные станы. Если взять очень точные весы, такой листочек золота можно даже взвесить и определить его толщину. Сусальное золото можно приобрести или на интернет-аукционах, или в Российской Федерации, в фирмах, продающих товары для художественной отделки. Цена на еВау Inc. обычно составляет около 15-20$ за 100 листов 30х30 мм.

Вес одного листочка сусального золота на точных весах
Цветные металлы сферах электротехники и машиностроения
Электротехника — область техники, связанная с получением, распределением, преобразованием и использованием электрической энергии. А также — c разработкой, эксплуатацией и оптимизацией электронных компонентов, электронных схем и устройств, оборудования и технических систем.

Определение электротехники
Машиностроение — отрасль обрабатывающей промышленности по производству всевозможных машин и оборудования, изготовляющая средства производства.

Определение понятия машиностроение
Электрические провода (алюминий, медь)
Электрический провод (провод) — кабельное изделие, содержащее одну или несколько скрученных проволок или одну или более изолированных жил, поверх которых в зависимости от условий прокладки и эксплуатации может иметься лёгкая неметаллическая оболочка, обмотка и (или) оплётка из волокнистых материалов или проволоки, и не предназначенное, как правило, для прокладки в земле.

Провод с медной жилой
Неодимовые магниты (неодим, никель и др.)
Неодимовый Магнит — постоянный мощный редкоземельный Магнит, состоящий из сплава неодима, бора и железа. Известен своей мощностью притяжения и высокой стойкостью к размагничиванию. Имеет металлический внешний вид, очень востребован и применяется в разных областях промышленности, медицины, в быту и электронике.
alt=»Неодимовый магнит с размерами 50x50x25 мм» width=»480″ height=»360″/> Неодимовый магнит с размерами 50x50x25 мм
Обмотка электродвигателя (медь)
Электрический двигатель — электрическая машина (электромеханический преобразователь), в которой электрическая энергия преобразуется в механическую, побочным эффектом при этом является выделение тепла.

Медная обмотка электродвигателя
Танталовые конденсаторы (тантал)
Около трети всего производимого тантала используется при изготовлении танталовых конденсаторов и других электронных приборов. Танталовые конденсаторы обладают намного большим сроком службы по сравнению с алюминиевыми электролитическими. Цветные цилиндрики на фото – это электроды из конденсаторов ЭТО и К-52. Яркий зеленый и красный цвет поверхности обусловлен присутствием пленки оксида различной толщины и структуры.

Электроды из танталовых конденсаторов
Свинцово-кислотные аккумуляторы (свинец)
Свинцово-кислотный аккумулятор — наиболее распространенный и широко применяемый на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: стартёрные аккумуляторные батареи в транспортных средствах, аварийные источники электроэнергии, резервные источники энергии.

Автомобильный свинцово-кислотный аккумулятор
Горелка для плазменной резки — плазмотрон (гафний, медь)
Сейчас для раскроя листового металла довольно широко используется плалменная резка. Основная суть этого метода состоит в том, что металл нагревается электрической дугой и сгорает или выдувается потоком воздуха из разреза. Пример горелки используемой для плазменной резки показан на первом фото.

Плазменная горелка для раскроя листового металла
Сам плазмотрон состоит из сопла, через которое продувается воздух, электрода на котором зажигается дуга и изолятора.

Плазматрон с гафниевыми вставками в медных электродах
Сами электрода изготовлены из меди, а вот небольшие вставки, которые хорошо видны на третьем фото — гафниевые.

Медные электроды плазматрона с гафниевыми вставками
Нержавеющая сталь (хром, никель и др.)
Нержавеющая сталь — легированная сталь, устойчивая к коррозии в атмосфере и агрессивных средах. Хром, очень широко применяется в промышленности и в быту. Многе сорта нержвеющей стали содержат больше 15% хрома. Им покрывают различные изделия для защиты от коррозии, соединения хрома используют в качестве пигментов.

Трубы из жаростойкой нержавеющей стали
Самарий-кобальтовые магниты (самарий, кобальт, никель и др.)
Самарий-кобальтовые магниты были получены в семидесятых годах, то есть на 10-15 лет раньше, чем система Nd-Fe-B, но сейчас в «народном хозяйстве» они распространены меньше неодимовых. У самариевых магнитов есть свои плюсы и минусы, которые определяют их применение и распространенность. К плюсам можно отнести: высокую рабочую температуру (они работоспособны до 250°C, в то время как неодимовые размагничиваются уже в кипящей воде) и хорошую коррозионную стойкость (Nd-Fe-B надо обязательно покрывать защитными покрытиями из никеля, золота или полимеров, иначе они быстро корродируют).

Магниты самарий-кобальтовые

Осколки самарий-кобальтовых магнитов
Медные шины (медь)
Медная шина востребована в электротехнических целях, среди которых можно отметить изготовление шинопроводов, шинная сборка, производство распределительных устройств. Она применяется практически для всех типов присоединения установок распределения и передачи энергии как высоковольтных, так и низковольтных. Медная шина также используется для соединения главных шин и непосредственно распределительным оборудованием.

Медные шины для электротехнического применения
Припой (олово, кадмий и др.)
Припой — металл или сплав, применяемый при пайке для соединения заготовок и имеющий температуру плавления ниже, чем соединяемые металлы. Применяют сплавы на основе олова, свинца, кадмия, меди, никеля и другие. Срок службы припоя зависит от правильности технологии и окружающей среды в эксплуатации до 20 лет.

Свинцово-оловянный припой
Цветные металлы в военной сфере

Различная военная техника
Инфракрасные сенсоры (мышьяк, галлий и др.)
Соединения мышьяка с некоторыми редкими металлами (например галлием, индием, марганцем) достаточно широко применяются при изготовлении полупроводниковых лазеров, ИК сенсоров, диодов и других устройств.
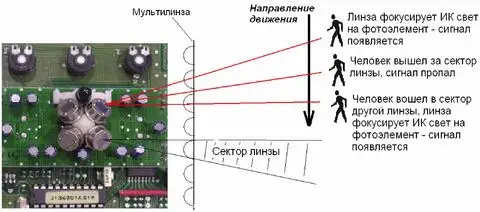
Принцип действия инфракрасных датчиков движения
Для синтеза таких соединений требуются исходные вещества очень высокой чистоты (99.9999% и выше) так как свойства полученных полупроводников очень сильно зависят даже от наличия небольшого количества (тысячные доли процента) примесей.. В ампуле на фотографии, находится мышьяк чистотой 99.99999% (или 7N) фирмы Alfa Aesar используемый при сентезе полупроводниковх соединений. Ампула заполнена аргоном чтобы мышьяк не окислялся на воздухе.

Мышьяк чистотой 99.99999% (или 7N) фирмы Alfa Aesar
Линзы для инфракрасной оптики (германий)
Еще одно свойство Германия – прозрачность для ИК-лучей, поэтому из него делают линзы и другие детали ИК оптики. На фото – германиевая линза. Она не прозрачна для видимого излучения, но в среднем ИК через неё можно смотреть как через стекло.

Линза из цветного металла германия
Полупроводниковый ОЧГ — детектор радиации (германий)
Существуют различные типы детекторов радиации. Поначалу, для оценки мощности излучения использовались фотопластинки (степень засветки пропорциональна количеству поглощенной радиации). Затем электроскопы (чем быстрее электроскоп разряжался, тем сильнее излучение). Потом появились сцинцилляционные датчики и счетчики Гейгера-Мюллера. В отличие от газовых счетчиков, полупроводниковые детекторы имеют гораздо большую эффективность. Одним из детекторов такого типа является детектор из сверхчистого Германия — детектор из особо чистого Германия (ОЧГ-детектор, или HPGe-детектор).

Детектор из особо чистого германия (ОЧГ или HPGe-детектор)
Ионизирующие излучения вызывают в особо чистом Германии образование пар электрон-дырка, а приложенное к кристаллу высокое напряжение позволяет эффективно собирать их на электродах и формировать сигнал на выходе. По сути, кристалл работает как ионизационная камера, только вероятность ионизации в нем намного выше. Чтобы электроны и дырки не поглощались примесями, чистота Германия должна быть очень высокой. Также, кристалл должен быть охлажден до низкой температуры, иначе электроны будут легко пересекать запрещенную зону полупроводника, попадать взону проводимости и очень сильно увеличивать тепловой шум детектора.

Ручной спектрометр NitroSPEC на основе детектора из ОЧГ
Тритиевая подсветка (тритий, цинк и др.)
Тритиевая подсветка (trigalight — тригалайт, GTLS — gaseous tritium light source) — подсветка на принципе радиолюминесценции, вызванной бета-распадом трития. По некоторым оценкам, устройства с тритиевой подсветкой могут содержать порядка 25 милликюри (современные) до 200 милликюри (подсветка для LCD, 1970-е) (0,9-7,4 ГБк). Принцип работы сходен с принципом работы обычного кинескопа. Тритий заключён в небольшую герметичную ёмкость, обычно из боросиликатного стекла, на внутреннюю поверхность которой нанесён тонкий слой люминофора.

Солдат с швейцарскими часами Luminox-a3951Navyseal (с тритиевой подсветкой)
Электроны, испускаемые в данном случае в результате бета-распада трития, возбуждают атомы вещества-люминофора, которые переходят из возбуждённого состояния в обычное, испуская при этом энергию. Кроме того, ввиду малой энергии электронов, толщины люминофора и стенок ёмкости достаточно, чтобы полностью поглотить электроны. Используется в военных и гражданских приборах (подсветка компасов, линзы для чтения карт в темноте), прицельных приспособлениях, часах, брелоках, аварийных надписях типа «выход».

Военный компас Cammenga с тритиевой подсветкой
Пули, дробь, шрапнель (свинец)
Пуля (предположительно от польск. kula — ядро) — снаряд (поражающий элемент) стрелкового оружия. Пулями также называют небольшие снаряды, которые использовались в пращах и старинной механической артиллерии. Две главные особенности пуль — большая дальность стрельбы и высокая поражающая способность — обусловлены одним физическим явлением — инерцией.

Свинцовые пули
Одно из традиционных применений свинца это изготовление всевозможных пуль, дроби, шрапнели и прочих снарядов для огнестрелного оружия. Главным образом этому способствуют дешевизна и низкая температура плавления свинца. Не знаю как сейчас, но раньше при литье дроби в свинец добавляли около одного процента мышьяка, для улучшения литейных свойств. А сейчас, для защиты окружающей среды от загрязнения свинцом, в некоторых странах для изготовления пуль предлагают заменить свинец висмутом.

Свинцовая охотничья дробь
Цветные металлы в сфере исследований

Определение понятия исследования
Платиновый тигель (платина)
В платиновом тигле можно нагревать «кислые» расплавы и растворы. Например серную кислоту, ее кислые соли. А вот в расплавах щелочей и особенно в присутствии окислителей, платина быстро корродирует, поэтому для нагревания гидроксидов щелочных металлов лучше использовать серебряную посуду. Платиновые тигли размером побольше, используют для варки специальных стекол или выращивания монокристаллов полупроводников.

Лабораторный платиновый тигель
Лабораторная термопара (платина, родий)
Еще одно достаточно известное применение платины это материал для термопар. Точнее, она входит в состав платино-родиевого сплава, из которого делают проводники термопары. Вообще, типов термопар существует великое множество. Хромель-алюмелевые, медно-константановые, вольфрам-рениевые, нихром-никелевые и т.д. Но платино-платонородиевые больше всего подходят для использования в лабораторной практике, поскольку позволяют надежно измерять температуру на воздухе до значений в 1600 °C — 1700 °C.

Спай платино-платинородиевой термопары
Газоразрядные лампы (ртуть)
Еще одно применение ртути – газоразрядные лампы. В них ртуть применяется как в чистом виде, так и в виде смесей с газами (в основном, с аргоном), для увеличения светоотдачи. Ртутные лампы используются в качестве источников интенсивного УФ излучения.

Ртутные газоразрядные лампы
Термометры сопротивления (платина)
Для более низких температур (от -200 °C до 600 °C) используют платиновые терморезисторы (термометры сопротивления). Их действие основано на том, что сопротивление металлической платины линейно возрастает с повышением температуры. Зная сопротивление платиновой проволочки при одной температуре и измерив его при другой, неизвестной, можно вычислить температуру по формуле. Для удобства, в качестве терморезисторов берут кусок проволоки, имеющий при 0°C сопротивление, равное 100, 50, 500 или 1000 Ом. Такие термодатчики обозначают соответственно Pt100, Pt50, Pt500 и Pt1000.

Платиновый терморезистор (термометр сопротивления)
Электроды для мощных дуговых ламп (вольфрам)
Еще одно применение вольфрама, это изготовление электродов для мощных дуговых ламп (например таких, как на страничке с ксеноном). Однако, как можно видеть на фото, даже вольфрам не вполне устойчив к воздействию мощной электрической дуги — концы электродов оплавлены.

Вольфрамовые оплавленные электроды (даже вольфрам не всегда выдерживает мощные разряды дуговых ламп)
Цветные металлы в авиакосмической и судостроительной сферах

Сборка пассажирского лайнера Боинг-747 (сборочный цех самолетостроительного завода Сиэтла)
Судостроение или кораблестроение — отрасль тяжёлой промышленности, осуществляющая постройку судов. Корабли или суда обычно строят на специализированных предприятиях, верфях.

Спуск на воду подводной лодки Б-265 Краснодар
Обшивка самолетов (алюминий)

Изготовление алюминиевой обшивки крыла самолета на заводе (Комсомольск-на-Амуре)
Элементы двигателей самолетов (титан, алюминий)

Двигатель SaM146 для самолета Сухой Суперджет 100
Детали подводных лодок (титан)

Многоцелевая атомная подводная лодка проекта «Ясень»
Элементы космических кораблей, станций (титан)

Международная космическая станция (МКС)
Части межконтинентальных ракет (титан)

Межконтинентальная ракета морского базирования Булава
Проблема воровства цветных металлов в России и мире
В 90-х годах на постсоветском пространстве цветные металлы тянули и собирали наверное все кто мог, отчасти время такое было, надо было как-то выживать, отчасти кто-то хорошо на этом наживался в то смутное время. Но проблема воровства цветных металлов в Российской Федерации, странах СНГ никуда не делась и в 21 веке. Да что Россия, в так называемых высокоразвитых зарубежных странах цветной металл на удивление воруют в самых разных масштабах. Ниже приведены различные факты и ситуации с воровством цветных металлов, попавших в СМИ, начиная с Российской Федерации и заканчивая США.

Воровство цветных металлов распространено по всему миру
Гастарбайтеры сняли пять тонн меди c термоядерной установки (Россия)
Двое рабочих, приехавших из Молдавии, сняли пять тонн меди с экспериментальной термоядерной установки Токамак Т-15 в Научно-исследовательском центре «Курчатовский институт». Об этом сообщает «Интерфакс» со ссылкой на источник в правоохранительных органах. По данным источника, в течение десяти дней — с 3 по 13 марта 2015 года — двоим гастарбайтерам удалось снять с установки медные шины и спрятать цветной металл на территории предприятия с целью вынести его позднее.

Экспериментальная термоядерная установка Токамак-Т-15
Однако пропажа была обнаружена и рабочих задержали. По данным проверки, ранее молдаване имели доступ к установке. Предположительно, похитители действовали вместе с соучастниками, личности которых устанавливаются. Возбуждено уголовное дело по статьям 30 УК РФ (приготовление к преступлению) и 158 УК РФ (кража). Установка Токамак Т-15 является одной из крупнейших в мире. Уникальность установке придает наличие самого большого в мире сверхпроводникового ниобий-оловянного тороидального магнита.

Медные шины, вполне возможно для Токамак-Т-15
Хищение около 200 метров железнодорожного кабеля (Россия)
Ранним утром во вторник, 18 августа 2015 года, на участке Москва Пассажирская — Москва Товарная Октябрьской железной дороги было украдено порядка 200 метров кабеля сигнализации, централизации и блокировки. Об этом сообщила пресс-служба дороги. «Это привело к отключению световой сигнализации, управляющей движением поездов», — передает ТАСС слова собеседника.
Наблюдались задержки до одного часа в движении пригородных поездов на участке Москва — Тверь. В настоящее время движение на Ленинградском направлении восстановлено. Работникам ОЖД потребовалось около пяти часов, чтобы ликвидировать последствия хищения электрокабеля, сообщает пресс-служба ОЖД.
В Уручье неизвестные срезали 8 километров интернет-кабеля (Беларусь)
С октября 2014 года в минском Уручье произошло 28 случаев хищения интернет-кабеля, принадлежащего компании МТС, из подъездов. За три месяца украдено 7,8 тыс. метров «витой пары», которая соединяет абонентов через оборудование, установленное в подвалах. Самая крупная кража — 666 метров кабеля — зафиксирована по адресу улица Никифорова, 17.

Обрезанный интернет кабель в Уручье
Злоумышленники выбирают провода, уложенные в короба вдоль стен, перерезают, вытягивают и уносят их с собой. Дома в Уручье строились задолго до того, как появилась необходимость предусматривать большие кабельные каналы, способные вместить в стенах подъездов провода нескольких провайдеров, что и вынуждает прокладывать кабель вдоль стен.

Обрезанные кабеля и поломанное оборудование
Воровство цветных металлов в Великобритании — национальное бедствие? (Англия)
В Великобритании — новое национальное бедствие. Оно рвёт провода, срывает крыши и даже уносит памятники. Остров захлестнуло воровство цветных металлов. Крестьянин из чеховского рассказа воровал гайки на железной дороге. Этих ребят больше интересуют кабели с проводами из цветных металлов. Из-за «подкопов» останавливаются поезда и тысячи людей каждый день не попадают на работу.

Ущерб от кражи металлов в год (Англия)
Воровство цветных металлов в Англии объявили национальным бедствием. Ущерб от него железнодорожные компании оценивают в один млрд. фунтов. Не помогают ни сигнализация, ни камеры наблюдения. Для государства это теперь проблема номер два после терроризма. Охотников за металлом с каждым днём всё больше. А всё из-за массовой безработицы и подскочивших цен на медь. На севере Англии скупщиков утиля обязали переписывать у сдающих паспортные данные. А полиция пугает в интернете отчётами о «металлических» рейдах.

Одни из украденных медных шин, найденные полицейскими (Англия)
«Сегодня довольно удачный день. Мы задержали несколько машин, выяснили, где был украден металл и собираемся вернуть его владельцам», — отмечает инспектор полиции Ковентри Джо Флойд. Бронзовую инсталляцию известного скульптора Барбары Хэпуорт вряд ли уже найдут. «Разделённый круг», он почти полвека украшал парк на юге Лондона, спилили за считанные минуты. Полиция лишь разводит руками.

Бронзовая скульптура Барбары Хепуорт (Разделенный Круг или Две Формы)
«Я не уверен, что рейды эффективны. Надо в целом ужесточать закон. Добросовестные скупщики и так спрашивают документы, а жулики всегда придумают, как обойти закон», — говорит заместитель министра внутренних дел Лорд Хенли. Украденный металл в основном идёт в Китай. Это серьёзный бизнес, хорошие деньги, а деньги порой заставляют людей забыть обо всём святом. В городке Редмаршал разобрали медную крышу церкви XIII века. Последний раз этот храм грабили 300 лет назад.

Все что осталось от скульптуры в лондонском парке Далич
«Люди, укравшие крышу, заработали три-четыреста фунтов, хотя сам металл стоил дороже. Чтобы всё восстановить — включая работу — нам нужно 30 тысяч фунтов», — говорит настоятель церкви Св Катберта пастор Дэвид Брук. Оказавшись без крыши над головой, паства требует, чтобы злоумышленников нашли и упрятали за решётку. Но даже если их поймают, им грозит лишь денежный штраф. И на ремонт храма его явно не хватит.
Хищение медных крыш в Париже и Лондоне (Франция, Англия)
В середине февраля 2013 года в пригороде Парижа злоумышленники украли крышу ресторана. Преступники с инструментами забрались на крышу и разобрали покрывавшие ее медные пластинки, заявили представители французской полиции. Похитители унесли около 60 квадратных метров крыши. Подобные происшествия случаются не только в модной столице мира.

Вот такие медные крыши Парижа, сдуваемые иногда ветром, могут стать объектом кражи
Не так давно в Лондоне пришлось закрыть библиотеку из-за того, что здесь также была похищена медная кровля и крыша стала протекать. Любопытную зависимость между ростом количества краж и динамикой цен на цветные металлы вывело британское издание The Economist. Главный его вывод звучит так. Чем выше цены, тем чаще воруют медь. Этот металл дорожает по вполне объективным причинам. Его использование в промышленности растет, а запасы стремительно тают.

Библиотека Западного Норвуда, здесь воры украли большую часть медной крыши (Англия, Лондон)
Воровство меди с ветряных двигателей (Франция)
Ссылаясь на анонимный источник в полиции, ежедневное издание пишет, что преступники воруют двигатели с крупных ветряных электростанций. Места это, как правило, малонаселённые, поэтому шансы быть пойманными на месте преступления — минимальны. «Сначала они прекращают подачу электроэнергии, чтобы остановить мотор двигателя, — рассказал полицейский. — Преступники взламывают дверь у основания турбины, поднимаются по лестнице к двигателю, расположенному на самом верху, на высоте около 40 метров. Затем, при помощи болторезного станка и других самодельных приспособлений, они режут на части сделанный преимущественно из меди двигатель».

Жандармы проверяют одну из ветровых турбин
По словам полиции, за один такой налёт преступники увозят до тонны добычи. А тонна меди на рынке — это примерно 4,5 тысячи евро. Однако по мнению офицера полиции воры сильно рискуют: выбранная ими схема предполагает, что они по крайней мере несколько минут находятся наверху. Если застать воров в этот момент, им будет абсолютно некуда скрыться — выход только один. Согласно имеющейся у Le Figaro информации, за последнее время было зафиксировано 20 таких эпизодов. Только в марте было совершено два успешных набега и одна сорвавшаяся попытка.

Жандармы задержали машину с тонной меди (Франция)
В ответ на возрастающее число краж, обслуживающие ветряные электростанции операторы установили системы видеонаблюдения, а полиция взяла на себя патрулирование крупных станций при помощи оборудованных камерами вертолётов. «Пока воровство турбин ещё не превратилось в проблему национального масштаба, но всё к тому идёт», — признался один из следователей в интервью французской газете.За 2012 и 2013 годы количество уголовных дел, связанных с воровством цветных металлов, возросло во Франции почти на 18 процентов: с 11 811 до 13 923. Медь составляет 65 процентов всего украденного металла.

Ветровые электростанции (турбины) во Франции
Воровство металла — доходный бизнес? (Германия)
Канализационные люки и решетки от сточных колодцев, водосточные трубы, рельсы, провода и даже скульптуры — воры не гнушаются ничем. Цены на металл, особенно цветной, неуклонно растут, а вместе с ними и прибыль. В городе Дармштадте воры украли водосточный желоб и трубу со здания музея. А заодно прихватили 200 килограммов медного листа, заготовленного для ремонта. Да что музей, в городе Плауэн грабители не пощадили даже церковь: она тоже лишилась медного водосточного желоба. В городке Мёрс охотники за металлом планомерно срывали бронзовые вазы и светильники, на местном кладбище осквернены 180 могил.

Воруя металл воры не гнушаются ничем
В Дюссельдорфе из парка исчезла бронзовая скульптура «Пандора», в Дармштадте — пастушок со свирелью. Полиция исходит из того, что воров привлекла не художественная ценность произведений искусства, а стоимость материала, из которого они изготовлены. За килограмм меди сегодня платят около 5 евро, за килограмм бронзы — около 3.

Статуя Пандора в парке Дюссельдорф до ее похищения
В прошлом году только на железных дорогах в Германии зарегистрировано около 3 тысяч случаев хищения металлов — от рельсов до сигнальных проводов. Совокупный ущерб — 15 миллионов евро, не считая расходов на ремонт и компенсации пассажирам. Еще больше, однако, потери для репутации немецкой железной дороги (Deutsche Bahn).

Найденная и задержанная полицией украденная медь (Kreispolizeibehörde Borken)
Крупнейший немецкий телекоммуникационный Концерн Deutsche Telekom оценивает материальный ущерб от кражи кабеля в 820 тысяч евро в год. Всего в прошлом году было зафиксировано 320 таких случаев. Казалось бы, семечки для мирового концерна с многомиллиардным оборотом. Но представитель Deutsche Telekom Филипп Бланк (Philipp Blank) указывает, что ущерб, причиненный репутации концерна из-за перебоев со связью, на порядок выше.

На этой строительной площадке украли многожильный кабель (Neumark. Oberneumarker Straße)
Ужесточение борьбы с воровством цветных металлов (США)
Сенат Конгресса США намерен внести воровство цветных металлов в список федеральных преступлений, предусматривающих лишение свободы на 10 лет. Как передает ИТАР-ТАСС, речь, в частности, идет о краже меди с вышек телефонной и сотовой связи, а также с других американских объектов жизнеобеспечения.

Рабочие восстанавливают обрезанный медный кабель на железной дороге (Нью Йорк, США, 2015 год)
Автор законопроекта, сенатор-демократ от штата Миннесота Эми Клобучар, отметила, что за последние годы уровень кражи цветных металлов вырос на 80 процентов. «Увеличение случаев кражи металла по всей стране подчеркивает важность действий со стороны федеральных органов», — указала политик. Кража цветных металлов ежегодно обходится американским компаниям в 1 млрд долларов. Чаще всего такие кражи совершают в Род-Айленде, а наименее популярен такой вид «дохода» у жителей Аляски.

Отчаянная надпись от рабочих для воров (нет меди), чтобы не портили зря оборудование (Кеттеринг, США)
Источник https://www.vsgipn.ru/interesnoe/tsvetnye-metally-13-metallov-opisanie-svojstva-gde-primenyayutsya-i-mesta-dobychi.html
Источник https://tdspecstal.ru/articles/tsvetnye-metally.html
Источник https://economic-definition.com/Other_extractive_materials/Cvetnye_metally_Non_ferrous_metal__eto.html