14 различных типов металлов

Термин «металл» происходит от греческого слова «metalléuō», что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы — это элементы с относительно высокой плотностью (обычно более 5 г/см³) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы — это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
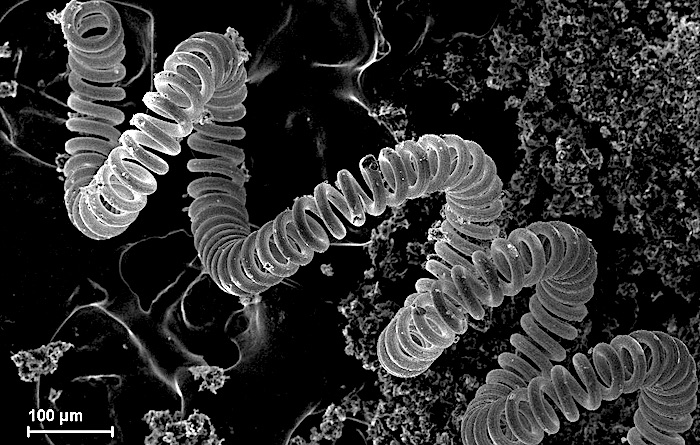
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин «железо» происходит от латинского слова «Ferrum», что переводится как «железо». Таким образом, термин «черный металл» обычно означает «содержащий железо», тогда как «цветной металл» означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы — это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель — для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро — второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие, как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов — использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
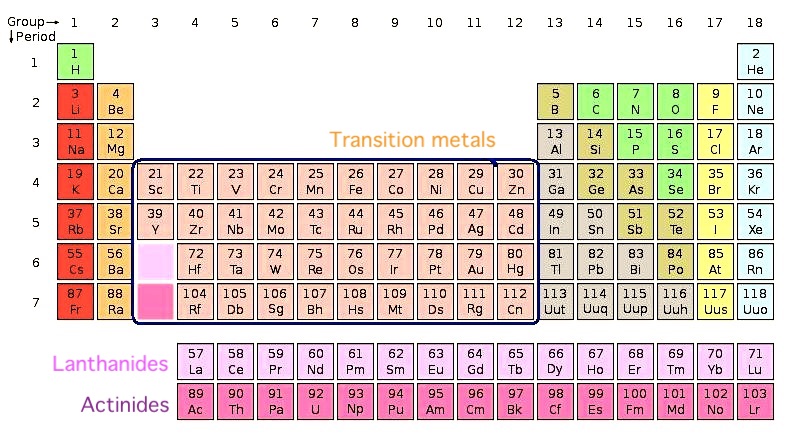
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице — это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются «бедными» или «другими» металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий — в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды — это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды — это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
Откуда у алюминия цвет и блеск

Алюминий обладает рядом уникальных свойств, которые делают металл востребованным в большинстве сфер жизни. Без него не обойтись в промышленном производстве. Ему нашли применение в сельском хозяйстве. Немало его и в повседневном быту, и в коммерции. Цвет и блеск алюминию придает оксидная пленка. Именно из-за нее у этого легкого минерала так много преимуществ перед другими металлами.
Как был открыт алюминий
Алюминий – это легкий металл, относящийся к парамагнетикам. В чистом виде его можно встретить лишь в жерлах вулканов, но в ничтожно малом количестве. А между тем элемент значительно широко распространен в земной коре, но только в виде различных соединений.
И среди металлов он занимает лидирующее положение, поскольку его концентрация приближается к 8 % от общей массы элементов. Больше его на Земле только кислорода и кремния. А если сравнить залежи с золотом, то количество последнего всего пять миллионных долей от одного процента (0,000005 %).
Алюминий можно встретить буквально везде. Есть он в тканях животных и растений. Также подтверждено присутствие и в воде. В ней он в основном находится в виде соединения – фторида алюминия. И если в морской воде его концентрация достигает лишь 0,01 мг/л, то в некоторых пресных водоемах количество доходит даже до 10 мг/л.
Но для серьезной разработки этого недостаточно. Поэтому основная добыча алюминия приходится на получение его из бокситов, алунитов и нефелинов. А также из базальтов, гранита и даже глины. И в основном в них он содержится в виде алюмосиликата. А в России самые богатые залежи находятся в районе Урала и Сибири.
Первые упоминания о применении алюминия пришли к нам из древности. Люди натолкнулись на вещество, которое имело отличные связывающие свойства. Его назвали квасцами и стали использовать при дублении кожи.
Именно латинское название квасцов (alumen) и послужило для обозначения современного алюминия. А в те времена так именовали горькую соль. Ведь состояло вещество из алюмокалия. И впервые разобрать квасцы на составляющие попытался Парацельс в 16 столетии. Он отделил от вещества «квасцовую землю». Так был получен оксид алюминия.
Но названия у элемента в то время не было. А появилось оно только в 18 веке, когда эксперименты Парацельса стал повторять немецкий химик Маргграф. Свойства металла заинтересовали научный мир своей уникальностью. И с этого момента не прекращались попытки получить алюминий в чистом виде.
Кроме немецких ученых в борьбу вступили также английские и датские физики. И среди последних отличился Ганс Эрстед. Лабораторным путем он смог из хлорида алюминия выделить чистый металл. Восстановление проводилось амальгамой калия при нагревании.
Впоследствии немецкий химик Вёлер улучшил способ. А в 1854 году французский ученый Сент-Клер Девиль, заменив калий на более безопасный натрий, смог добиться более стабильных результатов. И уже через два года предоставил ученому сообществу первый алюминиевый слиток, полученный полупромышленным способом.
В те временя электролиз требовал значительных финансовых затрат. Поэтому не удивительно, что алюминий был дороже золота. Последнее все же присутствовало в аналитических весах, которые были подарены Дмитрию Менделееву от имени британского ученого мира. За его выдающиеся заслуги.
Чашки измерительного прибора были сделаны из алюминия, что по тем временам считалось чуть ли непозволительной роскошью. Выполнить прибор полностью из такого дорогого металла не смогли позволить себе даже столь богатые колонизаторы. Поэтому алюминий частично заменили на золото.
С начала двадцатого столетия цены на электроэнергию стабилизировались. Поэтому алюминий начали добывать в промышленных масштабах. Именно этот период ознаменовался открытием большинства инновационных технологий, где начали применять алюминий.
Физические свойства металла
Алюминий обладает высокой электропроводимостью. Если сравнивать его с медью, то по международному стандарту он на целых 40 % хуже последней. Но поскольку удельный вес у алюминия составляет лишь треть от массы отожженной меди, то он способен проводить в два раза большее количество электричества. Поэтому материал повсеместно применяют как в промышленности, так и в быту. И его можно встретить в трансформаторах, линиях электропередач, электрических шинах и даже лампочках (цоколь).
Рассказывая о свойствах алюминия необходимо сделать небольшую сноску. Интересных особенностей у металла много. Но любая из них может увеличиваться или понижаться в зависимости от примесей. А поскольку использование алюминия в чистом виде происходит довольно редко, то способность металла к чему-либо чаще оценивают по добавкам.
Например, прочность у алюминия очень низкая. Но если в его состав внесены легирующие элементы, то она возрастает, можно сказать, в разы. К тому же последняя значительно повышается, если металл подвергнуть специальному упрочнению. К примеру, термическому. Или деформационному.
Самые распространенные легирующие элементы:
- марганец;
- цинк;
- магний;
- медь;
- титан;
- железо;
- кремний.
Возвращаясь к прочности, необходимо сказать о способности алюминия выдерживать серьезные низкие температуры. И не просто сопротивляться морозам, а даже повышать свою крепость, сохраняя высокую вязкость. Сталь на такое не способна. При больших минусовых температурах она становится хрупкой.
Из-за этой особенности алюминий применяют для постройки космических аппаратов. Ведь в безвоздушном пространстве распространен вечный холод. Поэтому космическая станция состоит в основном из алюминия.
Но удельная прочность металла на большой высоте по сравнению с другими. Это обеспечивается очень низкой плотностью. У алюминия она в три раза меньше, чем имеется у стали, а также меди. И благодаря такой особенности появилась возможность для увеличения грузоподъемности транспорта при значительной экономии топлива.
Алюминий также высоко цениться из-за своих антикоррозийных свойств. Ржавчина просто не может даже появиться на поверхности. А все из-за тончайшей, но прочной оксидной пленки. Она сразу же появляется при контакте этого металла с кислородом. Поэтому обработка поверхности анодированием или покраской обычно носит сугубо декоративный характер.
Проводить через себя тепло алюминий может в три раза скорее, чем сталь. Но если в его состав попадает марганец или магний, то теплопроводимость значительно падает. Поэтому, чем чище алюминий, тем он лучше подходит для различных теплообменников. Но и сплавы нашли себе широкое применение. Например, в кухонной посуде.
Блеск алюминия напрямую связан со способностью отлично отражать лучистую энергию. Причем это относится, как к видимому спектру, так и ультрафиолетовому или инфракрасному. Отражения касаются также и тепловых волн, и электромагнитных. И это нашло применение в радио и радарах. Поскольку алюминий является парамагнетиком, то это свойство используют для защиты оборудования от электромагнитного излучения.
Металл способен отбивать более 80 % световых волн. Это начали широко использовать в осветительных приборах. Также рефлекторные способности нашли применение в теплоизоляции. Это отлично отразилось в строительстве. И теперь в тех зданиях, где участвует алюминий, сохраняется прохлада в зной. А все из-за того, что кровля из серебристого металла отражает большую часть солнечных лучей.
Продолжая тему изоляции, следует сказать, что материал хорошо поглощает различные шумы. Также он отлично противостоит огню. Металл и сам совершенно неспособен к горению, так в добавок не создает искр при ударах. Этим также отличается от стали в положительную сторону. Правда нужно заметить, что при продолжительном воздействии жара, алюминий начинает терять свою прочность.
Модуль упругости в три раза ниже, чем у обычной стали. Поэтому там, где нужно смягчить столкновение, устанавливают алюминиевые детали. Они способны частично поглотить энергию удара. Это значительно повышает безопасность транспорта.
Очень ценится материал из-за своей технологичности:
- Его можно выплавить любым из известных методов.
- Прокатать на специальных станках, добиваясь толщины фольги.
- С помощью давления листы можно штамповать или вытягивать.
- Материал можно подвергать любому из методов ковки.
- Из-за высокой пластичности алюминий легко прессуется.
- А тонкие жилы проволоки заплетаются в толстый кабель.
Серебристый металл не меняет своих свойств даже находясь в воде. Хоть в морской, хоть в пресной. Способен сопротивляться действию многих органических кислот. Также не боится азотную кислоту. Последняя не может навредить алюминию даже в концентрированном виде.
Единственным минусом при взаимодействии с любой жидкостью является то, поверхность металла тускнеет. И, чтобы вернуть блеск алюминию, придется очистить его от налета. Это можно сделать, как химическим способом, так и физическим.
Химические свойства металла
В чистом виде алюминий становится активным веществом. И тогда на полную включаются его восстановительные свойства. Если добавить серебристый металл к большинству соединений, то он начинает выделять основное вещество, забирая все примеси на себя.
С алюминием могут вступать в реакцию:
- щелочи;
- кислоты;
- сера;
- галогены;
- оксиды металлов.
Последние сразу очищаются от примесей. Но для этого необходимо лишить алюминий его защитной пленки. И произвести нагрев. Исключением является йод. Это единственный галоген, который вступает в реакцию с алюминием без повышения температуры.
Также алюминию нужно освободиться от оксидной пленки перед взаимодействием с водой. В результате контакта получится гидроксид алюминия, который очень плохо растворяется. А еще отдельно выделяется чистый водород.
Основные области применения
Химические свойства алюминия получили широкий отклик для создания различных инновационных технологий. В основном для получения веществ с новыми способностями. Или для усиления уже применяемых в разных областях жизни.
Поскольку механические свойства чистого металла имеют много слабых сторон, то для использования в промышленности, алюминий легируют. Полученные сплавы в несколько раз по качеству превосходят многие металлы. Потому что они более стойкие к износу и не боятся коррозии. А еще их легче обрабатывать.
Самые знаменитые сплавы, имеющие собственные названия:
- силумин;
- дюралюминий;
- авиаль.
Не меньше востребованы во многих сферах жизни сплавы алюминия с марганцем, медью и магнием. Также для добавок используют титан и железо. Эти элементы повышают прочность у соединения. А также привносят в сплавы различные качества, которые находят для себя применение.
Область использования таких сплавов очень широка и из них делают:
- Конструкции и элементы для строительства.
- Самолеты и космические аппараты.
- Суда для морского и речного флота.
- Реакторы для различных станций.
- Автоматы и танки для оборонной промышленности.
- Насосы и двигатели в авиастроении.
- Проволоку и выпрямители для электроники.
- Рамы и цистерны для ж/д транспорта.
- Радиаторы и бампера для автомобилей.
- Фольгу, зеркала и посуду для бытовых нужд.
Алюминий даже используют для ракетного топлива. Он выступает в роли одного из компонентов горючего. А Российская академия наук разработала на базе пластин из серебристого металла уникальный источник электричества для автомобилей. Пока его применяют для американского гольфкара. Но в перспективе перенести новинку и на городской транспорт.

Алюминий смог на высоком уровне конкурировать с железом и его сплавами. А также понемногу вытесняет из производства более дорогую медь. И пока эти три металла человек в своей деятельности применяет чаще других и по всем отраслям.
Как используют алюминий в строительстве
Для начала немного статистики. Дело в том, что более 25 % всего производимого в мире алюминия используется именно для строительства. Ведь этот легкий металл совершенно нетоксичен и довольно-таки долговечен. Расчетный срок для службы алюминиевой конструкции начинается с 80 лет. Но эксплуатируется он намного дольше.
К тому же его можно использовать, практически, в любых климатических условиях. Диапазон температур, при которых металл не теряет своих свойств, простирается от минус 80 до плюс 300 °C. А теплоизолирующая способность сайдинга позволяет защитить помещение от холода в четыре раза лучше, чем дополнительная кирпичная кладка в один ряд.
Если брать жесткость и несущую способность, то по сравнению со сталью выигрыш будет в 2-3 раза. А если заменять железобетонные конструкции, то в целых семь раз. Поэтому вывод очевиден. С легким материалом работать не только проще, но и выгоднее.
Производство
Алюминий легко обрабатывается. И плоский или цилиндрический слиток без проблем превращается в нужные для строительства элементы. В плиты для подвесных потолков и стеновых панелей. В лестницы и листы для покрытия кровли. И даже в окна и двери.
Для создания любых форм, от самых простых до архитектурно сложных, чаще всего применяют метод экструзии. Он заключается в том, что размягченный металл помещают в специальную матрицу. Затем будущие детали просто выдавливаются через отверстия различных сечений. После такого процесса не требуется дальнейшая доводка. Размеры полученных элементов сохраняют максимальную точность.
Листы, проволоку и ленты получают горячим или холодным давлением. А детали чаще всего не требуют никакой защиты, поскольку алюминий не боится ржавчины. И для придания блеска алюминий полируют.
Но если по технологии в нем много различных примесей, то антикоррозийные свойства могут значительно снизиться. И в этом случае металл дополнительно анодируют. Или просто покрывают различными лакокрасящими составами.
Но анодирование чаще всего и так завершается окрашиванием. После создания на поверхности металла еще одной защитной пленки электрохимическим способом, деталь погружают в подогретую ванну с краской. После этого поверхность приобретает неповторимую привлекательность. И именно за это качество материал так горячо любим многими дизайнерами.
Небоскребы
Без подобных зданий уже не может обойтись ни один мегаполис. И дело не только в нехватке свободной площади для застроек. Применение алюминиевых конструкций позволяет значительно уменьшить выброс углекислоты в атмосферу. Что на сегодняшний день является важнейшей экологической проблемой.
К тому же легкие светопрозрачные фасады здания позволяют существенно экономить на его энергозатратах. Дело в том, что в алюминиевую раму вставляется не обычное стекло, а его аналог с низкой теплопроводностью. Этим одновременно закрываются две проблемы. Большая площадь остекления позволяет меньше использовать искусственное освещение. А благодаря технологии U-Value, стекло летом не пропускает внутрь зной, а зимой не выпускает тепло.
Ярким примером успешного применения алюминиевых фасадов является здание Crystal в Лондоне. В нем разместился Центр устойчивого городского развития. И хотя строение не является небоскребом, в нем отлично проявились все энергосберегающие технологии. Crystal на 46 % меньше использует электричества, чем здания из стали и бетона. К тому же оно на целых 65 % ниже по выработке углекислого газа. Это в сравнении с теми же железобетонными офисными строениями такой же площади.
Учитывая, что планете грозит скорая перенаселенность, алюминий выходит на первое место. Как строительный материал будущего. И то, что он снижает выбросы углекислоты, а также имеет стопроцентную перерабатываемость, играет значительную роль.
Павильоны
Нельзя обходить вниманием строительство помещений с огромной площадью. Такие здания всегда необходимы мегаполисам. Они служат развлекательными центрами, выставочными или торговыми залами. И современная архитектура, используя технологию создания сетчатой оболочки, выстраивает по всему миру павильоны любых форм и размеров.
Метод разработан еще в 1896 году. Его автор русский инженер и архитектор Владимир Шухов. Но для возведения подобной конструкции требуются очень сложные расчеты. А в те далекие времена не каждый за них брался.
Век компьютеризации значительно упростил моделирование. К тому же появились новые строительные материалы. Взять хотя бы тот же алюминий. Поэтому доработанная технология прочна вошла в современную архитектуру. А метод создания сетчатой оболочки стал доминировать при строительстве больших павильонов.
Способ позволяет придавать оболочке любую форму. А материалами может служить, как сталь, так и алюминиевые сплавы. В последнем случае конструкция облегчается почти в три раза. Ведь крышу можно также сделать из легких и прочных сплавов.
В качестве примеров можно привести несколько самых знаменитых павильонов. И у каждого из них есть свои особенности. Развлекательный парк, ну, просто гигантских размеров построила компания «Феррари» в Абу-Даби. Его крыша из алюминия побила все рекорды по площади. Из нее получилось бы более шестнадцати с половиной тысячи автомобилей.
Огромный атриум Riverwalk вблизи Далласа раскинулся на целых 16 000 квадратных метров. Павильон закрыт крышей из алюминия и это позволяет поддерживать внутри собственный микроклимат. А если бы кровля концертного зала «Дзинтари» в прибалтийской Юрмале была бы сделана не из алюминия, то она бы не смогла раздвигаться.
Спортивные сооружения
Алюминий позволил построить буквально все крытые стадионы и бассейны. Тяжелая сталь просто бы не смогла стать основой сетчатой оболочки. До использования алюминия можно было реализовывать только открытые спортивные сооружения.
Ярким примером выступает масштабная конструкция Центра для водных видов спорта в Лондоне. Под крышей нестандартной формы разместились сразу три крупных бассейна. Сама кровля имеет вид морской волны и весит целых три тысячи тонн. Под ней расположилось 17 500 мест для зрителей.
Алюминий стал ключевым материалом при строительстве всех значимых объектов для зимней олимпиады в Сочи. И это только пара примеров. Но на достигнутом никто не останавливается. Ведется поиск новых технологий. И уже в скором времени ученый мир обещает внедрить в производство инновационные панели из алюминия, которые сделают переворот в строительстве высотных зданий.
Алюминий на наших кухнях
Наряду с глобальными новостройками в нашей жизни еще немало мест, где алюминий занимает одну из ведущих ролей. И самую маленькую, но не менее важную площадь занимают наши кухни. Но если внимательно присмотреться, то серебристый металл захватил там, чуть ли не господствующее положение.
В нашем мире всегда полным-полно крайностей. Одни стремятся окружить себя только предметами роскоши. Другие стараются экономить везде, где это только можно. Так и на наших кухнях можно увидеть либо дорогую сталь с позолотой, либо дешевый пластик. И в основном это касается корпусов бытовой техники. Начиная от кофеварки и заканчивая холодильником.
Но в мире еще достаточно и людей, которые придерживаются золотой середины. И как не банально это звучит, они выбирают аппаратуру, заключенную в алюминиевый корпус. Ведь это самое разумное решение, которое может предложить производитель. Оно решает сразу несколько проблем.
В плане надежности и прочности конструкции, алюминий может легко поспорить со сталью. Отсюда и высокая безопасность при эксплуатации, поскольку материал не ржавеет и не горит. А высокая его пластичность позволяет штамповать различные формы, которые легко впишутся в любой дизайн кухни. От современного до ретро или кантри.
Кстати. Очень модный хай-тек вообще невозможен без серебристых сооружений. А все из-за великолепного блеска алюминия. Но бывает, что даже матовая поверхность смотрится намного выигрышнее. Правда, это все дело вкуса.
А на втором месте после техники находится кухонная посуда. Но приоритеты могут быть другими. А чтобы развеять возражения скептиков, следует указать на один факт. Современная посуда из алюминия, это далеко не то, к чему привык бывший советский обыватель. Времена, когда на кухнях ели из матовых алюминиевых мисок, ковыряясь в них серыми (а не серебристыми) ложками или вилками, давно прошли.
Производство современной посуды
Прежде всего следует сказать, чем мы пользуемся на кухне:
- Кастрюлями и сковородками.
- Котлами и казанами.
- Дуршлагами и утятницами.
- Мисками и кружками.
- Вилками и ложками.
И вот все это изобилие может быть сделано из алюминия. Но кто-то может сказать, что стальная продукция красивее смотрится. Во-первых, это спорное мнение. Во-вторых, дело вкуса. Для кого-то изящнее глиняная посуда. А кому-то по душе деревянная.
А в-третьих, всегда есть практическая сторона. И эта часть спора говорит, что алюминиевая посуда просто выгоднее. Она отлично проводит тепло и поэтому пища быстрее готовится. В ней ничего не пригорает. Только из-за этих показателей многие хозяйки выбирают лишь ее.
А производитель идет навстречу пожеланиям и вовсю расширяет ассортимент. Ведь материал недорогой и очень распространенный. К тому же обладает кучей различных свойств, облегчающих производство. И на выходе получается продукт с очень приемлемой ценой, доступной для любых слоев населения.
Изготавливают алюминиевую посуду двумя способами. Причем один из них все же требует больше вложений. Но товар получается более качественный. И от приобретения такой кухонной утвари не отказывается даже обеспеченная прослойка.

Штампованная посуда
Сразу следует оговориться, что это самый бюджетный способ. И в нем множество недостатков. Стоимость такой продукции настолько мала, что многие не обращают на минусы внимание. Подходит людям с крайностью в экономии.
Для изготовления предмета берут тонкий лист пищевого алюминия и прогоняют его через пресс. Поскольку дело поставлено на поток, то форма у кастрюль и мисок самая незамысловатая. А выдавливание и вытягивания материала при прессовке приводит к нарушению структуры.
Стенки у такой кастрюли тонкие. Не толще получается и дно. Поэтому в будущем возможны деформации от высоких температур и даже незначительных ударов. Бывает достаточно уронить предмет на пол, чтобы он получил вмятину. Правда таким грешит только продукция китайского производства.
Но можно и найти ряд преимуществ:
- Очень низкая цена.
- Позволит быстро разогреть пищу из-за тонких стенок.
- Легкая и поэтому удобная в использовании.
Некоторые производители пытаются немного выровнять недостатки. Например, вставляют при штамповке дополнительное дно. Специальный диск препятствует деформации. А также утолщает дно, что способствует более длительному сохранению тепла.
Еще наносят антипригарное покрытие. Правда выполняется это в процессе работы с заготовкой. Поэтому при штамповке оно также подвергается деформации. И часто качество покрытия снижается.
Самая дешевая посуда имеет толщину стенок всего в 1,5 мм. Многие брендовые производители применяют инновационную технологию по утолщению стенок. После специальной обработки можно получить посуду с толщиной перегородки в 3 мм. Такая продукция и тепло распределяет более равномерно, и служит дольше. Но это также отражается в поднятой на нее цене.
Литая посуда
Для ее производства всегда берется алюминий самого высокого качества. Расплавленный материал заливается в специальную матрицу. В ней и происходит застывание. В итоге получается крепкий предмет с толстыми стенками и дном.
Поскольку механические воздействия в технологии отсутствуют, то структура металла сохраняет свою целостность. Изделие не боится высоких температур. А также падений с любой высоты. Посуда способна долго хранить тепло. А после приготовления пища в ней еще некоторое время томится и это улучшает ее вкусовые качества.
Технология изготовления кастрюли проста:
- В литейную форму заливается алюминий, а его застывание заканчивается через три минуты.
- Матрица переворачивается, и изделие выпадает из нее.
- Заготовка перемещается под пресс, где отсекается все лишнее.
- На завершающем этапе 6 форсунок одновременно наносят на внутренние стенки оксид алюминия белого цвета.
Последняя операция позволяет антипригарному покрытию более плотно соединиться с поверхностью. И наносится последнее в самом конце. Поэтому его качество остается без изменений. То есть, на самом высоком уровне.
Следует отметить высокое качество изготовления литых сковородок по современным технологиям. Пища в них готовится быстро, без пригорания. А ухаживать за таким предметом очень легко. Блеск алюминия восстанавливается очень быстро. Достаточно протереть поверхность мягкой фланелью.
Вред от принятия пищи из алюминиевой посуды
Отсекая огромный ворох страшилок об опасностях, связанных с алюминием, следует обратить внимание на официальное заявление Всемирной организации здоровья. Еще в 1998 году было сказано, чтобы нанести вред организму человека алюминием, его нужно принять внутрь более 50 мг одномоментно.
Для простого примера можно сказать, что даже кислые щи, простояв в алюминиевой кастрюле целую неделю, вбирают в себя не более 3 мг вещества. А поскольку вся окружающая человека среда имеет в своем составе алюминий, то он поступает в организм постоянно. Мало того. Он еще и вырабатывается организмом.
Но даже усиленный прием лекарств (содержащих алюминий) не может быть опасен. Если собрать все факторы воедино, то суточная норма вещества никогда не может быть превышена при естественном порядке. Для того, чтобы получить отравление алюминием вместе с пищей, в нее необходимо только добавить его в большом количестве намеренно.
В течение 20 лет с момента первого заявления, ВОЗ неоднократно выступала с различными докладами, пресекающими различные мифы. Одним из них выступает связь болезни Альцгеймера с принятием пищи из алюминиевой посуды. Медицинские исследования это не подтвердили.

Также оказались ложными и страхи, что алюминий является канцерогенным. Связь с раковыми болезнями никак не подтвердилась. И на сегодняшний момент алюминий считается не опасным для человека. Но даже если у кого-то остаются сомнения, то стоит вспомнить о защитных пленках, которыми покрывается посуда. Они вообще препятствуют контакту пищи с алюминием.
Вот нарушения защитного покрытия следует избегать тем, кто не может избавиться от страхов о токсичности алюминия. Чтобы сохранить свой покой, достаточно соблюдать несколько правил. Поскольку на оксидную пленку негативно действует кислота, то следует контролировать ее появление.
Например, не проводить сбор ягод в алюминиевую посуду. В их соке содержится кислота, которая разъест защитное покрытие. А по мере возрастания массы собранных ягод, давление заставит нижний слой выделить сок. И этого никак не избежать.
Если в алюминиевой кастрюле варились кислые щи, то по завершении процесса их лучше перелить в другую емкость. А посуду тщательно вымыть. Негативное действие на защитную пленку также оказывают соли и щелочи. Поэтому хранить продукты с большим содержанием данных элементов в алюминиевой таре нежелательно.
Уход за алюминиевой посудой
Начать нужно с универсального совета. Посуду лучше мыть сразу после использования. Во-первых, это значительно легче. Во-вторых, так можно продлить срок службы у предмета. Единственная оговорка – необходимо дать время посуде на остывание. Ведь попадание даже капли холодной воды на раскаленный металл способно привести к его деформации.
Удаление жира и гари
Блеск у алюминия возвращается даже после удаления многолетней гари:
- Понадобится большая емкость из металла, чтобы в ней полностью утопилась испорченная сковорода или кастрюля.
- Тара заполняется водой.
- Кусок хозяйственного мыла измельчается на терке.
- Порошок добавляется в воду.
- Туда же вливается 300 грамм силикатного клея.
- Раствор доводится до кипения, и в него погружается грязная посуда.
- Необходимо продержать ее на медленном огне не меньше одного часа.
- После этого с предосторожностями ее достают из кипятка.
- Мягкая фланель легко и быстро убирает размягченную гарь.
После завершения чистящей операции следует тщательно прополоскать изделие. Таким же способом удаляется и накипь с поверхности. Но можно попробовать приготовить раствор из нашатырного спирта (10 капель на литр) и мыла. Технология очистки такая же.
Возвращение блеска
Сделать алюминиевые предметы, как новыми, помогут следующие действия:
- Внутрь посуды нужно залить кислое молоко и оставить на 40 минут.
- Натереть стенки половинкой кислого яблока или лимона. Оставить посуду на пару часов.
- Замочить предмет в пищевом уксусе на несколько часов.
- Прокипятить 10 минут в посуде порезанную луковицу.
- Натереть мокрую поверхность зубным порошком и оставить на всю ночь.
После выполнения любой из операций всегда необходимо заканчивать тщательным полосканием в теплой воде.
Борьба с чернотой
Вернуть блеск алюминию после его закопчения на костре может винный уксус или лимонная кислота:
- Салфетка смачивается данными растворами. Затем ей протираются стенки.
- Внутрь посуды наливается вода. В нее добавляется или уксус, или кислота.
- Жидкость доводится до кипения. Огонь убавляется до минимума и выжидается не более 15 минут.
- После остывания, раствор сливается.
- Стенки проходят мягкой губкой с теплой водой.
Обычно в походе для чистки используют песок для очистки котелка от копоти костра. Не нужно этого делать. Причины будут указаны ниже. Лучше принести закопченную посуду домой и воспользоваться вышеуказанным рецептом.
Предостережения
Все жесткие виды чистящих средств под строгим запретом. Даже если не прикладывать значительных усилий, поверхность все равно поцарапается. Нарушение защитной пленки приведет к тому, что алюминий будет контактировать с пищей.
Вторая причина исключения жестких средств для чистки заключается в том, что сталь способна оставлять глубокие борозды. Они со временем забиваются грязью. Удалить ее из глубокой царапины не представляется возможным. По этой же причине лучше не использовать песок или любые абразивы.
Еще под запретом сода. Хоть она и считается универсальным чистящим средством, но для алюминия категорически не подходит. Ведь в ней находятся щелочи, а они будут губительны для наружного защитного слоя.
Нельзя мыть предметы в посудомоечной машине. Во-первых, из-за этого блеск алюминий потеряет. Во-вторых, моющие средства для этих агрегатов все без исключения содержат щелочь. Производители даже специально увеличивают их количество для увеличения качества мытья. Посуда будет безнадежно испорчена.
Заключение
Алюминий медленно, но уверенно вытесняет многие металлы из различных сфер жизни. Замена стали в промышленности или строительстве на серебристый металл во многих случаях приносит чистый выигрыш. И между тем трудно переценить влияние алюминия на быт человека. Окна и двери, крыши и сайдинг, бытовая аппаратура и посуда. Трудно перечислить все области и предметы из алюминия, которые облегчают человеку жизнь и привносят в нее комфорт.
Алюминий — химические и физические свойства, особенности взаимодействия с веществами

Свое название серебристо-белый металл получил от латинского языка, в переводе оно означает квасцы. В 1825 году датский физик Ганс Эрстед нагрел амальгаму калия, восстановил хлорид вещества и выделил новый металл. Затем этот эксперимент повторил и улучшил Фридрих Велер. Он применил чистый металлический калий и первый описал химические особенности алюминия.

Полупромышленный способ выделения открыл Сент-Клер Девиль в 1854 году, но он использовал безопасный натрий. Полученный алюминиевый слиток ученый представил на Парижской выставке. А затем он провел еще один эксперимент — электролиз расплава двойной соли хлорида вещества.
До развития технологий алюминий, созданный электролитическим способом из глинозема, был слишком дорогим. Его слиток стоил больше, чем аналогичный кусок золота. Именно поэтому в 1889 году британские ученые подарили Менделееву аналитические весы. Чаши в них были изготовлены из разных металлов — золота и алюминия. В то время в России последнее вещество называли серебром из глины.
Только в 1886 году отдельно друг от друга химики Эру и Холл разработали промышленный метод добычи металла. Но еще с глубокой древности использовались квасцы — двойная соль калия и алюминия.
Распространенность в природе
По степени распространенности в земле алюминий занимает лидирующую позицию среди всех металлов и третью между элементами периодической таблицы. По исследованиям разных ученых его концентрация в почве колеблется от 7,4 до 8,1%. Молярная масса атома — 26,9815386 г/моль. У вещества высокая химическая активность, поэтому чаще всего оно встречается в виде соединений.
К природным минералам алюминия относятся:

- хризоберилл или александрит;
- бокситы;
- берилл, аквамарин, изумруд;
- нефелины;
- каолинит;
- алуниты;
- полевые шпаты;
- глиноземы — смесь каолинов с песком, магнезитом или известняком.
Но в специфических условиях — жерлах вулканов, например, есть незначительное количество самородного металла белого цвета. Содержат его и природные воды, но вещество приобретает вид малотоксичных соединений. Тип аниона или катиона зависит только от кислотности окружающей среды.
В составе алюминия есть радиоактивные изотопы, которые распадаются за 720 000 лет. Образуются они при расщеплении высокоэнергичными космическими лучами ядер аргона.
Способы получения
У алюминия очень прочная химическая связь с кислородом. Из-за высокой реакционной способности восстановиться металлу из алюмосиликатов и природных оксидов сложнее, чем другим подобным веществам. На это также влияет температура плавления его руд — корунды и бокситы.

Невозможно восстановить элемент путем обжига оксида с углеродом, что помогает при работе с железом. У алюминия слишком близкое взаимодействие с кислородом, у углерода этот показатель гораздо ниже. Получение металла возможно методом неполного восстановления, в ходе которого выделяется промежуточный продукт — карбид алюминия. Затем он разлагается при температуре 1900−2000 градусов, образуя природное вещество.
Этот способ считается более выгодным, чем привычный электролитический, найденный Эру и Холлом. Он требует гораздо меньше энергетических затрат и приводит к минимальному образованию углерода.
Для производства 1 т чернового алюминия необходимо 35 кг его фторида, 65 кг криолита, 600 кг графитовых анодных электродов, 1920 кг глинозема и 61 ГДж электрической энергии. Получить металл в лабораторных условиях можно с помощью метода, найденного Фридрихом Велером. Необходимо восстановить вещество калием его безводного хлорида. Реакция протекает без участия кислорода при нагревании.
Химические свойства
Алюминий — серебристо-белый легкий металл, технический состав плавится при температуре 658 градусов, чистый — при 660, а закипает он при 2518, 8. К физическим свойствам относится и пластичность. Она у вещества очень высокая: 35% и 50% у промышленного и природного сплава соответственно. Его можно раскатать до состояния фольги или тонкого листа.

Модуль Юнга у алюминия составляет 70 ГПа, коэффициент Пуассона — 0,34. Он отлично отражает свет, проводит тепло и электричество. Вещество может взаимодействовать практически со всеми металлами, образует сплавы с кремнием, магнием, медью.
В нормальных условиях алюминий покрыт прочной тонкой оксидной пленкой, поэтому на него не действуют обычные окислители. Но он реагирует на разбавленные серные растворы.
Металлу не опасна коррозия, благодаря чему он нашел широкое применение в промышленности.
Но если пленка разрушилась — ее могут повредить соли аммония, горячие щелочи или амальгамирование, то вещество превращается в восстановитель. Галий, олово и индий не дают ей образоваться, при этом поверхность металла нужно покрыть легкоплавкими эвтектиками.
Перечень того, с чем реагирует алюминий:
- кислородом;
- галогенами;
- неметаллами;
- водой и ее парами;
- щелочами;
- соляной, азотной и серной кислотами.

При реакции с кислородом образуется оксид алюминия, его формула — 4Al + 3O2 = 2Al2O3. Фторид вещества: 2Al + 3F2 = 2AlF3. Сульфид образуется при взаимодействии с серой:2Al + 3S = Al2S3, 2Al + N2 = 2AlN — это нитрид металла, 4Al + 3C = Al4C3 — карбид после реакции с углеродом.
Характерная степень окисления алюминия — плюс три, но его атомы могут образовывать дополнительные связи. При взаимодействии со щелочами образуется тетрагидроксоалюминат (или другие алюминаты): 2Al + 2NaOH + 6H2O = 2Na (Al (OH)4) + 3H2. Металл можно растворить в разбавленной серной кислоте: 2Al + 3H2SO4 = Al2 (SO 4)3 + 3H2.
Интересна реакция алюминия с водой. Для нее необходимо удалить защитную пленку с помощью раствора горячей щелочи или амальгамы: 2Al + 6H2O = 2Al (OH3) + 3H2. При взаимодействии с окислителями происходит разложение вещества: 2Al + 6H2SO4 = Al2 (SO4)3 + 3SO2 + 6H2O — растворимые соли, уравнение реакций. Химические свойства алюминия включают восстановление металлов из оксидов, реакцию с парами воды.
Производство алюминия
До начала позапрошлого века не было достоверной информации о производстве металла. Первые несколько миллиграммов получил Ганс Эрстед в 1825. Через два года Фридрих Велер выделил крупинки, но они моментально покрывались пленкой на воздухе.

До конца XIX столетия вещество не производили в промышленных масштабах. И только в 1854 при финансировании Наполеона III, который надеялся об усилении армии с помощью металла, Сент-Клер Девиль вытеснил алюминий натрием из двойного хлорида натрия. Через год он получил первый слиток массой 6 кг, а до 1890 ученый смог создать более 200 т вещества.
В 1885 году построили первый завод в Гмелингеме, Германия. Технологию для производства разработал Николай Бекетов. Его метод мало отличался от способа Сент-Клер Девиля, но основывался на взаимодействии магния и криолита. За пять лет работы завод создал более 58 т металла, что составило четверть мирового производства.
Эру и Холл практически одновременно изобрели еще один метод — электролиз глинозема. Его растворяли в расплавленном криолите. Он и стал основой современного создания алюминия. В России первый завод появился в 1932 году, тогда промышленность СССР порадовала 47,7 млн т металла. Стимулировала производство Вторая мировая война.
А к 2016 в мире сделали около 59 млн т, лидерами стали:
- Китай;
- РФ;
- Канада;
- США;
- Австралия.
Монополистом в РФ является «Российский алюминий», компания создает более 13% мирового рынка металла. Цены варьируются от 1253 до 3291 долларов за одну тонну.
Сферы применения
Благодаря основным свойствам алюминия — стойкости к коррозии, легкости, плавкости, теплопроводности и нетоксичности соединений — его применяют как конструкционное вещество.
А также металл используется во многих сферах человеческой деятельности:

- черная металлургия;
- создание сплавов;
- ювелирное дело;
- стекловарение;
- пищевая и военная промышленность;
- ракетная техника.
В черной металлургии алюминий необходим для создания стали. Он избавляет ее от пористости, делает более плотной. Сплавы металла широко применяют в разной промышленности. Наиболее востребованы соединения с магнием, марганцем, медью, кремнием. Когда алюминий был дорогим, из него делали ювелирные украшения. Обычно это были пуговицы, чаши для весов. Но когда изменились способы его изготовления, использование в этой сфере сразу прекратилось. Хотя сейчас из него делают бижутерию, а в Японии заменяют серебро.
Наполеон Третий приказывал изготавливать себе столовые приборы из белого металла. Их использовал только он и почетные гости, хотя другие предпочитали золото и серебро. Сейчас подобные изделия можно увидеть в столовых, а также в армии — из алюминия делают котелки, ложки и фляжки.
Фосфат, фторид и оксид вещества необходимы в стекловарении, а также металл зарегистрирован как пищевая добавка. Алюмогель — осадок быстрого охлаждения гидроксида алюминия.
Он выступает в качестве основы обезболивающих и обволакивающих средств. Используют металл и в военном деле: его легкость полезна при создании ручного стрелкового оружия. Соединения вещества — суспензии и порошки — применяют при строительстве ракетной техники.
Роль в биологии
Хотя алюминий распространен в природе, ни один живой организм не использует его в метаболизме. Из-за этого металл называют мертвым, только химия способна превратить его в полезные вещества. У него слабое токсичное действие, но некоторые неорганические соединения сохраняются в растворах, поэтому могут оказывать негативный эффект на организм человека и теплокровных животных.

Самыми опасными считаются сульфаты, хлориды, ацетаты и нитраты. Сначала они действуют на центральную нервную систему, приводят к серьезным расстройствам здоровья. По 15 мг металла может каждый день выходить с мочой, но для людей с нарушенной работой почек даже малейшая доза может оказаться смертельно опасной. Вещество способно накапливаться в тканях головного мозга, костей, печени.
Согласно некоторым медицинским характеристикам, алюминий вызывает болезнь Альцгеймера, рак молочных желез. Но не все исследования подтверждены официально.
Ведь в организм человека молекулы металла попадают с питьевой водой практически каждый день.
Источник https://new-science.ru/14-razlichnyh-tipov-metallov/
Источник https://m-strana.ru/articles/tsvet-i-blesk-alyuminiya/
Источник https://nauka.club/khimiya/khimicheskie-svoystva-alyuminiya.html