Мягкие металлы список
О том, какой металл самый мягкий, можно рассуждать довольно долго, если учитывать различные параметры. К примеру, многим известно, что золото в чистом виде является очень мягким металлом. Его очень просто поцарапать ногтем или сделать из нескольких грамм данного металла тончайшую проволоку.

Благодаря необычайной мягкости золота можно изготавливать из него любой формы драгоценные изделия, чем и пользуются ювелиры. Однако золото – это не самый мягкий металл. Зато таким с уверенностью можно назвать галлий.
Галлий: характеристики
Данный элемент представляет собой довольно пластичный металл, который отличается серебристым цветом и имеет синеватый оттенок. Расположен самый мягкий металл в мире в таблице Менделеева под номером 31. В природе этот металл не встречается в чистом виде, а извлекают его из цинковой руды или бокситов, которые содержат галлий в огромных количествах.

Однако вряд ли можно считать галлий самым мягким, если он оказывается под воздействием низких температурных режимов. В этом случае он является очень даже твердым. Но стоит лишь температуре воздуха подняться до отметки в плюс 29,8 градусов, как галлий начинает плавиться. Чтобы расплавить такой металл, можно лишь положить его в руку.

А уж если ложка, изготовленная из галлия, окажется в горячем чае, то процесс плавления пойдет еще быстрее. При температуре плюс 500 градусов данный металл и вовсе становится настолько «агрессивным», что способен разъедать множество металлов (исключением будет вольфрам). Например, если разогретая до такой температуры капля галлия окажется на банке из алюминия, то примерно через тридцать минут структура банки слабеет, и она раскрошится, словно тонкий лед от механического воздействия.

Есть возможность даже наблюдать, как галлий напоминает сердце, которое бьется, – выполняется эксперимент, когда представитель наиболее мягких элементов начинает совершать активные движения и даже напоминает при этом совершенно неизведанную форму жизни. А происходит это так – расплавленный галлий в виде одной капли соприкасается с кончиком гвоздя. При этом капля сначала продолжает плавиться, а затем, когда контакт заканчивается, снова собирается. В результате получается довольно эффектное зрелище, за которым хочется наблюдать и наблюдать.
Назначение мягкого металла

Особой роли с биологической точки зрения у данного металла не имеется. Но с того самого момента, когда он впервые был обнаружен (в 1875г.), галлий используется в микроэлектронике. Широко его используют также в фармацевтическом производстве. В наше время для создания микроволновых схем и инфракрасных приложений используют арсенид галлия.
Кроме того, что данный металл признан наиболее мягким, он является еще и дорогостоящим. К примеру, в 2005 году за 1000 килограммов данного металла покупателям приходилось выкладывать чуть больше одного миллиона долларов.
Другие мягкие металлы
Возможно, что некоторым приходит на ум противопоставить галлию ртуть, ведь она изначально является жидким металлом, а значит, тоже имеет право называться самой мягкой. Однако есть и еще несколько элементов из таблицы Менделеева, которые тоже могут считаться одними из самых мягких. Этот цезий, калий и рубидий.

Наиболее мягким элементом при комнатной температуре считается цезий. Он является щелочным металлом, имеющим серебристо-желтый цвет. В переводе с латинского «цезий» означает «небесно-голубой». А все потому, что цезий имеет две ярко-синие линии в эмиссионном спектре.
Встречающийся лишь в соединениях с другими элементами калий является щелочным металлом, обладающим серебристо-белым цветом. Он способен мгновенно окисляться на воздухе и оперативно вступать с водой в химическую реакцию, при которой получается щелочь.
И еще одним из наиболее мягких можно назвать рубидий, который тоже является щелочным металлом. Данный элемент представляет собой простой металл, обладающий серебристо-белым цветом.
Самый крепкие и мягкие металлы
Практическое применение металлов играет большую роль в жизни людей: от железобетонных конструкций домов до медицинских протезов и строительства космических ракет − везде участвуют различные виды соединений. Рассмотрим как наиболее твердые, так и самые мягкие из них.
Самые крепкие металлы
В качестве вспомогательной оценки твердости металлов в списке будут приведены данные по десятибалльной шкале Мооса. Она строится по принципу крепости того или иного вещества посредством легкости его разрушения относительно принятых за эталон 10 минералов.
Титан

Свое название титан получил в честь персонажа древнегреческой мифологии благодаря немецкому химику Мартину Клапроту. Механическая прочность этого металла превышает крепость алюминия в 4 раза, железа − в 2. Он также обладает устойчивостью к коррозиям и легкостью, ввиду чего используется для изготовления бронежилетов в военной промышленности, брони в авиации, протезов в медицине, его широко применяют в ювелирном деле. Твердость по шкале Мооса − 6.0.

Свое название уран так же, как и титан, получил от химика Мартина Клапорта. Однако, в этот раз ученый решил назвать новый открытый элемент в честь самой далекой из известных на 1789 год планет.
Тяжелый металл, в чистом виде немного легче стали. Уран радиоактивен и представляет серьезную опасность для человека. Его количество в земной коре в 1000 раз превышает концентрацию золота и в 30 − серебра. Изотоп урана-235 используется в ядерной энергетике ввиду того, что этот элемент наделен большим содержанием потенциальной энергии. Твердость по шкале Мооса − 6.0.
Вольфрам

Вольфрам относится к тяжелым и прочным металлам, обладает устойчивостью к коррозии, очень слабо взаимодействует с крайне опасными в мире химии веществами, уничтожающими многое. Вступает в реакцию с концентрированной соляной и разбавленной серной кислотами.
Благодаря своей прочности и тугоплавкости металл используется для изготовления нитей накаливания в осветительных приборах. Также ввиду высокой плотности вольфрам пригоден для защиты от ионизирующего излучения. Твердость по шкале Мооса − 9.0.
Рений

Свое название рений получил в честь реки Рейн, проистекающей в Германии. Металл один из наиболее редких на планете по содержанию в земной коре. Самое большое месторождение элемента находится в России: по предварительной оценке запасы на Курильских островах составляют 10-15 т этого вещества.
Рений − жесткий металл, обладает хорошей прочностью и высокой плотностью. Элемент еще более устойчив к окислению, чем вольфрам, он почти не растворяется в соляной и серной кислотах даже при нагревании. Ввиду своей редкости обладает высокой стоимостью, поэтому его физические и химические свойства используются в малом количестве областей и там, где он необходим. Рений применяют в изготовлении реактивных двигателей, в целом он незаменим в военной промышленности. Твердость по шкале Мооса − 7.0.
Бериллий

Бериллий − один из самых твердых металлов на Земле.
Свое название получил от древнегреческого слова «глиций», которое означает «сладкий». Дело в том, что растворимые в воде соединения этого металла имеют сладковатый вкус.
Бериллий используют для получения более крепких сплавов: добавление элемента повышает их твердость, прочность и устойчивость к коррозиям. Также металл обладает свойством слабого поглощения рентгеновского излучения, благодаря чему из него изготавливают детали различных аппаратов. Бериллий используется и в атомных реакторах − из него делают отражатели нейтронов. Твердость по шкале Мооса − 5.5.

Хром получил свое название от греческого слова «χρῶμα» и означает «цвет». Название дано металлу благодаря тому, что его соединения имеют различную окраску. Большое содержание этого элемента в земной коре отмечается в ЮАР − 1 место в мире, Казахстане − 2 место, а также еще 8 странах, расположенных преимущественно в Азии и Африке.
Самая крепкая сталь, как правило, получается при добавлении в нее хрома. Этот металл используется в качестве покрытий, повышающих износостойкость того, на что он нанесен. Применение вещества встречается в аэрокосмической промышленности: хром незаменим в изготовлении сопел плазмотронов. Твердость по шкале Мооса − 8.5.
Хром является биогенным элементом и входит в состав тканей всех растений и животных. У последних он участвует в регуляции липидного, белкового и углеводного обменов, недостаток металла в организме способен привести к повышению холестерина в крови.
Тантал

Свое название тантал получил в честь героя древнегреческой мифологии, когда все первые попытки химиков выделить металл в чистом виде при его открытии в 1802 году не увенчались успехом. Элемент относится к редким, его содержание в земной коре не превышает 0,0002%.
Месторождения тантала находятся в 12 странах мира, расположенных в Австралии, Азии, Африке,Северной Америке и Европе.
Тантал обладает удивительными физическими характеристиками: несмотря на свою прочность, он гибкий, как золото.
Химические свойства металла так же поражают: его устойчивость к реагентам схожа со стеклом. Элемент используется в атомной промышленности, авиакосмической технике, медицине и даже ювелирном деле. Твердость по шкале Мооса − 6.5.
Иридий

Самый твердый металл на сегодня, его тугоплавкость и устойчивость к кислотам пока не сыскали равных. Иридий обладает устойчивостью к коррозиям, в природе он практически не встречается, поэтому высокое нахождение металла в земных породах свидетельствует о метеоритном происхождении месторождений. Элемент является еще более редким, чем золото и платина. В число стран, где в природе встречается содержание этого металла, входят ЮАР, Канада, Россия, США, Новая Гвинея.
Высокая твердость и тугоплавкость иридия делают его тяжело поддающимся обработке. Металл не вступает в химическую реакцию ни с одной из известных человечеству кислот. Один из изомеров иридия используется в атомной энергетике, сам элемент нашел применение в машиностроении, авиации, производстве космических аппаратов, ювелирном деле. Твердость по шкале Мооса − 6.5.
Самый мягкий металл
Самый мягкий элемент во Вселенной − ртуть. Элемент является единственным, находящимся в жидком состоянии при нормальных условиях: тех, в которых привычно и комфортно существовать людям. Вещество ядовито − пары ртути, попавшие в организм человека, способны привести к тяжелому отравлению. Элемент редко встречается в земной коре, его месторождения находятся в 8 странах мира, расположенных на Кавказе, в Европе и Азии.
Ртуть известна человечеству с незапамятных времен: до открытия своих ядовитых качеств она применялась в медицине в составе антисептиков, мочегонных и слабительных. На сегодня этот металл используется для изготовления термометров, люминесцентных ламп, датчиков положения, детекторов радиационного излучения.
Твердость по шкале Мооса у ртути не может быть измерена ввиду ее чрезвычайной мягкости.

Определить крепость и твердость металла непросто: всегда важно учитывать все критерии оценки, благодаря которым прочность элементов будет различаться в зависимости от выбранного признака.
Видео в тему
Какие бывают виды и типы металлов и их сплавов
 В строительстве, промышленности и других сферах жизни человека часто используются различные виды металлов. Они отличаются между собой свойствами, по которым их отбирают и применяют в той или иной области. Материалы получают разнообразными способами. Некоторые разновидности металлов соединяют вместе, чтобы получить сплавы, приобретающие уникальные физические и химические свойства.
В строительстве, промышленности и других сферах жизни человека часто используются различные виды металлов. Они отличаются между собой свойствами, по которым их отбирают и применяют в той или иной области. Материалы получают разнообразными способами. Некоторые разновидности металлов соединяют вместе, чтобы получить сплавы, приобретающие уникальные физические и химические свойства.
- Характеристики и признаки
- Группа с железом и его сплавами
- Цветные разновидности
- Тяжёлые металлы
- Мягкие виды
- Благородные материалы
- Классификация по твёрдости
Характеристики и признаки
Металлы представляют собой группу элементов в виде простых веществ, имеющих характерные металлические свойства. В природе они присутствуют в виде руд или соединений. Изучением характеристик этих материалов занимаются такие науки, как химия, физика и металловедение.
Металлы обладают совокупностью различных свойств. По механическим определяют их способность сопротивляться деформации и разрушению. Технологические помогают определить податливость материалов к различным видам обработки. Химические свойства показывают их взаимодействие с разными веществами, а физические говорят об их поведении в тепловом, гравитационном или электромагнитном полях.
Металлы классифицируют по следующим свойствам:
 Твёрдость — устойчивость материала к проникновению другого.
Твёрдость — устойчивость материала к проникновению другого.- Прочность — сохранение формы, структуры и размера после воздействия динамической, статической и знакопеременной нагрузки.
- Упругость — изменение формы без нарушения целостности при деформации и возможность возвращения к первоначальному виду.
- Пластичность — удерживание полученной формы и целостности под воздействием сил.
- Износостойкость — сохранение наружной и внутренней целостности под воздействием продолжительного трения.
- Вязкость — удерживание целостности под увеличивающимся физическим воздействием.
- Усталость — число и период циклических воздействий, выдерживаемых металлом без изменения целостности.
- Жароустойчивость — стойкость к высоким температурам.
Первостепенным признаком металлов выступает отрицательный коэффициент проводимости электричества, который при понижении температуры повышается, а при повышении — частично или полностью теряется. Второстепенными признаками материалов являются металлический блеск и высокая температура плавления. Кроме того, некоторые типы металлов, являющихся соединениями, могут быть восстановителями при окислительно-восстановительных реакциях.
Металлические свойства взаимосвязаны, так как составляющие материала влияют на все остальные параметры. Металлы подразделяются на чёрные и цветные, но их классифицируют по многим признакам.
Группа с железом и его сплавами
Чёрным металлам свойственны внушительная плотность, большая температура плавления и тёмно-серый окрас. К этой группе в основном относят железо с его сплавами. Для придания последним специфических свойств используют легирующие компоненты.
Подгруппы чёрных видов металлов:
 Железные — железо, кобальт, марганец, никель. Обычно их берут за основу или как добавку к сплавам.
Железные — железо, кобальт, марганец, никель. Обычно их берут за основу или как добавку к сплавам.- Тугоплавкие — вольфрам, молибден, титан, хром. Они плавятся при температуре, превышающей уровень плавления железа. Из тугоплавких разновидностей получают легированные стали.
- Редкоземельные — лантан, неодим, церий. Они имеют родственные химические свойства, но различаются по физическим параметрам. Используются как присадка к сплавам.
- Урановые (актиноиды) — актиний, нептуний, плутоний, торий, уран. Широко используются в атомной энергетике.
- Щёлочноземельные — кальций, литий, натрий. В свободном виде не применяются.

Металлы чёрной группы представлены сплавами железа с разным содержанием углерода и содержанием дополнительных химических элементов: кремнием, серой или фосфором. Популярными материалами выступают сталь и чугун. В стали содержится до 2% углерода. Ей характерна хорошая пластичность и высокие технологические показатели. В чугуне содержание углерода может достигать 5%. Свойства сплава могут отличаться с различными химическими элементами: с содержанием серы и фосфора повышается хрупкость, а с хромом и никелем чугун становится стойким к высоким температурам и коррозии.
Цветные разновидности
Цветные металлы более востребованы, чем чёрные, поскольку большая часть из них представляет собой сырье для производства металлопроката. Эта группа материалов отличается широкой сферой применения: они используются в металлургии, машиностроении, радиоэлектронике, сфере высоких технологий и других областях.
Классификация по физическим параметрам:
- Тяжёлые — кадмий, никель, олово, ртуть, свинец, цинк. В природных условиях они образуются в прочных соединениях.
- Лёгкие — алюминий, магний, стронций, титан и другие. Характеризуются невысокой температурой плавления.
- Благородные — золото, платина, родий, серебро. Для них свойственна повышенная стойкость к коррозии.

Цветные металлы отличаются небольшой плотностью, хорошей пластичностью, невысокой температурой плавления и преобладающими цветами (белым, жёлтым, красным). Из них изготавливается различная техника. Поскольку прочность материалов довольно низкая, их не используют в чистом виде. Из них производят лёгкие сплавы различного назначения.
Тяжёлые металлы
Материалы этой группы характеризуются внушительным атомным весом и плотностью, превышающей показатель у железа.
 Большим спросом пользуется медь, которая выступает проводником электрического тока. Она отличается розовато-красным оттенком, маленьким удельным сопротивлением, хорошей теплопроводностью, небольшой плотностью, прекрасной пластичностью и устойчивостью к коррозии. В сфере техники используют сплавы меди: бронзу (с добавлением алюминия, никеля или олова) и латунь (с цинком). Бронзу применяют в производстве мембран, круглых и плоских пружин, червячных пар и разной арматуры. Из латуни изготавливают ленты, листы, проволоку, трубы, втулки, подшипники.
Большим спросом пользуется медь, которая выступает проводником электрического тока. Она отличается розовато-красным оттенком, маленьким удельным сопротивлением, хорошей теплопроводностью, небольшой плотностью, прекрасной пластичностью и устойчивостью к коррозии. В сфере техники используют сплавы меди: бронзу (с добавлением алюминия, никеля или олова) и латунь (с цинком). Бронзу применяют в производстве мембран, круглых и плоских пружин, червячных пар и разной арматуры. Из латуни изготавливают ленты, листы, проволоку, трубы, втулки, подшипники.
Группа тяжёлых металлов выступает одной из главных причин загрязнения окружающей среды. Токсичные вещества поступают в океаны через сточные воды с предприятий отрасли промышленности. Некоторые разновидности тяжёлой группы могут накапливаться в живых организмах.
Ртуть относится к высокотоксичным металлам для людей. При сжигании угля на электростанциях её соединения переходят в атмосферу, а затем преобразуются в осадки и попадают в водоёмы. Обитатели пресноводных и морских систем накапливают большое количество опасного вещества, что приводит к отравлениям или смерти людей.
Кадмий считается рассеянным и достаточно редким элементом, способным попадать в океан через сточные воды с металлургических предприятий. Это вещество в малом количестве есть в человеческом организме, но при высоком показателе он разрушает костную ткань и приводит к анемии.
Свинец в рассеянном состоянии присутствует почти везде. При избытке металла в организме человека наблюдаются проблемы со здоровьем.
Мягкие виды
Алюминий серебристо-белого цвета характеризуется лёгкостью, высокой устойчивостью к коррозии, хорошей электропроводностью и пластичностью. Характеристики материала сделали его полезным в самолётостроении, электропромышленности и пищевом производстве. Алюминиевые сплавы применяются в сфере машиностроения.
Магнию свойственна низкая коррозийная устойчивость, зато лёгкий материал незаменим в технической области. В сплавах с этим металлом используют алюминий, марганец и цинк, которые хорошо режутся и отличаются высокой прочностью. Магниевые сплавы используют в производстве корпусов для фотоаппаратов, двигателей и других приборов.
Титан применяют в машиностроении, ракетной отрасли и химической промышленности. Сплавы с содержанием этого вещества характеризуются небольшой плотностью, отличными механическими свойствами, коррозийной устойчивостью и податливостью обработке давлением.
Благородные материалы
Некоторые разновидности металлов редко встречаются в природе и отличаются трудоёмкими способами добычи. Металлы благородной группы — это:
 Золото.
Золото.- Серебро.
- Платина.
- Родий.
Люди узнали о золоте ещё в эпоху каменного века. Самый дорогой металл в мире можно встретить в природе в виде самородков, в которых присутствует небольшое количество примесей. Также он встречается в сплавах с серебром.
Золото отличается теплопроводностью и очень низким сопротивлением. Из-за хорошей ковкости материал применяют в изготовлении ювелирных изделий.
Серебро идёт вторым по ценности после золота. В природе оно обычно встречается в качестве серебряной руды. Серебру характерны мягкость, пластичность, тепло- и электропроводность.
Платина, открытая в середине XX века, выступает редким материалом, который можно отыскать только в залежах различных сплавов. Её довольно трудно добывать. Ценность металла заключается в том, что он не подвергается воздействию кислот. При нагревании платина не изменяется в окраске и не окисляется.
Родий тоже относится к благородным металлам. Он обладает серебристым цветом с голубым отливом. Родий отличает устойчивость к химическим воздействиям и перепадам температур, но хрупкий металл портится под механическим воздействием.
Классификация по твёрдости
Металлы также делят на твёрдые и мягкие.
 Самый твёрдый из чистейших материалов в мире — это хром. Он относится к тугоплавким разновидностям и отлично поддаётся механической обработке. Другим твёрдым элементом выступает вольфрам. Он характеризуется высокой температурой плавления, теплоустойчивостью и гибкостью. Из него выковывают различные детали и изготавливают небольшие элементы, необходимые для осветительных приборов. Вольфрам часто присутствует в тяжёлых сплавах. Твёрдые металлы сложно не только добывать, но и просто найти на планете. В основном их содержат упавшие на Землю метеориты.
Самый твёрдый из чистейших материалов в мире — это хром. Он относится к тугоплавким разновидностям и отлично поддаётся механической обработке. Другим твёрдым элементом выступает вольфрам. Он характеризуется высокой температурой плавления, теплоустойчивостью и гибкостью. Из него выковывают различные детали и изготавливают небольшие элементы, необходимые для осветительных приборов. Вольфрам часто присутствует в тяжёлых сплавах. Твёрдые металлы сложно не только добывать, но и просто найти на планете. В основном их содержат упавшие на Землю метеориты.
К самым мягким металлам относят калий, натрий, рубидий и цезий. Также в этой группе состоят золото, серебро, медь и алюминий. Золото присутствует в морских комплексах, осколках гранитов и человеческом организме. Внешние факторы способны разрушить ценный металл. Мягкое серебро применяют в изготовлении посуды и ювелирных украшений. Натрий широко используют практически в любой промышленной отрасли. Ртуть, выступающую самым мягким металлом в мире, применяют сельскохозяйственной и химической промышленности, а также электротехнике
Золото и серебро: какой металл тверже и долговечнее
Выбор золотых и серебряных никогда не основывается на том, какой металл тверже и прочнее. В основном все смотрят на его красоту в изделии. Кому-то нравятся теплые оттенки золота. Кто-то же без ума от холодного блеска серебра. И лишь после покупки приглянувшегося ювелирного украшения, и носки его пару месяцев понимаю, что стоило уделить внимание вопросу, что мягче, серебро или золото. Не пришлось бы нести еще совсем новое украшение в мастерскую для исправления досадных царапин и вмятин.
Покупка ювелирного украшения – это не только способ подчеркнуть свой личный стиль. Также это и немалое вложение в свое самовыражение. Чтобы очень скоро после покупки не было досадно, стоит взвесить все за и против относительно всех характеристик украшения, а не только цены на золото или серебро и на то, как украшение смотрится на вас.
Физические свойства драгоценных металлов
Вопрос, какой металл из золота и серебра мягче, очень относительный. И если не касаться только их физических свойств, то можно сказать, что оба вида металла по прочности проигрывают другим.
Говоря о ювелирных металлах, т.е. используемых для изготовления драгоценностей, можно перечислить группу. И по стоимости отнюдь не золото или серебро буду главенствовать в этом списке. Также к драгоценным металлам относятся: палладий, платина, родий. Именно в сравнении с ними как золото, так и серебро нельзя назвать прочными. И именно эти металлы помогают золотым и серебряным украшениям быть пригодными к длительной носке – их включают в сплавы золота и серебра.
Характеристики драгоценных металлов очень похожи. Но все же, среди всех золото и, конечно же, серебро более мягкие. И об этом говорит шкала Фридриха Мооса. Если расположить ювелирные металлы от самого прочного к самому мягкому, то перечень с указанием баллов будет выглядеть так:
- родий – 6;
- палладий – 4,75;
- платина – 4-4,45;
- серебро – 2,5-3;
- золото – 2,5-3.
Как видите, последнее место делят оба металла, который мы привыкли видеть в украшениях. Что же получается, серебро и золото в равной части твердые? Отнюдь.
Существует еще одна шкала определения твердости металлов, ученого Бринеля. По ней два этих металла очень схожи, но золото все же, мягче серебра: показатель 220-250 против 240-250. Так что, как не крути, серебро выигрывает в сравнении по твердости.
На самом деле, показатели твердости и по шкале Мооса, и Бринеля, говорят о том, что оба металла ну очень мягкие. В чистом виде их легко поцарапать ногтем. Именно по этой причине не существует украшений из стопроцентного золота или серебра.
Что делает драгоценные металлы прочными

Только благодаря лигатуре, золото и серебро становятся пригодными для изготовления украшений, а в случае с серебром и столовых приборов. Что это такое, лигатура? Простым языком – примеси других металлов, добавляющие прочности.
В золоте лигатуры 41,5 % из 100% всего металла в изделии. Из этого и рождена самая распространенная проба, т.е. остаточные 58,5 % преобразовываются в пробу 585. Конечно же, существует еще проба 375 и 750. Золото таких проб соответственно более прочное и менее прочное, чем 585 пробы.
В лигатуру самой распространенной пробы золота, т.е. 585, входят: медь, серебро, никель и палладий. В зависимости от оттенка изделия можно угадать, какого именно добавочного металла больше. В пробе 375 присутствует только медь и серебро, а вот в 750, напротив, к списку металлов 585 пробы еще добавляется платина.
Если так же рассматривать серебро, то лигатуры в нем 7,5%, т.е. чистого серебра в изделии 92,5%, что соответствует 925 пробе. Как и у золота, у белого металла тоже есть разные пробы. Но они совершенно не подходят для ювелирных украшений.
Лигатурой для ювелирного серебра выступает медь. Именно она делает украшения более прочными. Из-за малого содержания этого металла, красный цвет никак не проявляется в сплаве с серебром.
Как влияет мягкость золота и серебра на украшения
Итак, определив, что все же из двух металлов: золота и серебра, именно последнее более прочное, модно было бы предположить, что и покупать стоит именно его в некоторых случаях. Однако не все так просто. Не стоит принимать поспешных решений по массе причин.
Изделия бывают разные. И, если мы говорим, например, о кольце, то его сложно повредить, погнуть или сломать. Это касается и золотых украшений и серебряных. А вот цепочки, конечно же, прочнее серебряные, если взять за сравнение один и тот же вид плетения.
Вы можете купить серебряную цепочку на шею или браслет, а можете купить золотую, но с более надежным плетением.
Периодичность использования украшения. Если изделие предполагает ежедневное ношение, можно подумать, что стоит взять его из серебра. Однако не все так страшно, как может представиться.
Золотые кольца, например, легко отполировать даже в домашних условиях, убирая мелкие царапины. Ну а если изделие из золота очень дорогое, возможно с бриллиантами, то вы и так его не будете носить каждый день. И за время периодического выхода в свет, с ними точно ничего не случится.
Вид вашей деятельности. Работаете руками и переживаете, что золотое украшение будет все время тереться о станок или цепляться за инструмент? Не повод заменить его не серебряное. Просто снимайте украшения на время работы. При подобной занятости повредится любое, даже дешевая бижутерия.
Вмятины и царапины способны появиться как на серебре, так и на золоте. Однако это не повод отказываться от любимого вида металла в украшении в пользу другого. Достаточно знать, как ухаживать за украшениями и думать, в какой момент их лучше снять.
Классификация металлов. Характеристика металлов и области применения
Несколько научных дисциплин (материало- и металловедение, физика, химия) занимаются изучением свойств и характеристик металлов. Существует их общепринятая классификация. Однако каждая из дисциплин при их изучении опирается на особые специализированные параметры, находящиеся в сфере ее интересов. С другой стороны, все науки, изучающие металлы и сплавы, придерживаются одной точки зрения, что существует две основные группы: черные и цветные.
Признаки металлов
Различают следующие основные механические свойства:
- Твердость – определяет возможность одного материала противодействовать проникновению другого, более твердого.
- Усталость – количество, а также время циклических воздействий, которое может выдержать материал без изменения целостности.
- Прочность. Заключается в следующем: если приложить динамическую, статическую или знакопеременную нагрузку, то это не приведет к изменению формы, строения и размеров, нарушению внутренней и наружной целостности металла.
- Пластичность – это способность удерживать целостность и полученную форму при деформации.
- Упругость – это деформация без нарушения целостности под воздействием определенных сил, а также после избавления от нагрузки возможность к возращению первоначальной формы.
- Стойкость к трещинам – под влиянием внешних сил в материале они не образуются, а также сохраняется наружная целостность.
- Износостойкость – способность сохранять наружную и внутреннюю целостность при продолжительном трении.
- Вязкость – сохранение целостности при увеличивающихся физических воздействиях.
- Жаростойкость – противостояние изменению размера, формы и разрушению при воздействии высоких температур.
Классификация металлов
К металлам относятся материалы, обладающие совокупностью механических, технологических, эксплуатационных, физических и химических характерных свойств:
- механические подтверждают способность к сопротивлению деформации и разрушению;
- технологические свидетельствуют о способности к разному виду обработки;
- эксплуатационные отражают характер изменения при эксплуатации;
- химические показывают взаимодействие с различными веществами;
- физические указывают на то, как ведет себя материал в разных полях – тепловом, электромагнитном, гравитационном.

Химические, физические и механические свойства тесно взаимосвязаны между собой, так как состав материала устанавливает все остальные его параметры. Например, тугоплавкие металлы являются самыми прочными. Свойства, которые проявляются в состоянии покоя, называются физическими, а под воздействием извне – механическими. Также существуют таблицы классификации металлов по плотности — основному компоненту, технологии изготовления, температуре плавления и другие.
Черные металлы
Материалы, относящиеся к этой группе, обладают одинаковыми свойствами: внушительной плотностью, большой температурой плавления и темно-серой окраской. К первой большой группе черных металлов принадлежат следующие:
- Железные – кобальт, марганец, никель, железо. Применяются в качестве основы или добавок к сплавам.
- Тугоплавкие – хром, вольфрам, молибден, титан. Все они имеют температуру плавления, превышающую уровень, при котором плавится железо. Используются как основа или добавка для получения легированных сталей.

Цветные металлы
Вторая по величине группа имеет небольшую плотность, хорошую пластичность, невысокую температуру плавления, преобладающие цвета (белый, желтый, красный) и состоит из следующих металлов:
- Легкие – магний, стронций, цезий, кальций. В природе встречаются только в прочных соединениях. Применяются для получения легких сплавов разного назначения.
- Благородные. Примеры металлов: платина, золото, серебро. Они обладают повышенной устойчивостью к коррозии.
- Легкоплавкие – кадмий, ртуть, олово, цинк. Имеют невысокую температуру плавления, участвуют в производстве разных сплавов.

Медь и сплавы с медью
В чистом виде имеет розовато-красный цвет, маленькое удельное сопротивление, небольшую плотность, хорошую теплопроводность, отличную пластичность, обладает стойкостью к коррозии. Находит широкое применение как проводник электрического тока. Для технических нужд используют два вида сплавов из меди: латуни (медь с цинком) и бронзы (медь с алюминием, оловом, никелем и другими металлами). Латунь используется для изготовления листов, лент, труб, проволоки, арматуры, втулок, подшипников. Из бронзы изготавливают плоские и круглые пружины, мембраны, разную арматуру, червячные пары.
Алюминий и сплавы
Этот очень легкий металл, имеющий серебристо-белый цвет, обладает высокой коррозийной стойкостью. У него хорошая электропроводность и пластичность. Благодаря своим характеристикам нашел применение в пищевой, легкой и электропромышленности, а также в самолетостроении. Сплавы из алюминия очень часто используются в машиностроении для изготовления особо ответственных деталей.
Магний, титан и их сплавы
Магний неустойчив к коррозии, зато не существует легче металла, используемого для технических нужд. В основном его добавляют в сплавы с другими материалами: цинком, марганцем, алюминием, которые прекрасно режутся и являются достаточно прочными. Из сплавов с легким металлом магнием изготавливают корпусы фотоаппаратов, различных приборов и двигателей. Титан нашел свое применение в ракетной отрасли, а также машиностроении для химической промышленности. Титаносодержащие сплавы имеют небольшую плотность, прекрасные механические свойства и стойкость к коррозии. Они хорошо поддаются обработке давлением.
Антифрикционные сплавы
Такие сплавы определены для увеличения срока службы поверхностей, испытывающих трение. Они сочетают в себе следующие характеристики металла – хорошую теплопроводность, маленькую температуру плавления, микропористость, слабый коэффициент трения. К антифрикционным относят сплавы, основой которых является свинец, алюминий, медь или олово. К самым применяемым относятся:
- баббит. Его изготовляют на основе свинца и олова. Используют в производстве вкладышей для подшипников, которые работают на больших скоростях и при ударных нагрузках;
- алюминиевые сплавы;
- бронза;
- металлокерамические материалы;
- чугун.
Мягкие металлы
По системе классификации металлов это золото, медь, серебро, алюминий, но среди самых мягких выделяют цезий, натрий, калий, рубидий и другие. Золото сильно распылено в природе. Оно есть в морской воде, организме человека, а также его можно встретить практически в любом осколке гранита. В чистом виде золото имеет желтый с оттенком красного цвет, так как металл мягкий — его можно поцарапать даже ногтем. Под влиянием окружающей среды золото достаточно быстро разрушается. Этот металл является незаменимым для электрических контактов. Несмотря на то что серебра в двадцать раз больше, чем золота, он также является редким.

Металлом является ртуть, хоть и находится в жидком состоянии, поэтому считается одним из самых мягких в мире. Этот материал используется в оборонной и химической промышленности, сельском хозяйстве, электротехнике.
Твердые металлы
В природе практически нет самых твердых металлов, поэтому добыть их очень сложно. В большинстве случаев их находят в упавших метеоритах. Хром принадлежит к тугоплавким металлам и является самым твердым из чистейших на нашей планете, к тому же он легко поддается механической обработке.

Металлы в энергетике
Металлы, в состав которых входят свободные электроны и положительные ионы, считаются хорошими проводниками. Это довольно востребованный материал, характеризующийся пластичностью, высокой электропроводностью и способностью легко отдавать электроны.

- свинец — за большую устойчивость к коррозии;
- медь — за высокую электропроводность, легкость в обработке, стойкость к коррозии и достаточную механическую прочность;
- алюминий — за небольшой вес, устойчивость к вибрациям, прочность и температуру плавления.
Категории черных вторичных металлов
К отходам черных металлов предъявляют определенные требования. Для отправки сплавов в сталеплавильные печи потребуются определенные операции по их обработке. Перед подачей заявки на перевозку отходов необходимо ознакомиться с ГОСТом черных металлов для определения его стоимости. Черный вторичный лом классифицируют на стальной и чугунный. Если в составе присутствуют легирующие добавки, то его относят к категории «Б». В категорию «А» включены углеродистые: сталь, чугун, присад.
Металлурги и литейщики из-за ограниченности первичной сырьевой базы проявляют активный интерес к вторичному сырью. Использование лома черных металлов вместо металлической руды – это ресурсное, а также энергосберегающее решение. Вторичный черный металл используют как охладитель конвертерной плавки.

Диапазон применения металлов невероятно широк. Черные и цветные неограниченно используются в строительной и машинной индустрии. Не обойтись без цветных металлов и в энергетической промышленности. Редкие и драгоценные идут на изготовление украшений. В искусстве и медицине находят применение как цветные, так и черные металлы. Невозможно представить жизнь человека без них, начиная от хозяйственных принадлежностей и до уникальных приборов и аппаратов.
Сортамент металлопроката «Линейка — S»
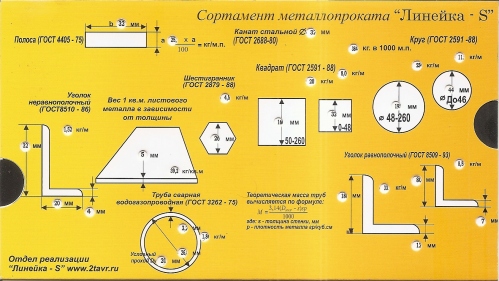
- Сортамент «Линейка-S»
- Цена «Линейки-S»
- Как работает сортамент
- С вашим логотипом от 200 шт.
- Фото «Линейки — S»
- Доставка
- Отзывы о сортаменте
- Купить
- ————————-
- Сортамент металла
- Сталь листовая
- Полоса стальная
- Вес металлопроката


Какой металл самый твёрдый, какой — самый мягкий?
Самый твердый металл — хром, титан.
Хром — элемент побочной подгруппы шестой группы четвёртого периода периодической системы химических элементов Менделеева Д.И., с атомным номером 24. Обозначается символом Cr (латин. Chromium). Простое вещество хром (CAS-номер: 7440-47-3) — твёрдый металл голубовато-белого цвета.
 Хром в природе встречается в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом):
Хром в природе встречается в основном в виде хромистого железняка Fe(CrO2)2 (хромит железа). Из него получают феррохром восстановлением в электропечах коксом (углеродом):
FeO · Cr2O3 + 4C → Fe + 2Cr + 4CO↑Хром относится к достаточно распространенным элементам, содержание его в земной коре составляет примерно 0,02% (22-е место).
Феррохром применяют для производства легированных сталей.
Чтобы получить чистый хром, реакцию ведут следующим образом:
1) сплавляют хромит железа с карбонатом натрия (кальцинированная сода) на воздухе:
4Fe(CrO2)2 + 8Na2CO3 + 7O2 → 8Na2CrO4 + 2Fe2O3 + 8CO2↑2) растворяют хромат натрия и отделяют его от оксида железа;
3) переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
4) получают чистый оксид хрома восстановлением дихромата углём:
Na2Cr2O7 + 2C → Cr2O3 + Na2CO3 + CO↑5) с помощью алюминотермии получают металлический хром:
Cr2O3+ 2Al → Al2O3 + 2Cr + 130 ккал6) с помощью электролиза получают электролитический хром из раствора хромового ангидрида в воде, содержащего добавку серной кислоты. При этом на катодах совершаются в основном 3 процесса:
восстановление шестивалентного хрома до трехвалентного с переходом его в раствор;
разряд ионов водорода с выделением газообразного водорода;
разряд ионов, содержащих шестивалентный хром, с осаждением металлического хрома;
Cr2O72− + 14Н+ + 12е− = 2Cr + 7H2OПолучение хрома
Сырьем для промышленного получения хрома служит хромистый железняк. Его химическая переработка приводит к Cr2O3. Восстановление Cr2O3 с помощью алюминия или кремния дает металлический хром невысокой степени чистоты:
Cr2O3+Аl=Аl2O3+2Cr
2Cr2O3+3Si=3SiO2+4Cr
Более чистый металл получают электролизом концентрированных растворов соединений хрома.Тита́н — (лат. Titanium; обозначается символом Ti) — элемент побочной подгруппы четвёртой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 22. Простое вещество титан (CAS-номер: 7440-32-6) — лёгкий металл серебристо-белого цвета. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура перехода α↔β 883 °C
Самые мягкие металлы — калий, рубидий, цезий.
Калий — элемент главной подгруппы первой группы, четвёртого периода периодической системы химических элементов Менделеева Д.И., с атомным номером 19. Обозначается символом K (латин. Kalium). Простое вещество калий (CAS-номер: 7440-09-7) — мягкий щелочной металл серебристо-белого цвета.
В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Он очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь. Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они все же отличаются. Рубидий — элемент главной подгруппы первой группы, пятого периода периодической системы химических элементов Менделеева Д.И., с атомным номером 37. Обозначается символом Rb (лат. Rubidium). Простое вещество рубидий (CAS-номер: 7440-17-7) — мягкий щелочной металл серебристо-белого цвета.
Рубидий — элемент главной подгруппы первой группы, пятого периода периодической системы химических элементов Менделеева Д.И., с атомным номером 37. Обозначается символом Rb (лат. Rubidium). Простое вещество рубидий (CAS-номер: 7440-17-7) — мягкий щелочной металл серебристо-белого цвета.Цезий — элемент главной подгруппы первой группы шестого периода периодической системы химических элементов Менделеева Д.И., атомный номер 55. Обозначается символом Cs (лат. Caesium). Простое вещество цезий (CAS-номер: 7440-46-2) — мягкий щелочной металл серебристо-жёлтого цвета. Своё название цезий получил за наличие двух ярких синих линий в эмиссионном спектре (от лат. caesius — небесно-голубой).
Из рубрики Почемучка.
— Для начала скажи-ка мне, Панамка, какие ты вообще знаешь металлы?
— Железо.
— А еще?
— Еще? Нет, больше не знаю.
— Знаешь, знаешь. Ты подумай хорошенько, вспомни. Ладно, подскажу. Вот ответь, из чего сделано грузило для удочки?
— Из свинца.
— А мамино колечко из чего?
— Из золота.
— Правильно. Но и свинец и золото — металлы. Кастрюля — алюминиевая, значит, металлическая, ступка и пестик — латунные, металлические провода, если соскоблить с них пластмассовую «одежду», — медные, металлические. Много еще на свете разных металлов! И у многих из них удивительнейшие свойства. Какие? А вот ответь на мои вопросы: обязательно ли металлы тонут в воде?
— Обязательно. Даже иголка и та тонет. Я видел.
— Так вот, есть, Панамка, такие легкие металлы, которые плавают в воде, как пробка. Один из них называется литием. Он легче воды. не помню, на сколько. Бумка, наверное, знает.
— АЛЛО, ВКЛЮЧАЮСЬ.
ЛИТИЙ ВДВОЕ ЛЕГЧЕ ВОДЫ И В 15 РАЗ ЛЕГЧЕ ЖЕЛЕЗА. ЛИТИЙ ВХОДИТ В СОСТАВ БОЛЕЕ 150 МИНЕРАЛОВ ОН ЕСТЬ ПОЧТИ В КАЖДОМ КАМНЕ И ПОЭТОМУ ПОЛУЧИЛ ТАКОЕ НАЗВАНИЕ: ГРЕЧЕСКОЕ СЛОВО «ЛИТОС» ОЗНАЧАЕТ «КАМЕНЬ». ЭТОТ СЕРЕБРИСТОБЕЛЫЙ МЕТАЛЛ В ЖАРКИХ
ПЕЧАХ РАСПЛАВЛЯЮТ И СМЕШИВАЮТ С ДРУГИМИ МЕТАЛЛАМИ. ПОЛУЧАЮТСЯ СПЛАВЫ. АЛЮМИНИЙ НЕ ОЧЕНЬ ПРОЧЕН, НО, ЕСЛИ ЕГО СПЛАВИТЬ С ЛИТИЕМ, ПОЛУЧАЕТСЯ МЕТАЛЛ КУДА ПРОЧНЕЕ.
— Спасибо, Бумка. Задаю новый вопрос: металлы болеют?
— Болеют?! Вот смешно!
Значит, у водопроводного крана бывает насморк, а у перочинного ножика — коклюш?
Умора!
— Металлы еще как болеют.
Разве ржавчина, о которой мы недавно говорили, не болезнь металлов? Они от нее даже «умирают», разрушаются. Была сталь, а долго пролежала в воде — разрушилась, покрылась рыжей ржавчиной. Тронь — рассыплется в порошок. Недаром в народе говорят: ржа (тоесть ржавчина) железо ест. Вот и съела. Теперь ответь — бывает ли металл жидкий? Не когда его расплавят в жаркой печи, а всегда жидкий?
— Жидкий металл, дедушка Знай? Да это все равно что «горячий лед»!
— Значит, говоришь, не бывает? А ты разве забыл про ртуть, которая показывает температуру в градуснике? Это же самый настоящий жидкий металл! Случайно уронишь, разобьешь градусник — ртуть растечется по полу мелкими шариками. Соберешь их — мигом сольются в один. Твердеет этот жидкий металл лишь на очень сильном морозе.
Кстати, ртуть нужна не только для градусников. Она необходима и для ламп-трубок, которые дают яркий дневной свет. Ртуть входит в состав красок, которыми покрывают днища кораблей. После этого корабли не так ржавеют даже в соленой морской воде и их днище меньше обрастает ракушками и водорослями.
Ну а под конец давай ответим на вопрос: какой металл самый прочный, какой самый мягкий?
Сперва о самом прочном. Он серебристо-белого цвета и называется титаном. Титан в 12 раз тверже алюминия, в 4 раза тверже железа и меди. Если раскалить другие металлы, они сразу потеряют прочность. Но титан. температура 500 градусов, а он все такой же прочный, как был. Не зря ведь многие части реактивных самолетов сделаны из титана. Этот металл такой прочный, что поддается только самым могучим машинам-молотам.
Зато натрий (тоже серебристо-белый) , хоть он и металл, ничего не стоит сплющить пальцами. А магний знаменит тем, что хорошо горит. Да, да — металл, а горит! Поднес к тонкой стружке магния зажженную спичку — он и вспыхнул.Вот вам ответ на вопрос: Какой металл самый твёрдый, какой — самый мягкий
Физические свойства металлов: твердость, плотность и др.












Металлы имею такие физические свойства, как твердость, температуру плавления, плотность, пластичность, электропроводность, теплопроводность и цвет.
Твёрдость:
Все металлы, кроме ртути и, условно, франция, при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью.
Таблица твёрдости металлов по шкале Мооса:
Твёрдость Металл 0.2 Цезий 0.3 Рубидий 0.4 Калий 0.5 Натрий 0.6 Литий 1.2 Индий 1.2 Таллий 1.25 Барий 1.5 Стронций 1.5 Галлий 1.5 Олово 1.5 Свинец 1.5 Ртуть 1.75 Кальций 2.0 Кадмий 2.25 Висмут 2.5 Магний 2.5 Цинк 2.5 Лантан 2.5 Серебро 2.5 Золото 2.59 Иттрий 2.75 Алюминий 3.0 Медь 3.0 Сурьма 3.0 Торий 3.17 Скандий 3.5 Платина 3.75 Кобальт 3.75 Палладий 3.75 Цирконий 4.0 Железо 4.0 Никель 4.0 Гафний 4.0 Марганец 4.5 Ванадий 4.5 Молибден 4.5 Родий 4.5 Титан 4.75 Ниобий 5.0 Иридий 5.0 Рутений 5.0 Тантал 5.0 Технеций 5.0 Хром 5.5 Бериллий 5.5 Осмий 5.5 Рений 6.0 Вольфрам 6.0 β-Уран Температура плавления:
Температуры плавления чистых металлов лежат в диапазоне от −38,83 °C (ртуть) до 3422 °C (вольфрам).
Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые металлы, например, олово и свинец, могут расплавиться на обычной электрической или газовой плите.
В зависимости от температуры плавления металлы делятся на: легкоплавкие (до 600 °C); среднеплавкие (от 600 до 1600 °C); тугоплавкие (выше 1600 °C).
Таблица температуры плавления легкоплавких металлов и сплавов:
Название металла Температура плавления, о С Ртуть -38,83 Франций 25 Цезий 28,44 Галлий 29,7646 Рубидий 39,3 Калий 63,5 Натрий 97,81 Индий 156,5985 Литий 180,54 Олово 231,93 Полоний 254 Висмут 271,3 Таллий 304 Кадмий 321,07 Свинец 327,46 Цинк 419,53 Таблица температуры плавления среднеплавких металлов и сплавов:
Название металла Температура плавления, о С Сурьма 630,63 Нептуний 639 Плутоний 639,4 Магний 650 Алюминий 660,32 Радий 700 Барий 727 Стронций 777 Церий 795 Иттербий 824 Европий 826 Кальций 841,85 Лантан 920 Празеодим 935 Германий 938,25 Серебро 961,78 Неодим 1024 Прометий 1042 Актиний 1050 Золото 1064,18 Самарий 1072 Медь 1084,62 Уран 1132,2 Марганец 1246 Бериллий 1287 Гадолиний 1312 Тербий 1356 Диспрозий 1407 Никель 1455 Гольмий 1461 Кобальт 1495 Иттрий 1526 Эрбий 1529 Железо 1538 Скандий 1541 Тулий 1545 Палладий 1554,9 Протактиний 1568 Таблица температуры плавления тугоплавких металлов и сплавов:
Название металла Температура плавления, о С Лютеций 1652 Титан 1668 Торий 1750 Платина 1768,3 Цирконий 1855 Хром 1907 Ванадий 1910 Родий 1964 Технеций 2157 Гафний 2233 Рутений 2334 Иридий 2466 Ниобий 2477 Молибден 2623 Тантал 3017 Осмий 3033 Рений 3186 Вольфрам 3422 Плотность:
В зависимости от плотности металлы делят на лёгкие (плотность от 0,53 до 5 г/см³) и тяжёлые (от 5 до 22,6 г/см³).
Самым лёгким металлом является литий (плотность 0,53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22,6 г/см³ — ровно в два раза выше плотности свинца ), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Пластичность:
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними.
Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются.
Пластичность зависит и от чистоты металла . Так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы, такие, как золото, серебро, свинец, алюминий, осмий, могут срастаться между собой, но на это могут уйти десятки лет.
Электропроводность:
Все металлы хорошо проводят электрический ток, обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля.
Серебро, медь и алюминий имеют наибольшую электропроводность. По этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также и натрий. В экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Теплопроводность:
Теплопроводность металлов зависит от подвижности свободных электронов.
Поэтому ряд теплопроводностей похож на ряд электропроводностей, и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла. Широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Наименьшая теплопроводность — у висмута и ртути.
Цвет у большинства металлов примерно одинаковый — светло-серый, иногда с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Металлы подразделяются на цветные и черные.
Чёрные металлы – железо и сплавы на его основе (стали, ферросплавы, чугуны). К чёрным металлам также зачастую относят марганец и, иногда, – хром и ванадий.
Цветные металлы — это особый класс нержавеющих металлов и сплавов, в составе которых нет железа. Металлы называются цветными, потому что каждый из них имеет определенный окрас. К цветным металлам относятся медь, молибден, свинец, цинк, олово, никель, кадмий, кобальт, алюминий, титан, магний, висмут, вольфрам, ртуть, золото, платину, серебро, палладий, родий, рутений, осмий, иридий.
Учимся плавить аллюминий
Чтобы правильно плавить металл, необходимо учитывать температуру плавки алюминия. Чистый сплав легко плавится уже при +660°С, а оксидная пленка только при +2300°С. Опасно самостоятельно плавить порошок, он способен воспламениться. Кусочки алюминия плавят сухими, вода в расплаве способна спровоцировать взрыв.
О температуре плавления
Необходимо помнить: алюминий очень легко поддается литью и начинает превращаться в жидкую субстанцию уже при температуре в 660 градусов. Для того чтобы понять, что этот показатель довольно низкий, достаточно сравнить его с температурами плавления других металлов, которые также нередко используются для изготовления тех или иных, нужных в обиходе предметов.
- сталь начинает плавиться лишь при температуре в 1300 градусов;
- чугун — при 1100 градусах.
Но все же, хоть температура плавления алюминия по Цельсию и не слишком высока по сравнению со многими другими металлами, достичь 600 градусов в домашних условиях с использованием обыкновенной газовой или электрической плиты довольно трудно.
Уменьшение температуры
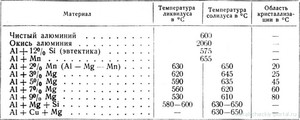
Прежде чем подвергать металл плавлению, можно специальными методами уменьшить его температуру плавления, например, использовать в виде порошка. В этом случае он начнет плавиться чуть быстрее. Но при этом он становится опасным, так как взаимодействуя с атмосферным кислородом, может окислиться или воспламениться. А в результате окисления, как мы помним из школьного курса химии, образуется оксид алюминия; и температура, при которой начинает плавиться это вещество, уже превышает две тысячи градусов.
Вообще избежать образования оксида не получится, если заниматься плавлением алюминия, но уменьшить количество лишнего вещества вполне возможно. При плавлении алюминия нужно не допускать попадания в вещество воды. Ведь если это случится, то произойдет взрыв.
Перед началом процесса нужно убедиться в том, что сырье является абсолютно сухим. Чаще всего в качестве исходного материала применяется алюминиевая проволока. Предварительно ее нужно с помощью ножниц разделить на множество мелких по длине кусочков. А для того, чтобы уменьшить площадь контакта с содержащимся в атмосфере кислородом, эти кусочки прессуются пассатижами.
Не всегда есть необходимость создать алюминиевое изделие высокого качества, поэтому вовсе не обязательно всегда использовать порошок или мелко нарезанную и плотно сдавленную проволоку. Можно взять любой предмет, который уже был использован, например, банку, в которой хранились консервы. Но перед плавкой нужно лишить ее нижнего шва или обрезать профиль. Полученное сырье может быть окрашено или испачкано. Не нужно об этом беспокоиться. Все, что имеется лишнее на поверхности, быстро отходит в виде шлаков.
Температура плавления чистого алюминия
Плавление алюминия, как и других веществ, происходит при подводе к нему тепловой энергии, снаружи или непосредственно в его объём, как это происходит, например, при индукционном нагреве.
Температура плавления алюминия зависит от его чистоты:
- Температура плавления сверхчистого алюминия 99,996 %: 660,37 °С.
- При содержании алюминия 99,5 % плавление начинается при 657 °С.
- При содержании алюминия 99,0 % плавление начинается при 643 °С.
Температура плавления металлов
Металлы и неметаллы
Любой кусок металла, например, алюминия, содержит миллионы отдельных кристаллов, которые называются зернами. Каждое зерно имеет свою уникальную ориентацию атомной решетки, но все вместе зерна ориентированы внутри этого куска случайным образом. Такая структура называется поликристаллической.
Аморфные материалы, например, стекло, отличаются от кристаллических материалов, например, алюминия, по двум важным отличиям, которые связаны друг с другом:
- отсутствие дальнего порядка молекулярной структуры
- различия в характере плавления и термического расширения.
Различие молекулярной структуры можно видеть на рисунке 1. Слева показана плотно упакованная и упорядоченная кристаллическая структура. Аморфный материал показан справа: менее плотная структура со случайным расположением атомов.

Рисунок 1 – Структура кристаллических (а) и аморфных (б) материалов.
Кристаллическая структура: упорядоченная, повторяющаяся и плотная,
аморфная структура – более свободно упакованная
с беспорядочным расположением атомов.Плавление металлов
Это различие в структуре проявляется при плавлении металлов, в том числе, плавлении алюминия различной чистоты и его сплавов. Менее плотно упакованные атомы дают увеличение объема (снижение плотности) по сравнению с тем же металлом в твердом кристаллическом состоянии.
Металлы при плавлении испытывают увеличение объема. У чистых металлов это объемное изменение происходит весьма резко и при постоянной температуре – температуре плавления, как это показано на рисунке 2. Это изменение представляет собой разрыв между наклонными линиями по обе стороны от точки плавления. Обе эти наклонные линии характеризуют температурное расширение металла, которое обычно является различным в жидком и твердом состоянии.

Рисунок 2 – Характерное изменение объема чистого металла
по сравнению с изменением объема аморфного материала [4]:
Tg – температура стеклования (перехода жидкого состояния в твердое);
Tm – температура плавленияТеплота плавления
С этим резким увеличением объема при переходе металла из твердого состояния в жидкое связано определенное количество тепла, которое называется скрытой теплотой плавления. Это тепло заставляет атомы терять плотную и упорядоченное кристаллическую структуру. Этот процесс является обратимым, он работает в обоих направлениях – и при нагреве, и при охлаждении.
Равновесная температура плавления
Как было показано выше, чистые кристаллические вещества, например, чистые металлы, имеют характерную температуру плавления, которую часто называют «точкой плавления». При этой температуре это чистое твердое кристаллическое вещество плавится и становится жидкостью. Переход между твердым и жидким состоянием для малых образцов чистых металлов настолько мал, что может измеряться с точностью 0,1 ºС.
Жидкости имеют характерную температуру, при которой они превращаются в твердое вещество. Эту температуру называют температурой затвердевания или точкой затвердевания. Теоретически – в равновесных условиях – равновесная температура плавления твердого вещества является той же самой, что и равновесная температура его затвердевания. На практике можно наблюдать небольшие различия между этими величинами (рисунок 3).

Рисунок 3 – Кривые охлаждения и нагрева чистого металла.
Видны явления переохлаждения при охлаждении и перегрева при нагреве.
В начале затвердевания наблюдается впадина на кривой охлаждения,
что объясняется замедленным началом кристаллизации [4]Температуры ликвидус и солидус
- Температура начала плавления называется температурой солидус (или точкой солидус)
- Температура окончания плавления – температурой ликвидус (или точкой ликвидус).
«Солидус» означает, понятно, твердый, а «ликвидус» – жидкий: при температуре солидуса весь сплав еще твердый , а при температуре ликвидуса – весь уже жидкий .
При затвердевании этого сплава из жидкого состояния температура начала кристаллизации (затвердевания) будет та же температурой ликвидус, а окончания кристаллизации – та же температура солидус. При температуре сплава между его температурами солидуса и ликвидуса он находится в полужидком-полутвердом, кашеобразном состоянии.
Плавление алюминия
Влияние легирующих элементов и примесей
Добавление в алюминий других элементов, в том числе легирующих, снижает температуру его плавления, точнее – начала его плавления. Так, у некоторых литейных алюминиевых сплавов с большим содержанием кремния и магния температура начала плавления снижается почти до 500 °С. Вообще, понятие «температура плавления» распространяется только на чистые металлы и другие кристаллические вещества. У сплавов же нет определённой температуры плавления: процесс их плавления (и затвердевания) происходит в некотором интервале температур.

Рисунок 4- Изменение удельного объема чистого металла (алюминия) и
сплава этого металла (алюминиевого сплава) [4]Интервалы температуры плавления
В таблице ниже представлены температуры ликвидуса и солидуса некоторых промышленных деформируемых сплавов. Необходимо иметь в виду, что понятия температур солидус и ликвидус определены для равновесных превращений жидкой фазы в твердую и обратно, то есть при бесконечной длительности процессов. На практике надо делать поправки с учетом скорости нагрева или охлаждения.
Плавление силумина
Не все сплавы имеют интервал между температурами солидус и ликвидус. Такие сплавы называют эвтектическим. Например, у алюминиевого сплава с содержанием 12,5 % кремния точки ликвидуса и солидуса сводятся в точку: этот сплав как и чистые металлы имеет не интервал, а точку плавления. Эта точка и температура называются эвтектическими. Этот сплав относится к знаменитым литейным алюминиево-кремниевым сплавам – силуминам с узким интервалом солидус-ликвидус, что и дает их лучшие литейные свойства.
В двойном сплаве Al-Si температура солидус постоянна и составляет 577 °С. При увеличении содержания кремния температура ликвидус снижается от максимального значения для чистого алюминия 660 °С и до совпадения с температурой солидуса 577 °С при содержании кремния 12,6 %.
Среди других легирующих элементов алюминия сильнее всего понижает температуру плавления магний: эвтектическая температура 450 °С достигается при содержании магния 18,9 %. Медь дает эвтектическую температуру 548 °С, а марганец – всего лишь 658 °С! Большинство сплавов являются не двойными, а тройными и даже четверными. Поэтому при совместном влиянии нескольких легирующих элементов температура солидуса – начала плавления или конца затвердевания может быть еще ниже.
Технология плавления алюминия в домашних условиях
Суть плавления состоит из нескольких этапов:
- Подготовка лома. В качестве исходного сырья используют профиль из алюминия, проволоку (ее предварительно уминают пассатижами), отслужившие детали. Кусочки должны быть небольшими. Краску, вкрапления других металлов из них не достают, все это будет в составе шлака.
- Подбор емкости, в которой можно плавить алюминий. Подойдет прочная посудина из стали (температура плавления 1300°С) или чугунок (1100°С), используют готовые огнеупорные тигли.
- Подготовка формы для расплава. В домашних условиях их делают самостоятельно. Процедура изготовления представлена ниже.
- Плавление лома. Предварительно определяют источник тепла.
- Снятие шлака, изготовление отливки. Самый простой способ плавки – аккуратно слить жидкий алюминий в подготовленную емкость или форму, шлак остается на стенках плавильной посудины. Чтобы он не прилип, требуется быстро ее охладить.
В принципе, технология промышленного и кустарного литья ничем не отличается. Лом плавят до состояния текучести. После этого отделяют расплав от шлака, сливают в заготовленные формы. Их после охлаждения отливки разбивают. Важно определить, что в результате должно получиться из жидкого алюминия. Даже если плавить металл решили ради эксперимента, емкость или форму для литья все равно необходимо приготовить. Тогда можно будет рассмотреть получившийся слиток, проверить его на пористость, чистоту, однородность структуры.
Оборудование и способы плавки
Прежде, чем плавить алюминий, выбирают место и способ разогрева металла. Два часто используемых варианта:
- В гаражах или домовладениях плавят алюминий, сооружается плавильня, ее составляют из кирпича без использования связующего раствора. В качестве опоры удобен металлический каркас, в нем должно быть отверстие для нагнетания воздуха, для этого используют пылесос или фен. Самодельная печь обкладывается углем. Емкость для плавления с ломом помещают внутрь. Для лучшего сохранения тепла кирпичи сверху накрывают листом металла.
- В домашних условиях для разогрева небольшого количества лома пользуются:
— газовой плитой, можно плавить небольшое количество лома, но выход расплава будет невысокий.
Литье плавят в стальной посуде. Для повышения скорости нагрева используют конструкцию из двух емкостей, их вставляют одна в другую с зазором 1 см. Дно большой посудины перфорируется, оно выполняет функцию пламярассекателя. Когда есть газовая горелка, совмещают нижний нагрев с верхним. Плавить металл можно быстрее.
Для небольших порций лома иногда используют жестяные банки. Но эта тара ненадежная, не исключено прогорание жести. Надежнее использовать керамический или металлический огнеупорный тигель для муфельных печей. Хороший вариант – обрезанный стакан огнетушителя. Для удобства делают желоб, по которому будет стекать расплавленный алюминий. При работе используют длинные щипцы. Понадобится ложка на длинной ручке для сбора шлака.
Как сделать форму для отливки
Перед тем, как расплавить алюминий, готовят болванку для отливки. Существует несколько способов заливки жидкого расплава. Чаще используют открытый и закрытый метод. О каждом стоит рассказать подробнее.
Открытая форма
Когда плавят алюминий по открытой методике, после плавления расплав выливают в подготовленную емкость, например, жестяную банку. Алюминиевую отливку вынимают из банки в горячем виде, когда горячий расплав немного схватится сверху. Достаточно несильно постучать по емкости. Если не нужен слиток заданной геометрии, расплавленный металл выливают на любую ровную огнеупорную поверхность, он хорошо держится, не растекается, внешне напоминает ртуть.
Закрытая форма
Сложные по геометрии отливки получают в специально приготовленных формах. Она должна соответствовать параметрам детали, обычно делается разъемной. Для изготовления формы используют деталь-макет, по которому делают отливку. В качестве формующего материала используют кремнезем, он хорошо трамбуется, его несложно найти. Кремнезем заменяют:
- смесью речного песка и жидкого стекла;
- смесь песка, цемента, вместо воды добавляют тормозную жидкость;
- гипс, он удобен для сложных макетов.
Из гипса делают сплошные бесшовные формы, они одноразовые, их после застывания алюминия разбивают. Деталь-макет изготавливают из воска или пенопласта. Его помещают внутрь емкости, используемой для формы, затем заливают пустоты. Получаются ровные детали, не требующие дополнительной обработки. Когда используется гипс, его сушат в течение пары дней. Гипс боится влаги, разбухает. Он склонен к растрескиванию при высыхании. При контакте с парафином или пенопластом гипс сохраняет свою структуру, не образуется рытвин, раковин.
Затвердевание алюминия
Чистый алюминий
Чистые металлы, в том числе, чистый алюминий, имеют четкую температуру плавления – точку плавления. Затвердевание или «замерзание» чистого алюминия происходит также при постоянной температуре. Когда чистый жидкий алюминий охлаждается, его температура падает до температуры затвердевания и остается при этой температуре, пока весь он (жидкий алюминий) не затвердеет. На рисунках 5 и 6 показаны типичные кривые охлаждения чистого металла с переходом его из жидкого состояния в твердое.

Рисунок 5 – Кривая охлаждения чистого металла (например, алюминия) [3]

Рисунок 6 – Затвердевание чистого алюминия [5]Алюминиевый сплав
При затвердевании алюминиевого сплава, который состоит из алюминия и растворенного в нем легирующего элемента, например, кремния или меди, то кривая охлаждение этого сплава показывает, что начало затвердевания происходит при одной температуре, а окончание – при другой температуре (рисунок 7).

Рисунок 7 – Кривая охлаждения сплава (например, алюминиевого сплава) [3]
Расплавление алюминиевых сплавов для литья
Для нагрева алюминиевого сплава до температуры жидкого состояния, при которой возможно выполнение операций литья, применяют плавильные печи различных видов. Тепловая энергия, которая требуется для того, чтобы нагреть металл до температуры жидкого состояния, при которой его можно разливать в литейные формы, состоит из суммы следующих компонентов:
- Теплота, чтобы поднять температуру металла до температуры плавления
- Теплота плавления, чтобы перевести металл из твердого состояния в жидкое состояние
- Теплота для нагрева расплавленного металла до заданной температуры разливки
Температура разливки – это температура расплавленного металла, при которой он заливается в литейную форму. Важным фактором здесь является разность между температурой разливки и температурой, при которой начинается затвердевание. Этой температурой является температура (точка) плавления для чистого алюминия или температура ликвидус для алюминиевого сплава. Эту разность температур иногда называют перегревом. Этот термин также может применяться для количества теплоты, которое надо отобрать от жидкого металла между разливкой и моментом начала затвердевания.
Применение металла в промышленном производстве
В естественных условиях алюминий имеет свойство образовывать тонкую оксидную пленку, что предотвращает реакции с водой и азотной кислотой (без нагрева). При разрушении пленки в результате контакта со щелочами химический элемент выступает в качестве восстановителя.
С целью предотвращения образования оксидной пленки в сплав добавляют другие металлы (галлий, олово, индий). Металл практически не подвергается коррозионным процессам. Он является востребованным материалом в различных отраслях промышленности.
Источник https://podyem.ru/metall/myagkie-metally-spisok.html
Источник https://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/fizicheskie-svoystva-metallov-tverdost-plotnost-i-dr/
Источник https://nashampure.ru/obrabotka-metalla/plavka/uchimsya-plavit-allyuminij
