Свойства алюминия
Основные физические свойства алюминия и алюминиевых сплавов, которые являются полезными для применения:
- или удельный вес; ;
- коэффициент теплового расширения;
- теплопроводность;
- электропроводность.
Эти свойства алюминия представлены ниже в таблицах [1]. Они могут рассматриваться только как основание для сравнения сплавов и их состояний и не должны применяться для инженерных расчетов. Они не являются гарантированными величинами, поскольку в большинстве случаев являются осредненными значениями для изделий с различными размерами, формами и методами изготовления. Поэтому они не могут быть в точности репрезентативными для изделий любых размеров и форм.
Номинальные величины плотности популярных алюминиевых сплавов представлены для отожженного состояния (О). Различия в плотности связаны с тем, что сплавы имеют различные легирующие элементы и в разных количествах: кремний и магний легче алюминия (2,33 и 1,74 г/см 3 ), а железо, марганец, медь и цинк – тяжелее (7,87; 7,40; 8,96 и 7,13 г/см 3 ).
О влиянии физических свойств алюминия и, в частности, его плотности, на конструкционные характеристики алюминиевых сплавов см. здесь.
Алюминий как химический элемент
- является третьим по распространенности – после кислорода и кремния – среди около 90 химических элементов, который обнаружены в земной коре.
- Среди элементов-металлов – он первый.
- Этот металл обладает многими полезными свойствами, физическими, механическими, технологическими – благодаря которым он широко применяется во всех сферах человеческой деятельности.
- Алюминий – это ковкий металл, который имеет серебристо-белый цвет и легко обрабатывается большинством методов обработки металлов давлением: прокаткой, волочением, экструзией (прессованием), ковкой.
- Его плотность – удельный вес – составляет около 2,70 граммов на кубический сантиметр.
- Чистый алюминий плавится при температуре 660 градусов Цельсия.
- Алюминий имеет относительно высокие коэффициенты теплопроводности и электропроводности.
- В присутствии кислорода всегда покрыт тонкой, невидимой пленкой оксида. Эта пленка является в значительной степени непроницаемой и имеет довольно высокие защитные свойства. Поэтому алюминий обычно демонстрирует стабильность и длительный срок службы при нормальных атмосферных условиях.
Комбинация свойств алюминия и его сплавов
Алюминий и его сплавы обладают уникальными комбинациями физических и других свойств. Это сделало алюминий одним из наиболее разносторонних, экономически выгодных и привлекательных конструкционных и потребительских материалов. Алюминий находит применение в очень широком диапазоне – от мягкой, очень пластичной упаковочной фольги до самых ответственных космических проектов. Алюминий по праву является вторым после стали среди многочисленных конструкционных материалов.
Низкая плотность
Алюминий – это один из самых легких промышленных конструкционных. Плотность алюминия приблизительно в три раза ниже, чем у стали или меди. Это физическое свойство обеспечивает ему высокую удельную прочность – прочность на единицу массы.
 Рисунок 1.1 – Объем единицы веса алюминия в сравнении с другими металлами [3]
Рисунок 1.1 – Объем единицы веса алюминия в сравнении с другими металлами [3]
 Рисунок 1.2 – Влияние легирующих элементов на
Рисунок 1.2 – Влияние легирующих элементов на
прочностные свойства, твердость,
хрупкость и пластичность [3]

Рисунок 1 – Прочность на единицу плотности алюминия в сравнении с различными металлами и сплавами [3]

Рисунок 2 – Кривые растяжения алюминия в сравнении с различными металлами и сплавами [3]
Поэтому алюминиевые сплавы широко применяют в транспортном машиностроении для увеличения грузоподъемности транспортных средств и экономии топлива.
- Паромные катамараны,
- нефтяные танкеры и
- самолеты –
вот лучшие примеры применения алюминия в транспорте.

Рисунок 3 – Плотность алюминия в зависимости от его чистоты и температуры [2]
Коррозионная стойкость
Алюминий имеет высокую коррозионную стойкость благодаря тонкому слою оксида алюминия на его поверхности. Эта оксидная пленка мгновенно образуется, как только свежая поверхность алюминия входит в контакт с воздухом (рисунок 4). Во многих случаях это свойство позволяет применение алюминия без какой-либо специальной обработки поверхности. Если требуется дополнительное защитное или декоративное покрытие, то применяют анодирование или окраску его поверхности.

Рисунок 4
а – естественное оксидное покрытие на сверхчистом алюминии;
б – коррозия алюминия чистотой 99,5 % с естественным оксидным покрытием
в коорозионно агрессивной среде [2]

Рисунок 5.1 – Влияние легирующих элементов на коррозионную стойкость и усталостную прочность [3]

Рисунок 5.2 – Точечная коррозия (питтинговая коррозия) алюминиевых листов
из сплава 3103 в различных коррозионных условиях [3]
Прочность
Прочностные свойства чистого алюминия являются довольно низкими (рисунок 6). Однако эти механические свойства могут возрастать очень сильно, если в алюминий добавляют легирующие элементы и, кроме того, его подвергают термическому (рисунок 6) или деформационному (рисунок 7) упрочнению.
Типичными легирующими элементами являются:
- марганец,
- кремний,
- медь,
- магний
- и цинк.

Рисунок 6 – Влияние чистоты алюминия на его прочность и твердость [2]

Рисунок 7 – Прочностные свойства высокочистых деформируемых
алюминиево-медных сплавов в различных состояниях [2]
(О – отожженный, W – сразу после закалки, Т4 – естественно состаренный, Т6 – искусственно состаренный)

Рисунок 8 – Механические свойства алюминия 99,50 %
в зависимости от степени полученной холодной деформации [2]

Рисунок 2 – Влияние легирующих элементов на плотность и модуль Юнга [3]
Прочность при низких температурах
Известно, что сталь становится хрупкой при низких температурах. Алюминий же, напротив, при низких температурах повышает свою прочность и сохраняет высокую вязкость. Именно это физическое свойство дало возможность его применения в космических аппаратах, которые работают в условиях космического холода.
Рисунок 9 – Изменение механические свойства алюминиевого сплава 6061
с понижением температуры
Теплопроводность
Алюминий проводит тепло в три раза быстрее, чем сталь. Это физическое свойство является очень важным в теплообменных аппаратах для нагрева или охлаждения рабочей среды. Отсюда – широкое применение алюминия и его сплавов в кухонной посуде, кондиционерах воздуха, примышленных и автомобильных теплообменниках.

Рисунок 10 – Теплопроводность алюминия в сравнении с другими металлами [3]
Отражательная способность
Алюминий является отличным отражателем лучистой энергии во всем интервале длин волн. Это физическое свойство позволяет применять его в приборах, которые работают от ультрафиолетового спектра через видимый спектр до инфракрасного спектра и тепловых волн, а также таких электромагнитных волн, как радиоволны и радарные волны [1].
Алюминий имеет способность отражать более 80 % световых волн, что обеспечивает ему широкое применение в осветительных приборах (рисунок 11). Благодаря этому физическому свойству он находит применение в теплоизоляционных материалах. Например, алюминиевая кровля отражает большую долю солнечного излучения, что обеспечивает в помещениях прохладную атмосферу летом и, в то же время, сохраняет тепло помещения зимой.

Рисунок 11 – Отражательные свойства алюминия [2]

Рисунок 12 – Отражательные свойства и эмиссивность алюминия с различной обработкой поверхности [3]

Рисунок 13 – Сравнение отражательных свойств различных металлов [3]
Электрические свойства
- Алюминий является одним из двух доступных металлов, которые имеют достаточно высокую электрическую проводимость, чтобы применять их в качестве электрических проводников.
- Электрическая проводимость «электрической» марки алюминия 1350 составляет около 62 % от международного стандарта IACS – электрической проводимости отожженной меди.
- Однако удельный вес алюминия составляет только треть от удельного веса меди. Это означает, что он проводит в два раза больше электричества, чем медь того же веса. Это физическое свойство обеспечивает алюминию широкое применение в высоковольтных линиях электропередачи (ЛЭП), трансформаторах, электрических шинах и цоколях электрических лампочек.

Рисунок 14 – Электрические свойства алюминия [3]
Магнитные свойства
Алюминий обладает свойством не намагничиваться в электромагнитных полях. Это делает его полезным при защите оборудования от воздействия электромагнитных полей. Другим применением этого свойства является компьютерные диски и параболические антенны.

Рисунок 15 – Намагничиваемость алюминиевого сплава AlCu [3]
Токсические свойства
Это свойство алюминия – отсутствие токсичности – было обнаружено еще в начале его промышленного освоения. Именно это свойство алюминия дало возможность его применения для изготовления кухонной посуды и приборов без какого-либо вредного воздействия для тела человека. Алюминий со своей гладкой поверхностью легко поддается чистке, что важно для обеспечения высокой гигиены при приготовлении пищи. Алюминиевая фольга и контейнеры широко и безопасно применяются при упаковке с прямым контактом с продуктами.
Звукоизоляционные свойства
Это свойство алюминия дает ему применение при выполнении звукоизоляции потолков.
Способность поглощать энергию удара
Алюминий имеет модуль упругости в три раза меньший, чем у стали. Это физическое свойство дает большое преимущество для изготовления автомобильных бамперов и других средств безопасности автомобилей.

Рисунок 16 – Автомобильные алюминиевые профили
для поглощения энергии удара при аварии
Пожаробезопасные свойства
Алюминиевые детали не образует искр при ударе друг о друга, а также другие цветные металлы. Это физическое свойство находит применение при повышенных мерах пожарной безопасности конструкций, например, на морских нефтяных вышках.
Вместе с тем, с повышением температуры выше 100 градусов Цельсия прочность алюминиевых сплавов значительно снижается (рисунок 17).

Рисунок 17 – Прочность при растяжении алюминиевого сплава 2014-Т6
при различных температурах испытания [3]
Технологические свойства
Легкость, с которой алюминий может быть переработан в любую форму – технологичность, является одним из наиболее важных его достоинств. Очень часто он может успешно конкурировать с более дешевыми материалами, которые намного труднее обрабатывать:
- Этот металл может быть отлит любым методом, который известен металлургам-литейщикам.
- Он может прокатан до любой толщины вплоть до фольги, которая тоньше листа бумаги.
- Алюминиевые листы можно штамповать, вытягивать, высаживать и формовать всем известными методами обработки металлов давлением.
- Алюминий можно ковать всеми методами ковки
- Алюминиевая проволока, которую волочат из круглого прутка, может затем сплетаться в электрические кабели любого размера и типа.
- Почти не существует ограничений формы профилей, в которые получают из этого металла методом экструзии (прессования).

Рисунок 18.1 – Литье алюминия в песчаную форму

Рисунок 18.2 – Непрерывная разливка-прокатка алюминиевой полосы [5]

Рисунок 18.3 – Операция высадки при изготовлении алюминиевых банок [4]
 Рисунок 18.4 – Операция ковки алюминия
Рисунок 18.4 – Операция ковки алюминия

Рисунок 18.5 – Холодное волочение алюминия

Рисунок 18.6 – Прессование (экструзия) алюминия
- .
- A. Sverdlin Properties of Pure Aluminum // Handbook of Aluminum, Vol. 1 /ed. G.E. Totten, D.S. MacKenzie, 2003
- TALAT 3710
- />← Previous Technical Brochures
- Применение алюминия Next → />
Алюминий: свойства, применение, виды, способы получения

Алюминий – металлический элемент серебристо-белого цвета, его механические характеристики и технологические свойства обеспечивают широкое применение в различных отраслях промышленности, строительстве и быту.
Алюминий сочетает малую плотность и прочность, устойчивость к коррозии и резким температурным перепадам. В периодической таблице Менделеева обозначается как Al, атомный номер – 13. Этот элемент распространен в земной коре, по содержанию в ней занимает третье место после кислорода и кремния. В недрах его содержится примерно 8%. Для сравнения – золото в земной коре присутствует в количестве, равном всего миллионным долям процента.
Технологии промышленного получения алюминия
Впервые о существовании этого металла в 16 веке догадался Парацельс, выделивший из квасцов «квасцовую землю». В нейон выявил оксид неизвестного на тот момент металла, очень заинтересовавший ученого. В 18 веке его опыты повторил немецкий химик Маргграф, который и дал имя новому элементу. В переводе с латыни переводится как «вяжущий». Только в конце позапрошлого века был найден экономически выгодный способ промышленного получения алюминия.
Чаще всего этот металл получают из бокситов –вторичных пород. Они образовались при распаде алюмосиликатов первичного происхождения, которые, в свою очередь, сформировались в высокотемпературных условиях вулканических извержений. В России алюминий выделяют из нефелиновых руд, добываемых на Кольском полуострове и в Кемеровской области. Вторичные продукты добычи Al из нефелиновых руд: портландцемент, сода, удобрения.
Популярная технология получения глинозема (оксида алюминия) из бокситов – щелочной метод Байера, разработанный российскими учеными в конце 19 века. Полученный в результате этого процесса оксид Al2O3 – прочное химическое соединение, плавящееся при +2050°C. Металл в чистом виде получают электролизным восстановлением оксида. ОсобочистыйAlполучают трехслойным электролизом. Дополнительную очистку, если такая требуется, проводят рафинирующим электролизом с электролитом из алюмоорганических соединений, а также с помощью зонного плавления или дистилляции через субфторид.
Основные свойства алюминия
Этот элемент химически активен, но образующаяся на его поверхности плотная оксидная пленка защищает полуфабрикаты и готовые изделия от коррозионного разрушения.
Для алюминия характерны следующие физические свойства:
- плотность – 2,7 г/см 3 (для сравнения – плотность железа составляет 7,85 г/см 3 );
- температура плавления +600°C (железа+1535°C);
- высокие электро- и теплопроводность;
- парамагнетизм – металл притягивается магнитом исключительно при наличии магнитного поля;
- объемная гранецентрированная металлическая кристаллическая решетка.
Основные естественные примеси, присутствующие в Al после восстановления из оксида (кремний, цинк, титан, железо, медь), влияют на физические и технологические параметры металла. Чем он чище, тем выше его электропроводность, теплопроводность, коррозионная стойкость и, конечно, цена. Основные механические параметры: предел прочности после холодного пластического деформирования– 150 МПа, относительное удлинение – 50%.
Alлегко формуется, поддается механической обработке, сваривается различными видами сварки. Для повышения коррозионной стойкости поверхность деталей и конструкций анодируют. Анодирование – электрохимический процесс создания толстой оксидной пленки.
Химические характеристики металла алюминия:
- Химическая активность. В мелкофракционном состоянии при высоких температурах Al активно соединяется с кислородом, фосфором, серой, азотом, йодом, углеродом. При комнатных температурах реагирует с бромом, хлором, щелочами.
- Взаимодействие с другими металлами с образованием сплавов, содержащих алюминиды, – интерметаллические соединения.
- При наличии на поверхности плотной оксидной пленки –стойкость к атмосферной коррозии, пресной и соленой воде, инертность к органическим кислотам, разбавленной и концентрированнойHNO3. При очищенной оксидной пленке этот металл активно вступает в реакцию с водой.
Виды алюминия по степени очистки
В зависимости от процентного содержания основного элемента принята следующая классификация степеней чистоты:
- 99,5-99,79% – промышленная чистота (техническая);
- 99,8-99,949% – высокочистая;
- 99,95-99,9959% – сверхчистая;
- 99, 9960-99,9990 % – особо чистая;
- свыше 99,999% – ультрачистая.
Алюминий технической чистоты имеет широкое применение в промышленности, где важны его главные физические свойства – небольшая плотность, электро- и теплопроводимость. Он выпускается в виде алюминиевых листов, труб, плит, прутков, профильного проката. Их применяют для изготовления деталей и элементов конструкций, не запланированных для значительных нагрузок. Из высокоочищенных материалов выпускают фольгу и токопроводящие элементы.
Виды алюминиевых сплавов
Основная область применения алюминия– производство сплавов, которые разделяют на деформируемые и литейные.
Деформируемые
Такие марки хорошо обрабатываются на всех стадиях обработки, сочетают прочность и пластичность. Используется при производстве листов, прутков, труб, поковок, штамповок. Применяемые способы деформирования: прокатка, волочение, прессование, ковка. По способности повышать прочностные характеристики деформируемые материалы на базе алюминия подразделяют на термически неупрочняемые и термически упрочняемые.
Популярный сплав, относящийся к этой группе, – дюралюминAl-Cu-Mg, в который дополнительно вводится марганец, повышающий устойчивость к коррозии. Если ранее наиболее распространенным был материал Д1, то постепенно его заменила более технологичная марка Д16. В Евросоюзе и США используются марки 2017, 2024, 2117.Дюралюмин, выпускаемый в листах, для дополнительного улучшения коррозионной стойкости плакируют – покрывают поверхность слоем чистого Al.
Еще один представитель этой группы – авиаль (АВ), материал, используемый в авиастроении. Он немного уступает по прочности дюралюминам, но превышает их по пластичности в нормальном и нагретом состояниях. Удовлетворительно обрабатывается режущими инструментами, сваривается аргонодуговой и контактной сваркой.
Высокопрочные сплавы на основе алюминия обладают повышенными прочностными свойствами, но меньшей пластичностью по сравнению с дюралюминами. Марка В95широко применяется в самолетостроении для конструкций, эксплуатируемых при температурах выше +100°C. Хорошо сваривается точечной сваркой и обрабатывается режущими инструментами.
Литейные
Алюминиевые сплавы для фасонного литья отличаются жидкотекучестью, небольшой усадкой, стойкостью к образованию горячих трещин, коррозии. Количество легирующих элементов в таких материалах выше, чем в деформируемых. Наиболее распространены композиции Al-Si, Al-Cu, Al-Mg, дополнительно легированные небольшими количествами марганца, хрома, никеля.
Примеры использования алюминия и его сплавов при производстве различных видов транспорта
Современные отрасли транспортостроения невозможно представить без материалов, созданных на основе Al, которые сочетают достаточно высокую прочность, пластичность, малую плотность и хорошую устойчивость ко многим видам коррозии.
Самолетостроение
В РФ при создании авиационной техники широко используют тремоупрочняемые высокопрочные марки, содержащие, помимо AL, цинк, магний, медь. Марки повышенной прочности и среднепрочные, не имеющие в своем составе цинка, используются для изготовления киля, крыла, фюзеляжа. Для гидросамолетов востребованы магнийсодержащие марки АМг5, АМг6 с хорошей свариваемостью и марки В92, 1915, 1420.
Создание объектов космической техники
В этой области используют сплавы на основе алюминия, обладающие хорошей устойчивостью к низким температурам. Из марки 2219, способной работать при криогенных температурных условиях в контакте с жидким кислородом, гелием, водородом, изготавливались листы, применяемые при создании космических «Шаттлов». Из алюминиево-литиевой марки 2090 изготавливают емкости для жидкого водорода.
Судостроение
Алюминиевая промышленность изготавливает полуфабрикаты из алюминия и его сплавов для использования в судостроении. Из них производят судовое оборудование, корпуса судов, коммуникационные системы, надстройки для палубы. Применение этих материалов вместо стали уменьшает массу судна, улучшает его маневренность и максимально допустимую скорость. Чаще всего в этой отрасли востребованы магний- и марганецсодержащие марки.
Железнодорожный транспорт
Подвижной состав, эксплуатируемый на железной дороге, изготавливается только из прочных, износостойких, коррозионностойких, долговечных материалов. Такие свойства имеют алюминий и сплавы на его основе. Из них изготавливают емкости для перевозки сырой нефти, темных и светлых нефтепродуктов, масел.
Автомобильный транспорт
Сочетание небольшой плотности, прочности, декоративных характеристик и коррозионной устойчивости позволяет успешно использовать алюминиевые марки в автомобилестроении. Их применение расширяет ассортимент перевозимых товаров, среди которых могут быть жидкости и газы высоких классов опасности.
Применение алюминия в металлургии
Алюминий – высокоактивный металл, поэтому его используют в металлургии в качестве мощного восстановителя при производстве хрома, кальция, марганца. Для раскисления стали используется низкокачественный материал, не подходящий для производства полуфабрикатов и готовой металлопродукции. В ходе этого процесса из расплавленного железа удаляется кислород, негативно влияющий на эксплуатационные свойства конечного продукта.
Алюминий – общая характеристика элемента, химические свойства
В 16 веке знаменитый Парацельс сделал первый шаг к добыче алюминия. Из квасцов он выделил «квасцовую землю», которая содержала оксид неизвестного тогда металла. В 18 веке к этому эксперименту вернулся немецкий химик Андреас Маргграф. Оксид алюминия он назвал «alumina», что на латинском языке означает «вяжущий». На тот момент металл не пользовался популярностью, так как не был найден в чистом виде.
Долгие годы выделить чистый алюминий пытались английские, датские и немецкие учёные. В 1855 году в Париже на Всемирной выставке металл алюминий произвёл фурор. Из него делали только предметы роскоши и ювелирные украшения, так как металл был достаточно дорогим. В конце 19 века появился более современный и дешёвый метод получения алюминия. В 1911 году в Дюрене выпустили первую партию дюралюминия, названного в честь города. В 1919 из этого материала был создан первый самолёт.
Распространенность в природе
По степени распространенности в земле алюминий занимает лидирующую позицию среди всех металлов и третью между элементами периодической таблицы. По исследованиям разных ученых его концентрация в почве колеблется от 7,4 до 8,1%. Молярная масса атома — 26,9815386 г/моль. У вещества высокая химическая активность, поэтому чаще всего оно встречается в виде соединений.
К природным минералам алюминия относятся:
- хризоберилл или александрит;
- бокситы;
- берилл, аквамарин, изумруд;
- нефелины;
- каолинит;
- алуниты;
- полевые шпаты;
- глиноземы — смесь каолинов с песком, магнезитом или известняком.
Но в специфических условиях — жерлах вулканов, например, есть незначительное количество самородного металла белого цвета. Содержат его и природные воды, но вещество приобретает вид малотоксичных соединений. Тип аниона или катиона зависит только от кислотности окружающей среды.
В составе алюминия есть радиоактивные изотопы, которые распадаются за 720 000 лет. Образуются они при расщеплении высокоэнергичными космическими лучами ядер аргона.
Строение атома
Алюминий – это 13 элемент периодической таблицы. Он находится в третьем периоде, III группе, главной подгруппе.
Свойства и применение алюминия связаны с его электронным строением. Атом алюминия имеет положительно заряженное ядро (+13) и 13 отрицательно заряженных электронов, располагающихся на трёх энергетических уровнях. Электронная конфигурация атома – 1s22s22p63s23p1.
На внешнем энергетическом уровне находится три электрона, которые определяют постоянную валентность III. В реакциях с веществами алюминий переходит в возбуждённое состояние и способен отдавать все три электрона, образуя ковалентные связи. Как и другие активные металлы, алюминий является мощным восстановителем.
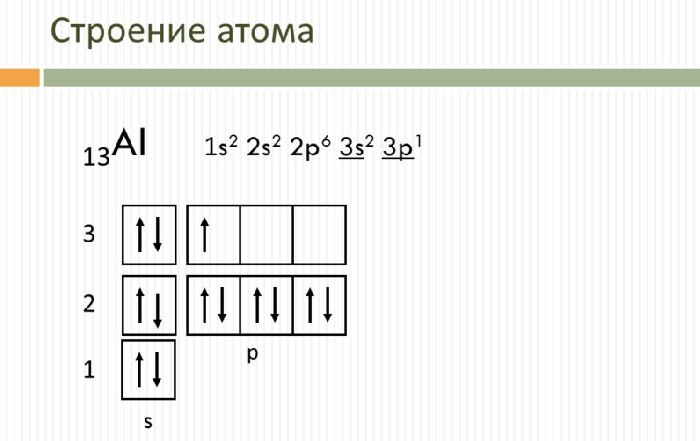
Рис. 1. Строение атома алюминия.
Алюминий – амфотерный металл, образующий амфотерные оксиды и гидроксиды. В зависимости от условий соединения проявляют кислотные или основные свойства.
Месторождения и методы добычи
Главное сырье для получения алюминия – бокситы. Их залежи сосредоточены в тропиках и субтропиках.
Россия богата нефелиновыми рудами, источник которых – север страны (Кольский полуостров и Кемеровская область).
Мировые запасы сырья исчисляются миллионами тонн.
Добыча ведется открытым либо закрытым способом.
Химические свойства
Алюминий — серебристо-белый легкий металл, технический состав плавится при температуре 658 градусов, чистый — при 660, а закипает он при 2518, 8. К физическим свойствам относится и пластичность. Она у вещества очень высокая: 35% и 50% у промышленного и природного сплава соответственно. Его можно раскатать до состояния фольги или тонкого листа.
Модуль Юнга у алюминия составляет 70 ГПа, коэффициент Пуассона — 0,34. Он отлично отражает свет, проводит тепло и электричество. Вещество может взаимодействовать практически со всеми металлами, образует сплавы с кремнием, магнием, медью.
В нормальных условиях алюминий покрыт прочной тонкой оксидной пленкой, поэтому на него не действуют обычные окислители. Но он реагирует на разбавленные серные растворы.
Металлу не опасна коррозия, благодаря чему он нашел широкое применение в промышленности.
Но если пленка разрушилась — ее могут повредить соли аммония, горячие щелочи или амальгамирование, то вещество превращается в восстановитель. Галий, олово и индий не дают ей образоваться, при этом поверхность металла нужно покрыть легкоплавкими эвтектиками.
Перечень того, с чем реагирует алюминий:
- кислородом;
- галогенами;
- неметаллами;
- водой и ее парами;
- щелочами;
- соляной, азотной и серной кислотами.
При реакции с кислородом образуется оксид алюминия, его формула — 4Al + 3O2 = 2Al2O3. Фторид вещества: 2Al + 3F2 = 2AlF3. Сульфид образуется при взаимодействии с серой: 2Al + 3S = Al2S3, 2Al + N2 = 2AlN — это нитрид металла, 4Al + 3C = Al4C3 — карбид после реакции с углеродом.
Характерная степень окисления алюминия — плюс три, но его атомы могут образовывать дополнительные связи. При взаимодействии со щелочами образуется тетрагидроксоалюминат (или другие алюминаты): 2Al + 2NaOH + 6H2O = 2Na (Al (OH)4) + 3H2. Металл можно растворить в разбавленной серной кислоте: 2Al + 3H2SO4 = Al2 (SO 4)3 + 3H2.
Интересна реакция алюминия с водой. Для нее необходимо удалить защитную пленку с помощью раствора горячей щелочи или амальгамы: 2Al + 6H2O = 2Al (OH3) + 3H2. При взаимодействии с окислителями происходит разложение вещества: 2Al + 6H2SO4 = Al2 (SO4)3 + 3SO2 + 6H2O — растворимые соли, уравнение реакций. Химические свойства алюминия включают восстановление металлов из оксидов, реакцию с парами воды.
Физическое описание
- лёгкостью (плотность 2,7 г/см3);
- серебристо-серым цветом;
- высокой электропроводностью;
- ковкостью;
- пластичностью;
- температурой плавления – 658°C;
- температурой кипения – 2518,8°C.
Из металла делают жестяные ёмкости, фольгу, проволоку, сплавы. Алюминий используют при изготовлении микросхем, зеркал, композитных материалов.

Рис. 2. Жестяные ёмкости.
Алюминий – парамагнетик. Металл притягивается магнитом только в присутствии магнитного поля.
Получение
Алюминий находится на первом месте среди металлов и на третьем среди всех элементов по распространённости в земной коре. Приблизительно 8% массы земной коры составляет именно этот металл. Алюминий содержится в тканях животных и растений в качестве микроэлемента. В природе он встречается в связанном виде в форме горных пород, минералов. Каменная оболочка земли, находящаяся в основе континентов, формируется именно алюмосиликатами и силикатами.
Алюмосиликаты – это минералы, образовавшиеся в результате вулканических процессов в соответствующих условиях высоких температур. При разрушении алюмосиликатов первичного происхождения (полевые шпаты) сформировались разнообразные вторичные породы с более высоким содержанием алюминия (алуниты, каолины, бокситы, нефелины). В состав вторичных пород алюминий входит в виде гидроокисей или гидросиликатов. Однако не каждая алюминийсодержащая порода может быть сырьём для глинозёма – продукта, из которого при помощи метода электролиза получают алюминий.
Наиболее часто алюминий получают из бокситов. Залежи этого минерала распространены в странах тропического и субтропического пояса. В России также применяются нефелиновые руды, месторождения которых располагаются в Кемеровской области и на Кольском полуострове. При добыче алюминия из нефелинов попутно также получают поташ, кальцинированную соду, цемент и удобрения.
В бокситах содержится 40-60% глинозёма. Также в составе имеются оксид железа, диоксид титана, кремнезём. Для выделения чистого глинозёма используют процесс Байера. В автоклаве руду нагревают с едким натром, охлаждают, отделяют от жидкости «красный шлам» (твёрдый осадок). После осаждают гидроокись алюминия из полученного раствора и прокаливают её для получения чистого глинозёма. Глинозём должен соответствовать высоким стандартам по чистоте и размеру частиц.
Из добытой и обогащённой руды извлекают глинозём (оксид алюминия). Затем методом электролиза глинозём превращают в алюминий. Заключительным этапом является восстановление процессом Холла-Эру. Процесс заключается в следующем: при электролизе раствора глинозёма в расплавленном криолите происходит выделение алюминия. Катодом служит дно электролизной ванны, а анодом – угольные бруски, находящиеся в криолите. Расплавленный алюминий осаждается под раствором криолита с 3-5% глинозёма. Температура процесса поднимается до 950°С, что намного превышает температуру плавления самого алюминия (660°С). Глубокую очистку алюминия проводят зонной плавкой или дистилляцией его через субфторид.
Применение алюминия
Еще Д.И.Менделеев писал, что «металлический алюминий, обладая большою легкостью и прочностью и малою изменчивостью на воздухе, очень пригоден для некоторых изделий». Алюминий – один из самых распространенных и дешевых металлов. Без него трудно представить себе современную жизнь. Недаром алюминий называют металлом 20 века. Он хорошо поддается обработке: ковке, штамповке, прокату, волочению, прессованию. Чистый алюминий – довольно мягкий металл; из него делают электрические провода, детали конструкций, фольгу для пищевых продуктов, кухонную утварь и «серебряную» краску. Этот красивый и легкий металл широко используют в строительстве и авиационной технике. Алюминий очень хорошо отражает свет. Поэтому его используют для изготовления зеркал – методом напыления металла в вакууме.
В авиа- и машиностроении, при изготовлении строительных конструкций, используют значительно более твердые сплавы алюминия. Один из самых известных – сплав алюминия с медью и магнием (дуралюмин, или просто «дюраль»; название происходит от немецкого города Дюрена). Этот сплав после закалки приобретает особую твёрдость и становится примерно в 7 раз прочнее чистого алюминия. В то же время он почти втрое легче железа. Его получают, сплавляя алюминий с небольшими добавками меди, магния, марганца, кремния и железа. Широко распространены силумины – литейные сплавы алюминия с кремнием. Производятся также высокопрочные, криогенные (устойчивые к морозам) и жаропрочные сплавы. На изделия из алюминиевых сплавов легко наносятся защитные и декоративные покрытия. Легкость и прочность алюминиевых сплавов особенно пригодились в авиационной технике. Например, из сплава алюминия, магния и кремния делают винты вертолетов. Сравнительно дешевая алюминиевая бронза (до 11% Al) обладает высокими механическими свойствами, она устойчива в морской воде и даже в разбавленной соляной кислоте. Из алюминиевой бронзы в СССР с 1926 по 1957 чеканились монеты достоинством 1, 2, 3 и 5 копеек.
В настоящее время четвертая часть всего алюминия идет на нужды строительства, столько же потребляет транспортное машиностроение, примерно 17% часть расходуется на упаковочные материалы и консервные банки, 10% – в электротехнике.
Алюминий содержат также многие горючие и взрывчатые смеси. Алюмотол, литая смесь тринитротолуола с порошком алюминия, – одно из самых мощных промышленных взрывчатых веществ. Аммонал – взрывчатое вещество, состоящее из аммиачной селитры, тринитротолуола и порошка алюминия. Зажигательные составы содержат алюминий и окислитель – нитрат, перхлорат. Пиротехнические составы «Звездочки» также содержат порошкообразный алюминий.
Смесь порошка алюминия с оксидами металлов (термит) применяют для получения некоторых металлов и сплавов, для сварки рельсов, в зажигательных боеприпасах.

Алюминий нашел также практическое применение в качестве ракетного топлива. Для полного сжигания 1 кг алюминия требуется почти вчетверо меньше кислорода, чем для 1 кг керосина. Кроме того, алюминий может окисляться не только свободным кислородом, но и связанным, входящим в состав воды или углекислого газа. При «сгорании» алюминия в воде на 1 кг продуктов выделяется 8800 кДж; это в 1,8 раза меньше, чем при сгорании металла в чистом кислороде, но в 1,3 раза больше, чем при сгорании на воздухе. Значит, в качестве окислителя такого топлива можно использовать вместо опасных и дорогостоящих соединений простую воду. Идею использования алюминия в качестве горючего еще в 1924 предложил отечественный ученый и изобретатель Ф.А.Цандер. По его замыслу можно использовать алюминиевые элементы космического корабля в качестве дополнительного горючего. Этот смелый проект пока практически не осуществлен, зато большинство известных в настоящее время твердых ракетных топлив содержат металлический алюминий в виде тонкоизмельченного порошка. Добавление 15% алюминия к топливу может на тысячу градусов повысить температуру продуктов сгорания (с 2200 до 3200 К); заметно возрастает и скорость истечения продуктов сгорания из сопла двигателя – главный энергетический показатель, определяющий эффективность ракетного топлива. В этом плане конкуренцию алюминию могут составить только литий, бериллий и магний, но все они значительно дороже алюминия.
Широкое применение находят и соединения алюминия. Оксид алюминия – огнеупорный и абразивный (наждак) материал, сырье для получения керамики. Из него также делают лазерные материалы, подшипники для часов, ювелирные камни (искусственные рубины). Прокаленный оксид алюминия – адсорбент для очистки газов и жидкостей и катализатор ряда органических реакций. Безводный хлорид алюминия – катализатор в органическом синтезе (реакция Фриделя – Крафтса), исходное вещество для получения алюминия высокой чистоты. Сульфат алюминия применяют для очистки воды; реагируя с содержащимся в ней гидрокарбонатом кальция:
Al2(SO4)3 + 3Ca(HCO3)2 ® 2AlO(OH) + 3CaSO4 + 6CO2 + 2H2O, он образует хлопья оксида-гидроксида, которые, оседая, захватывают, а также сорбируют на поверхности находящиеся в воде взвешенные примеси и даже микроорганизмы. Кроме того, сульфат алюминия применяют как протраву при крашении тканей, для дубления кожи, консервирования древесины, проклеивания бумаги. Алюминат кальция – компонент вяжущих материалов, в том числе портландцемента. Иттрий-алюминиевый гранат (ИАГ) YAlO3 – лазерный материал. Нитрид алюминия – огнеупорный материал для электропечей. Синтетические цеолиты (они относятся к алюмосиликатам) – адсорбенты в хроматографии и катализаторы. Алюминийорганические соединения (например, триэтилалюминий) – компоненты катализаторов Циглера – Натты, которые используются для синтеза полимеров, в том числе синтетического каучука высокого качества.
Рассмотрим, как используют различные изделия из алюминия
Алюминиевая лента представляет собой тонкую алюминиевую полосу толщиной 0,3-2 мм, шириной 50-1250 мм, которая поставляется в рулонах. Используется лента в пищевой, лёгкой, холодильной промышленности для изготовления охлаждающих элементов и радиаторов.
Круглая алюминиевая проволока применяется для изготовления кабелей и проводов для электротехнических целей, а прямоугольная для обмоточных проводов.
Алюминиевые трубы отличаются долговечностью и стойкостью в условиях сельских и городских промышленных районов. Применяются они в отделочных работах, дорожном строительстве, конструкции автомобилей, самолётов и судов, производстве радиаторов, трубопроводов и бензобаков, монтаже систем отопления, магистральных трубопроводов, газопроводов, водопроводов.
Алюминиевые втулки характеризуются простотой в обработке, монтаже и эксплуатации. Используются они для концевого соединения металлических тросов.
Алюминиевый круг — это сплошной профиль круглого сечения. Используется это изделие для изготовления различных конструкций.
Алюминиевый пруток применяется для изготовления гаек, болтов, валов, крепежных элементов и шпинделей.
Около 3 мг алюминия каждый день поступает в организм человека с продуктами питания. Больше всего металла в овсянке, горохе, пшенице, рисе. Учёными установлено, что он способствует процессам регенерации, стимулирует развитие и рост тканей, оказывает влияние на активность пищеварительных желёз и ферментов.
При использовании алюминиевой посуды в быту необходимо помнить, что хранить и нагревать в ней можно исключительно нейтральные жидкости. Если же в такой посуде готовить, к примеру, кислые щи, то алюминий поступит в еду, и она будет иметь неприятный «металлический» привкус.
Алюминий входит в состав лекарственных препаратов, используемых при заболеваниях почек и желудочно-кишечного тракта.
Отличия алюминиевых сплавов
Сплавы АД1 представляют собой технический алюминий, содержат до 0,7% примесей, среди которых главная роль принадлежит кремнию и железу. Они стойкие к воздействиям химических веществ. Подходят в качестве материалов для резервуаров, прокладок, шайб. АД31 склонен к упрочнению при термической обработке, содержит: Al, Mg, Si. Имеет высокую пластичность, не подвержен ржавчине. Из него получаются сложные по форме полуфабрикаты. Он прост в обработке, хорошо поддается окрашиванию. Из него получают профили, емкости для перевозки азотной кислоты, продуктов питания. Также он является материалом для фляг, консервных банок, пробок бутылок.
В сплаве В95, помимо Al, присутствует цинк, магний и медь. Самый прочный среди всех разновидностей, поэтому востребован в конструкциях с высокой нагрузкой. Из него выпускают плиты, ленты, профили. Под точечной нагрузкой склонен к коррозийному разрушению.
Д16 очень распространен, представляет алюминиевый сплав с медью и магнием. Его можно деформировать в холодном и горячем состоянии. Не предназначен для сваривания. Сплав Д16т – дюралюминий, востребованный в авиа и судостроении. В три раза легче стали, не подвержен микроскопической деформации. Хорошо обрабатывается на токарных станках. Буква Т обозначает, что он искусственно состаренный. В таком состоянии он очень прочный, не подвержен коррозийному влиянию.
Под обозначением АМГ следует понимать алюминиево-магниевые сплавы. Не упрочняются термической обработкой. Незаменимы в технологиях глубокой штамповки. Морозоустойчивы, пластичны. Цифры, следующие за буквенными обозначениями, указывают на количество магния.
Сплав А5 – первичный алюминий, из которого делают проволоку, фольгу, слитки.
АМЦ содержит алюминий и марганец. Пластичный, но малопрочный. Среди достоинств таких сплавов – стойкость к коррозии, способность без труда свариваться контактной, газовой, атомно-водородной сваркой. Склонны к деформации как в холодном, так и в горячем состоянии в пределах 320-470 ° C.
Предостережение
Алюминий не заложен изначально в биологические организмы. Но человек получает его микродозы ежедневно – с пищей.
Им богаты горох, пшеница, рис, овсяный «геркулес». Доказана польза алюминия как стимулятора регенерации, развития тканей, работы ЖКТ, ферментов.
Однако его переизбыток (откладывается в костях, мозге, печени, почках) чреват тяжелыми расстройствами нервной системы.
По стандартам РФ, в литре питьевой воды не должно быть более 0,2 мг алюминия.
Алюминиевой посудой пользоваться можно, но ограниченно. Безопасны готовка, подогрев, хранение продуктов с нейтральными характеристиками. Приготовление кислых блюд (щи, томат, компот) опасно. Алюминий поступит в еду, создавая избыточную дозу при попадании в организм, плюс «железный» привкус.
Источник https://aluminium-guide.com/fizicheskie-xarakteristik-deformiruemyx-alyuminievyx-splavov/
Источник https://www.adamantsteel.ru/info/articles/vse-ob-alyuminii/
Источник https://chimical-docs.ru/alyuminij-obshhaya-harakteristika-elementa-himicheskie-svojstva/

